大黄通便颗粒中大黄的含量测定研究
2011-07-25陈邦恩刘美龙
陈邦恩,刘美龙
(福建生物工程职业技术学院,福建 福州 350001)
大黄通便颗粒主要是由大黄等中药组成,具有清热通便的功效,临床常用于治疗实热食滞、便秘以及湿热型食欲不振等。大黄为其方中主药,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚为其所含的主要有效成分,故本研究参考中国药典2010年版一部大黄药材[1]及文献报道的含量测定方法,建立高效液相色谱法测定芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量,并对方法学进行了考察,该方法简便,可行,重复性好。
1 仪器和试药
1.1 仪器
Agilent 1200液相色谱仪;超纯水器(MILLI-Q);KQ-500VDB型三频数控超声波清洗器(奥特宝恩斯仪器有限公司)。
1.2 试药
对照品:芦荟大黄素对照品(含量以98.0%计,购自中国药品生物制品检定所,批号:110795-201007);大黄酸对照品(供含量测定用,购自中国药品生物制品检定所,批号:0757-200206);大黄素对照品(供含量测定用,购自中国药品生物制品检定所,批号:110756-200110);大黄酚对照品(供含量测定用,购自中国药品生物制品检定所,批号:110796-200514);大黄素甲醚对照品(含量以99.8%计,购自中国药品生物制品检定所,批号:110758-201013)。样品:大黄通便颗粒(江苏辰牌药业有限公司,批号:110118、110307、110316)以及阴性样品。试剂:甲醇为色谱纯,磷酸为分析纯,提取用的甲醇、二氯甲烷为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:XB-C18(5μm,4.6mm×250mm);流动相:甲醇-0.1%磷酸溶液(85:15);检测波长为254nm;理论塔板数按大黄素峰计算应不低于3000。
2.2 溶液的制备
2.2.1 对照品溶液的制备
精密称取芦荟大黄素对照品、大黄酸对照品、大黄素对照品、大黄酚对照品和大黄素甲醚对照品适量,加10%二氯甲烷的甲醇溶液溶解,分别制成每1mL含芦荟大黄素、大黄酸、大黄素、大黄酚各100μg,大黄素甲醚50μg的溶液;分别精密量取上述对照品溶液各1mL,置同一25mL量瓶中,加10%二氯甲烷的甲醇溶液定溶至刻度,摇匀,即得。
2.2.2 供试品溶液制备
取本品粉末(过四号筛)约2g,精密称定,置具塞锥形瓶中,精密加入甲醇25mL,密塞,称定重量,加热回流45min,放冷,密塞,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液10mL,置烧瓶中,挥去溶剂,加8%盐酸溶液10mL,超声处理(功率250W,频率40kHz)2min,再加二氯甲烷10mL,加热回流1h,冷却,移至分液漏斗中,用少量二氯甲烷洗涤容器,并入分液漏斗中,分取二氯甲烷液,酸液用二氯甲烷振摇提取2次,每次15mL,合并二氯甲烷液,减压回收溶剂至干,残渣加10%二氯甲烷甲醇溶液使溶解,转移至25mL量瓶中,加10%二氯甲烷甲醇溶液至刻度,摇匀,滤过,取续滤液,即得。
2.2.3 阴性样品溶液的制备
取缺大黄阴性样品,按供试品溶液制备方法制备阴性样品溶液。
2.2.4 测定法
分别精密吸取对照品溶液与供试品溶液各20μL,注入液相色谱仪,测定,即得。
2.3 空白试验
分别吸取“2.2”项下的混合对照品溶液、供试品溶液及阴性样品溶液,注入高效液相色谱仪进行测定,实验结果表明阴性样品溶液在与对照品相应的保留时间处无色谱峰出现。方中各味药对芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚色谱峰无干扰。结果见图1。
2.4 线性试验
精密称取在105℃干燥12h的芦荟大黄素对照品、大黄酸对照品、大黄素对照品、大黄酚对照品和大黄素甲醚对照品适量,加10%二氯甲烷的甲醇溶液溶解分别制成每1mL含芦荟大黄素、大黄酸、大黄素、大黄酚各100μg,大黄素甲醚50μg的溶液。分别精密吸取上述5种溶液各1、2、3、4、5、6、16mL分别置100mL容量瓶中,加10%二氯甲烷的甲醇溶液稀释定容至刻度,摇匀,即得,精密吸取20μL,分别注入高效液相色谱仪中,按上述色谱条件进行测定。以进样量(X)对峰面积(Y)进行线性回归,得回归方程为:芦荟大黄素 Y=5545.9X-31.839,r=0.9998;大黄酸 Y=4695.2X-20.192,r=0.9997;大黄素 Y=4000.5X-14.995,r=0.9997;大黄酚 Y=5814.8X-28.445,r=0.9996;大黄素甲醚 Y=3088.1X-7.9162,r=0.9996。试验结果表明,芦荟大黄素在0.02436~0.3898μg/mL范围内呈良好线性关系;大黄酸在0.0181~0.2896μg/mL范围内呈良好线性关系;大黄素在0.01856~0.2970μg/mL范围内呈良好线性关系;大黄酚在0.01866~0.2986 μg/mL范围内呈良好线性关系;大黄素甲醚在0.01~0.16 μg/mL范围内呈良好线性关系。
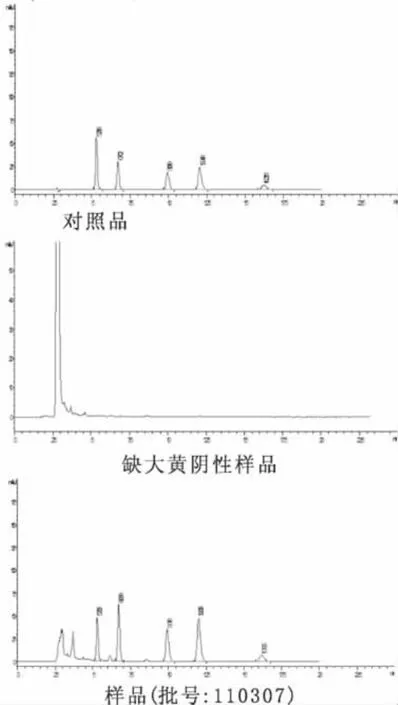
图1 对照品、样品及阴性样品的色谱
2.5 重复性试验
取同一批号(批号:110118)样品,按“2.2”项下供试品的方法,平行制备6份供试品溶液,进样测定,计算芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量,RSD分别为1.01%、2.62%、1.18%、2.54%、2.99%,表明该方法重复性良好。
2.6 稳定性试验
取同一批号(批号:110118)样品溶液,分别于0、2、4、6、8、10、12h后按上述色谱条件测定芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量,含量基本不变,RSD分别为2.79%、1.48%、0.50%、0.82%、0.57%,表明供试品液在12h内稳定性良好。
2.7 精密度试验
在上述色谱条件下,取按“2.2”项下配置的芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚对照品溶液分别连续进样6次,RSD 分别为 1.01%、0.45%、0.68%、0.73%、0.79%。
2.8 回收率试验
精密称取已知含量的大黄通便颗粒(江苏辰牌药业有限公司,批号:110118)样品,分别精密加入一定量的芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚对照品,按“2.2”项下操作制备供试品溶液并测定,计算回收率,取得了较满意的回收率,表明该方法可行。结果见表1、2、3、4、5。
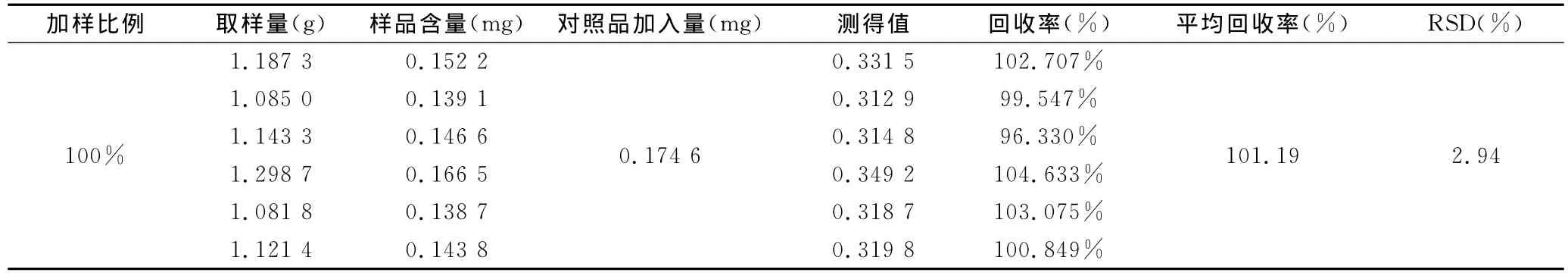
表1 芦荟大黄素加样回收率试验结果(n=6)
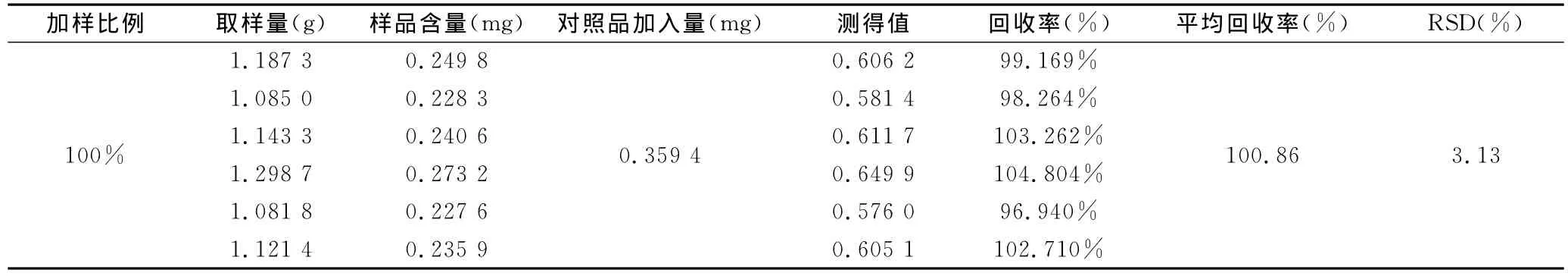
表2 大黄酸加样回收率试验结果(n=6)
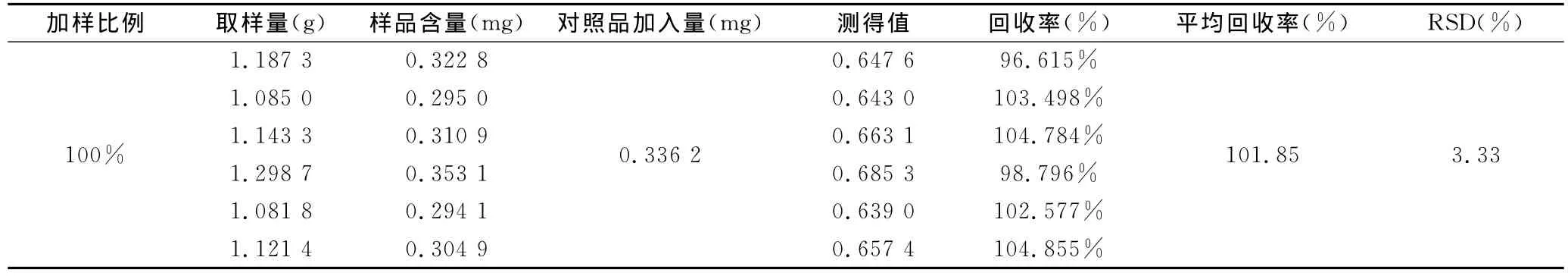
表3 大黄素加样回收率试验结果(n=6)
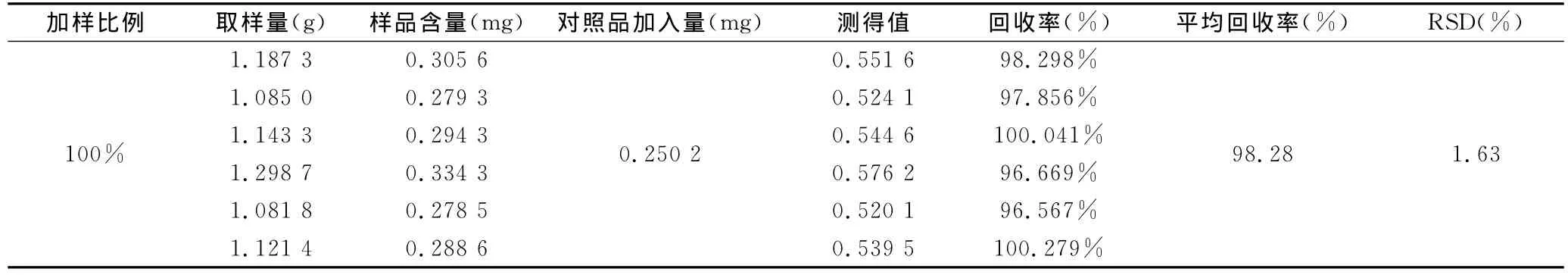
表4 大黄酚加样回收率试验结果(n=6)
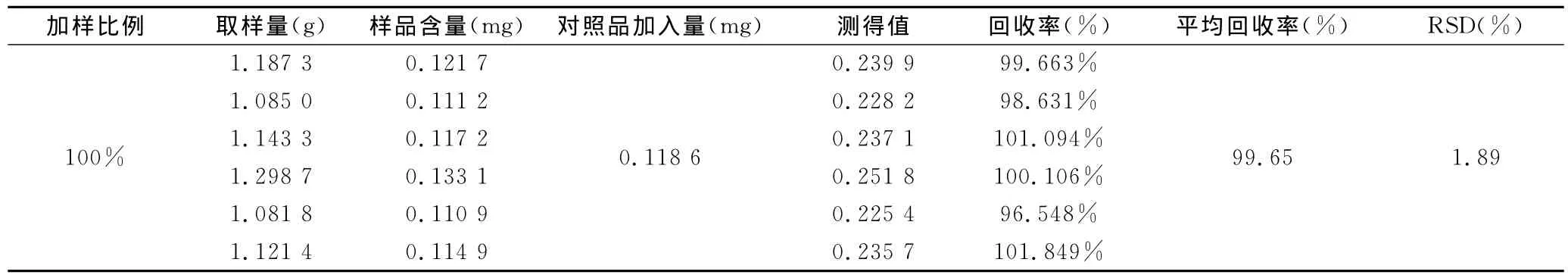
表5 大黄素甲醚加样回收率试验结果(n=6)
2.9 样品测定
取3批样品,按“2.2”项下供试品溶液制备方法制备,按上述色谱条件测定,计算,结果见表6。
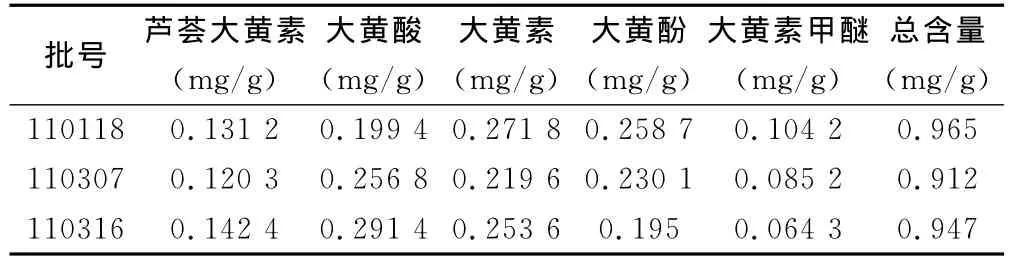
表6 大黄含量测定结果
3 讨论
我们曾比较氯仿与二氯甲烷作为提取溶剂进行提取,结果表明二者提取的含量相当,而氯仿毒性较大,故采用二氯甲烷作为本方法的提取溶剂。本实验所采用测定方法测定芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚,重现性良好,回收率高,且在该色谱条件下,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚进样精密度良好,故该方法结论可靠,可作为大黄通便颗粒的质量控制标准。
[1]国家药典委员会编.中国药典2010年版[S].一部.北京:中国医药科技出版社,2010:22-23.
