锂离子电池电解液新型锂盐的研究进展
2011-07-01任永欢吴伯荣杨春巍陈飞彪
任永欢,吴伯荣,杨春巍,吴 锋,2,陈飞彪
(1.北京理工大学化工与环境学院,北京 100081;2.国家高技术绿色材料发展中心,北京 100081)
如今锂离子电池得到广泛应用,由手机、笔记本电脑等电器所用电池而逐步应用到潜艇、航天及电动车等领域。锂盐作为电解液组成之一,使用性能优良的锂盐是获得高比能量、高比功率、宽电化学窗口、长循环寿命和存储寿命、良好安全性能及低温性能的锂离子二次电池的关键。它不仅是电解质中锂离子的提供者,其阴离子也是决定电解质物理和化学性能的主要因素。目前商品化应用的LiPF6对水敏感,低温生成的SEI膜阻抗过大,并由于其在80℃开始分解,导致锂离子电池的高温性能更是差强人意。因此国内外展开了大量对新型锂盐的研究。
锂盐可分为无机锂盐和有机锂盐。无机锂盐如LiPF6、LiBF4、LiClO4;有机锂盐包括螯合 B 类如 LiB(C2O4)2,螯合 P类如 LiP(C6H4O2)3,全氟膦类如 Li(RfPF5),烷基类如 LiC(CF3-SO2)3,磺酸盐类如 CnF2n+1SO3Li,铝酸盐类如 Li3Al(CSO3Cl4),亚胺锂如LiN(CF3SO2)2[1]。
锂离子电池电解质对锂盐的要求有以下几点:(1) 锂盐极性要强,以促进其在有机溶剂中的溶解;(2)阴离子与Li+的结合能要小,要为负电荷分散程度较高的基团,晶格能越小,锂盐越容易离解;(3)阴离子基团质量不能过大,否则会影响电池的比能量;(4)阴离子参与反应形成的SEI膜阻抗要小,并能够对正极集流体实现有效的钝化,以阻止其溶解;(5)锂盐本身有较好的热稳定性和电化学稳定性;(6)可行的生产工艺以及有竞争力的性价比,对环境友好。
1 无机锂盐
1.1 LiBF4
在常温电解液中LiBF4的应用较少,因其电化学稳定性低于LiPF6。由于其阴离子半径小,易缔合,由LiBF4组成的电解液电导率较小,在(EC+DMC)混合溶剂中的电导率也只有LiClO4电解液电导率的一半。
但研究表明LiBF4低温性能良好。与LiPF6相比,以LiNiO2/石墨为电极的1 mol/L LiBF4/(PC+EC+EMC)(质量分数为1∶1∶3) 在低温-30℃和-50℃分别可放出常温放电容量的86%和20%;后者在-30℃只能放出76%,-50℃时已经无法放电。LiBF4热稳定性高,对水不敏感,低温电荷转移电阻小,适合低温和高倍率放电。基于这些低温特性,研究人员又开始了对LiBF4的大量研究。由于LiBF4成膜性不好,常与成膜性能好的锂盐共同作用。
1.2 LiBF3Cl
用Cl取代LiBF4中的一个-F后,阴离子半径会有所增大,由此可降低阴离子缔合度,增大锂盐的溶解度,从而提高溶液的电导率;另外,由于结构的不对称性增强,LiBF3Cl的熔点会更低。B-Cl比B-F更容易断裂,释放出的Cl-可以参加成膜反应,克服了LiBF4成膜性能不好的缺点。Zhang[2]通过X射线衍射(XRD)图谱分析看出LiBF3Cl跟LiBF4具有相似的晶体结构。其研究表明,在质量比为3∶7的EC∶EMC组成的溶剂中,LiBF3Cl作为锂盐的Li/石墨电池的首次库仑效率可以从LiBF4的82%提高到89.6%。同时还发现LiBF3Cl可以钝化铝箔保护其不受腐蚀。
由此可见,LiBF3Cl性能优于LiBF4,克服了后者溶解度低、成膜性不好等缺点,有望成为新型低温锂盐应用于锂离子电池电解液中。
1.3 LiX
LiF、Li2O和Li2O2合成简单,成本低。但因其在碳酸酯类溶剂中几乎不溶,一直被排除作为锂离子电池的锂盐。但当三(五氟苯基)硼烷(TPFPB)或三(六氟异丙基)硼酸酯(THFPB)作为阴离子受体时,会大大增加LiX的溶解度,大约能达到2×10-3S/cm。其锂离子的迁移数高达0.7,比同样情况下用LiPF6、LiClO4或LiBF4作为锂盐都几乎高出一倍[3]。锂离子迁移数的提高可能会减小极化和改善库仑效率。LiF、Li2O和Li2O2与正极都有很好的相容性和循环性。Li2O和Li2O2具有能在正极表面反应的独特成膜性能,由此比LiF更优异。如在LiMn2O4为正极0.4 mol/L TPFPB+0.2 mol/L LiX/(PC+DMC)(体积比1∶1)的半电池中库仑效率分别可达到92%和89%[4]。另外,以此三种盐作为锂盐,也拓宽了电化学窗口范围。LiF在(PC+EC+DMC)(体积比1∶1∶1)中的分解电压超过了5.1 V。
但不足在于与负极的相容性不是很好,尤其是PC存在时不能在负极上生成稳定的SEI膜。解决办法:(1)在溶剂中添加LiBOB作为成膜剂,实验取得了很好的成果,负极可逆比容量可达到308 mAh/g左右[5];(2)PFPBO作为BBAR,因其结合了TPFPB与LiBOB的优点,也可解决PC共嵌的问题[6]。
由此可见,BBAR的出现,极大地提高了LiX类盐用于电解液中的可能性。
2 有机锂盐
2.1 硼基类锂盐
硼基类锂盐对环境友好,其种类比较多,大致可以分为两类:芳基硼酸锂和烷基硼酸锂。在诸多硼基类锂盐中,芳香硼酸锂盐电导率较低,分解电压也较低,由此影响了其实际应用。烷基硼酸锂盐中最有应用前景的当属LiBOB和LiDOFB。
2.1.1 LiB(C2O4)2(LiBOB)
LiBOB以硼原子为中心,呈现独特的四面体结构。硼原子具有强烈的吸电子能力,由于B上的负电荷被周围两个草酸根上的八个氧原子高度分散,使阴阳离子键的作用力减小,由此使得LiBOB在有机溶剂中的溶解性增大。LiBOB高温性能很好,LiPF6在50℃时已经不能正常循环,但换用LiBOB会在60、70℃依旧循环良好[7]。LiBOB的最大优点在于成膜性好[8]。
尽管具有诸多优点,但由于LiBOB研究年限比较短,其不足还有待研究。目前研究发现[7],LiBOB在线性碳酸酯中的溶解度不大;LiBOB对水比较敏感[9],目前批量生产的LiBOB的纯度不达标。杂质的存在会增大SEI膜的阻抗,影响电池倍率放电功能[9],还会影响电池的循环使用寿命[10]。并且单独使用LiBOB时电池低温性能并不好,在-50℃已经无法放电[11]。由于LiBOB具有很强的吸湿性,所以大多数情况下都作为添加剂与其他锂盐共同使用。
(1)LiBOB与LiClO4
PC是很好的低温共溶剂,但在PC存在的情况下单独使用LiBOB或LiClO4作为锂盐效果都不理想[12]。图1表明单独使用LiBOB时,还原峰强度相对较弱,表明电池容量不足,研究认为这是由于Rct太大造成的。单独使用LiClO4时PC发生了共嵌造成严重的石墨脱落,电池无法正常工作。
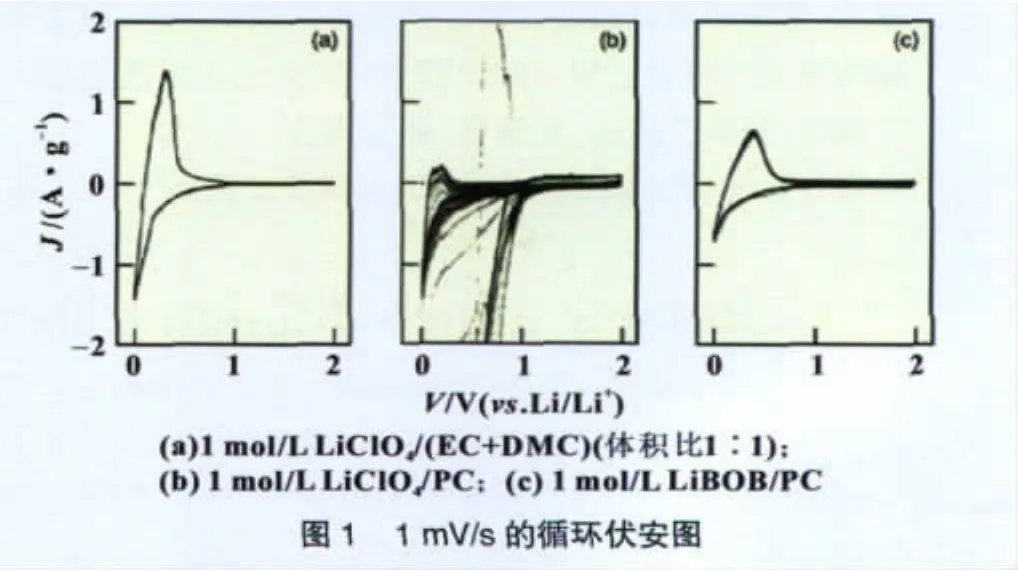
但如果在LiClO4中添加LiBOB后(摩尔比1∶50),在碳负极可有效形成SEI膜抑制分解,LiClO4的使用可以减小RSEI和Rct,保证电池容量不逊于常规电池。但不足之处在于循环性能有所降低[12]。
(2)LiBF4-LiBOB
LiBOB的添加可以有效地形成SEI膜,稳定电池性能。高温下LiBOB生成的表面膜可以阻止Fe的溶解,由此可以提高锂离子电池工作的高温范围[11]。使用石墨/LiNiO2电池配合1.0 mol/L(0.98LiBF4-0.02LiBOB)/(PC+EC+EMC)(质量比1∶1∶3)的电解液在-30℃和-40℃分别可以放出常温容量的83%和63%[13]。应用Li/LiFePO4电极,相比于单独使用Li-BOB在-50℃无法放电的情况,1.0 mol/L的0.9LiBF4-0.1Li-BOB/(PC+EC+EMC)(质量比1∶1∶3)的电解液仍可以放出常温容量的30%。
但LiBOB的含量不能过多。通过图2放电曲线可以看出,随着LiBOB的比例的增加虽然电池比容量没有变化,但是放电平台却在降低。研究认为是LiBF4的减少导致Rct增大。不足之处的克服有待进一步研究。

2.1.2 LiBF2(C2O4)(LiODFB)
LiODFB结合了LiBOB成膜性好和LiBF4低温性好的优点[14],在1.5 V左右会发生还原反应在碳负极生成SEI膜[15]。Zhang[16]的研究发现,草酸硼酸类锂盐的充放电曲线几乎都在1.5 V左右有个平台。Zhang分析认为平台的出现是由于-CO-COOLi基团的还原,而杂质以及水的存在会造成ODFB-的开环形成更多的-CO-COOLi,会延长1.5 V这个平台。Li-ODFB跟LiBOB相比,因只有一个草酸根,1.5 V的平台会较短,这是用F-取代一个草酸根后的一个优点。
如表1所示,LiODFB的低温放电性能明显优于LiPF6和LiBOB[17]。LiDOFB跟正极也有很好的相容性,不仅能钝化铝箔而且能够很好地抑制电解液的氧化。M.H.Fu等人[18]研究发现ODFB-阴离子可以捕获溶解的Mn2+离子,生成致密的表面膜从而进一步阻止Mn2+的溶解。LiODFB的高温性能也优于LiPF6。1.0 mol/L LiODFB溶于PC/EC/EMC(质量分数为30∶30∶40)的LiNiO2/石墨电池在60℃下循环200次后容量衰减<10%。LiODFB可提高电池的安全性能。其分解温度为240℃,分解之后产生的CO2,可以在电池过充的情况下增大电池内压,在热涌发生前提供一个安全出口[16]。
LiODFB的这些优良性能展示了其替代LiPF6的可能性。但其常温下的放电比容量相对较低,并且LiODFB的产业化也有一定的难度,作为新型锂盐还有待进一步探究。

2.2 磺酸锂盐
LiCF3SO3(LiTf)基的锂盐在有机液体电解液的应用中会出现腐蚀集流体的现象。但LiTf比较适合作为高温锂离子电池的离子液体电解液组成[19]。CF3SO3Li(LiTf),CF3SO3Na(NaTf),CF3SO3K(KTf)以0.5∶1∶1的摩尔比混合时,在250℃时的电化学窗口为4.7 V,在230~270℃电导率可达到10-2S/cm。TG/DTA研究表明,400℃下此种电解液依然保持着热稳定性。与卤化物和碘化物相比,LiTf显示了作为电解质盐的优越性。
2.3 烷基锂盐
LiC(SO2CF3)3不腐蚀集流体,熔点为271~273℃,热分解温度高达340℃以上。其电导率比其它有机阴离子锂盐均要高,在1 mol/L电解质溶液中可达1.0×10-2S/cm,溶于EC/DMC的电解质在-30℃都不发生凝固,且电导率仍可达到10-3S/cm以上,这主要归结于其阴离子半径较大,约0.375 nm,较易电离,其电化学窗口也在4.0 V以上。但是由于其合成困难、价格昂贵,限制了其广泛应用。
2.4 亚胺锂盐
LiN(SO2CF3)2(LiTFSI)阴离子中的中酰胺N与强吸电子基团相连,使得N上的负电荷更加分散,更容易脱离出Li+。LiTFSI热分解温度超过360℃。LiTFSI能够在MCMBs上形成低电阻、稳定的SEI膜,除第一次循环外几乎每次充放电循环的库仑效率都接近100%。在石墨/Li2FeSiO4电池中,LiTFSI在正极可以生成钝化膜,不会像LiPF6一样生成HF导致Fe的溶解[20]。尽管TFSI的大型阴离子会导致溶液的粘度升高,但电导率与LiPF6相当[21]。LiTFSI低温情况下的电荷传递电阻小,相比LiPF6小一个数量级[21]。较小的电荷传递电阻保证了LiTFSI良好的低温性能。
由于其腐蚀集流体,具体应用性能有待进一步研究。其他亚胺锂盐理论研究较多,但实际应用并不常见。
2.5 含P有机锂盐
该类锂盐的阴离子为含氟烷基及-F与P形成六配位的络合物,或者为邻苯二酚衍生物与P形成六配位的五元环螯合物。LiPF3(C2F5)3(简称LiFAP),-C2H5基团中的H被F取代后,形成强的吸电子基团,由此LiFAP会具有较低的HOMO,从而会有较好的抗氧化的稳定性。LiFAP具有同LiPF6相当的电导率和电化学稳定窗口,并且有比LiPF6好的稳定性不易水解,即使在10-3H2O的环境下依然稳定。随着循环次数加大LiFAP的库仑效率优势更加明显。研究表明,含LiPF3(C2F5)3的电解液的闪点会提高,可增大锂离子电池的安全性,如在(EC+DEC+DMC)(质量分数40∶20∶40)组成的溶剂中,LiPF3-(C2F5)3作为锂盐的闪点可达到37.8℃,而LiPF6只有24℃。
3 展望
锂盐在锂离子电池中作用非常重要,新型锂盐的开发仍是一个重要的研究方向。新型锂盐的研究一方面集中于对LiPF6的改进,尝试研究新的取代基对LiPF6各种性能的改善情况。另一方面是寻找替代LiPF6的新型锂盐。以B为中心的硼基盐类对环境友好,高低温性能也良好,LiODFB是最有希望改善锂离子电池性能的锂盐。
[1]薛照明,陈春华.锂离子电池非水电解质锂盐的研究进展[J].化学进展,2005,17(3):399-405.
[2]ZHANG S S.LiBF3Cl as an alternative salt for the electrolyte of Li-ion batteries[J].Journal of Power Sources,2008,180:586-590.
[3]LI L F,LEE H S.New electrolytes for lithium on batteries using LiF salt and boron based anion receptors[J].Journal of Power Sources,2008,184:517-521.
[4]XIE B,LEE H S,LI H,et al.New electrolytes using Li2O or Li2O2oxides and tris-(pentafluorophenyl)borane as boron based anion receptor for lithium batteries[J].Electrochemistry Communications,2008,10:1195-1197.
[5]LI L F,XIE B,LEE H S,et al.Studies on the enhancement of solid electrolyte interphase formation on graphitized anodes in Lix-carbonate based electrolytes using Lewis acid additives for lithium-ion batteries[J].Journal of Power Sources,2009,189:539-542.
[6]LI L F,LEE H S,LI H,et al.A pentafluorophenylboron oxalate additive in nonaqueous electrolytes for lithium batteries[J].Electrochemistry Communications,2009,11:2296-2299.
[7]XU K,ZHANG S S.LiBOB:Is it an alternative salt for lithium ion chemistry?[J].Journal of Power Sources,2005,146:79-85.
[8]ZHANG S S,XU K,JOW T R.Enhanced performance of Li-ion cell with LiBF4-PC based electrolyte by addition of small amount of LiBOB[J].Journal of Power Sources,2006,156:629-633.
[9]YANGA L,FURCZONB M M,XIAO A,et al.Effect of impurities and moisture on lithium bisoxalato-borate(LiBOB)[J].Journal of Power Sources,2010,195:1698-1705.
[10]XU K,DEVENEY B,NECHEV K,et al.Evaluating LiBOB/Lactone electrolytes in large-format lithium-ion cells based on nickelate and iron phosphate[J].Electrochem Soc,2008,155(12):959-964.
[11]ZHANG S S,XU K.An improved electrolyte for the LiFePO4cathode working in a wide temperature range[J].Journal of Power Sources,2006,159:702-707.
[12]HIROAKI K,KYOICHI S,TAKAMURA T.Power capability improvement of LiBOB/PC electrolyte for Li-ion batteries[J].Journal of Power Sources,2005,146:142-145.
[13]ZHANG S S,XU K,JOW T R.Enhanced performance of Li-ion cell with LiBF4-PC based electrolyte by addition of small amount of LiBOB[J].Journal of Power Sources,2006,156:629-633.
[14]ZHANG S S,XU K.A new approach toward improved low temperature performance of Li-ion battery[J].Electrochemistry Communication,2002,4:928-932.
[15]GAO H Q,LAI Y Q.Electrochemical behaviors of new lithium salt LiBC2O4F2in EC+DMC solvents[J].Acta Physico-Chinmica Sinica,2009,25(5):905-910.
[16]ZHANG S S.An unique lithium salt for the improved electrolyteof Li-ion battery[J].Electrochemistry Communications,2006,8(9):1423-1428.
[17]邓凌峰,陈洪.锂电池用草酸二氟硼酸锂有机电解液的电化学性能[J].无机化学学报,2009,25(9):1646-1650.
[18]FUA M H,HUANGA K L.Lithium difluoro(oxalato)borate/ethylene carbonate+propylene carbonate+ethyl(methyl)carbonate electrolyte for LiMn2O4cathode[J].Journal of Power Sources,2010,195:862-866.
[19]TU X H,CHU Y Q.New ternary molten salt electrolyte based on alkali metal triflates[J].Ionics,2010,16:81-84.
[20]ENSLING David.A comparative XPS surface study of Li2FeSiO4/C cycled with LiTFSI-and LiPF6-based electrolytes[J].Journal of Materials Chemistry,2009,19:82-88.
[21]MANDAL B K.New low temperature electrolytes with thermal runaway inhibition for lithium-ion rechargeable batteries[J].Journal of Power Sources,2006,162:690-695.
