LiCo x Al0.05Mn1.95-x O3.95F0.05的合成与电化学性能研究
2011-07-01张景会王俊芳张海朗
张景会, 王俊芳, 张海朗
(1.河南科技大学化工与制药学院,河南 洛阳 471003;2.江南大学化学与材料工程学院,江苏 无锡 214122)
尖晶石LiMn2O4由于电化学性能好、成本低、污染小、安全性好等优点,成为锂离子电池正极材料的研究热点[1-2]。但是尖晶石LiMn2O4循环性能差和在高温(55℃)条件下容量衰减快的问题一直制约着其商品化进程[3-4]。目前公认的引起容量衰减的原因主要有[5-6]:Jahn-Teller效应即立方相向四方相转变;LiMn2O4正极材料中Mn的溶解损失;电解液在高温高压下的氧化分解。
目前,研究者主要通过体相掺杂、表面修饰、改进合成工艺等方法来提高LiMn2O4的循环性能。研究表明:掺杂能有效改善尖晶石锰酸锂的电化学性能[7-12],通过掺杂阳离子(Li+,Ni2+,Mg2+,Co3+,Al3+,Ga3+,etc.)可以起到稳定材料结构的作用,通过F-等阴离子的掺杂可以使部分Mn4+还原为Mn3+,提高材料的容量,且由于F-具有很强的吸引作用,能进一步稳定材料的结构。但单一元素掺杂往往只能从某一方面改善电极的性能,保证了循环性能却降低了容量,或者提高了容量却不能保证循环性能,相比较而言,多元素复合掺杂对改善材料的综合电化学性能有优势[13-15]。本实验采用溶胶-凝胶法合成了多元复合掺杂的 LiCoxAl0.05Mn1.95-xO3.95F0.05(x=0,0.01)正极材料,对其结构和电化学性能进行了研究。
1 实验
1.1 样品的制备及电池的组装
将分析纯的LiNO3、Mn(CH3COO)2·4 H2O、Co(NO3)2·6 H2O、Al(NO3)3·9 H2O和LiF按一定化学计量比溶于去离子水中形成溶液,升温至75℃,再称取适量柠檬酸(AR)溶于去离子水中形成溶液,并在不断搅拌条件下与上述溶液混合,然后加入28%的氨水,调节溶液pH为7.0左右,75℃下反应3~4 h,形成溶胶,将溶胶置于真空干燥箱中,85℃干燥6 h,去除水分后的凝胶置于刚玉坩锅中,在马弗炉中加热至150℃并保温10 h,然后加热至300℃保温12 h,在研钵中研磨后在马弗炉中升温至700℃烧结12 h,自然冷却后在研钵中磨成粉末备用。
将制得的正极活性物质、乙炔黑和聚偏四氟乙烯(PVDF)按质量比80∶12∶8混合,用1-甲基-2-吡咯烷酮作溶剂,搅拌得到糊状物,将此物用Doctor Blade技术均匀地涂在铝箔上,80℃下真空干燥10 h,在辊轧机上轧成0.12~0.16 mm的薄膜,然后制得直径为14 mm的工作电极,在充满氩气的手套箱里[水含量(1×10-6)]制作CR2032纽扣电池,对电极为金属锂片,LB315(mDMC∶mEMC∶mEC=1∶1∶1)溶液,聚丙烯微孔膜Celgard 2325作隔膜。
1.2 材料的结构分析及电化学性能测试
采用德国Bruker公司生产的X射线衍射仪对材料进行结构分析,测试用 CuKα靶,管压 45 kV,管流30 mA,扫速3(°)/min,扫描范围 2θ =10°~90°。
充放电循环实验:将组装好的电池在室温(25±1)℃(空调控温)和高温(55±1)℃(恒温箱控温)下,用武汉金诺电子有限公司生产的蓝电电池测试系统LAND BT1210电池测试仪进行恒电流充放电测试,充放电电流密度为0.2 mA/cm2,充放电电压为3.0~4.5 V。
循环伏安实验在德国产的IM6电化学工作站进行,循环伏安的扫描速度为0.1 mV/s,电压范围3.0~4.5 V。
2 结果与讨论
2.1 样品的X射线衍射(XRD)分析
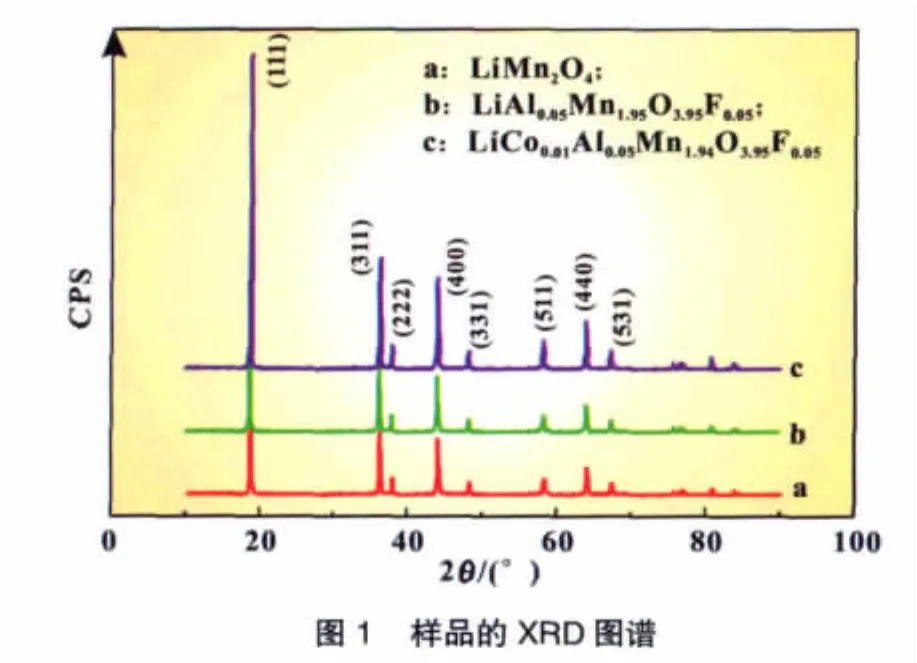
由图1可以得出合成材料的X射线衍射峰均为尖晶石型立方晶系特征衍射峰,样品的相组成均为单一的尖晶石结构,没有其他杂质衍射峰出现。这说明掺杂的原子已完全进入了尖晶石结构中,Fd3m空间群保持不变[16]。在Fd3m结构中Li+占据 8a 位置,Co3+、Al3+、Mn3+占据 16d 位置,O2-和 F-占据 32e 位置。样品LiCoxAl0.05Mn1.95-xO3.95F0.05中掺杂的阳离子Co3+和Al3+的半径与Mn3+的半径比较接近,很容易进入LiMn2O4尖晶石晶格中的16d位置,生成尖晶石型固熔体。随着掺杂元素的增加,衍射峰向高衍射角方向移动,X射线衍射峰的强度有所减弱,即晶体的晶胞产生了不同程度的收缩,复合掺杂材料因Mn-F键键能大,使得晶体结构的强度增加,有利于保证材料在充放电循环中的结构稳定性,经充放电测试得到进一步证明。
2.2 电化学性能
2.2.1 电压与容量的关系
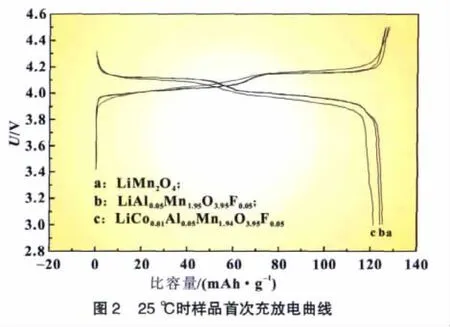
各样品的首次充放电曲线图2表明:不同元素掺杂的电极材料的充放电曲线均由两个平台组成,说明Li+嵌入尖晶石材料的过程是分步进行的;随着掺杂元素的增加,平台的阶梯性变得平滑,这可能是由于元素的掺杂导致晶胞收缩所致;未掺杂的材料放电比容量高于掺杂的,体现了掺杂材料的电化学特点;在各自相对应的放电平台内放电曲线非常接近,可以认为不同元素掺杂的正极材料在放电过程中锂离子嵌入的作用机理基本相同[17]。
2.2.2 充放电循环性能
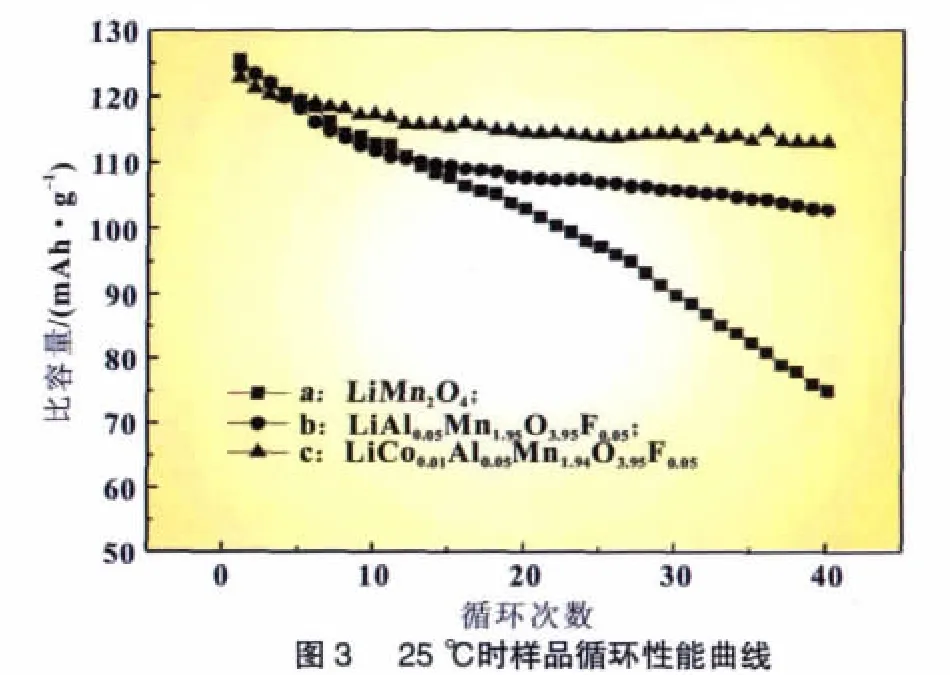
由图3和图4可以得出,掺杂型尖晶石LiCoxAl0.05-Mn1.95-xO3.95F0.05正极材料的循环性能较LiMn2O4循环性能有不同程度的改善,其中LiCo0.01Al0.05Mn1.94O3.95F0.05循环性能最好,原因可能是Co3+、Al3+掺杂能提高锰离子的平均价态,抑制Jahn-Teller效应的发生;掺杂使材料的电导率得到了提高,进而提高了锂离子在材料中嵌入-脱出的可逆性能;掺杂离子有着比Mn-O键更强的键能,可以起到稳定尖晶石结构的作用,进而稳定了材料的循环性能。阴阳离子复合掺杂形成的均匀固熔体增强了材料在电解液中抵抗HF酸歧化的能力[18],从而提高了尖晶石材料在循环过程中的稳定性。阴阳离子复合掺杂的容量较高,其可能的原因是掺杂的阴离子的电负性较高和离子极化率较小。本实验合成的多元复合掺杂材料使得各种离子间的键能增强,晶胞收缩,从而强化了材料的晶体结构,较好地满足了Li+的反复嵌脱,表明LiCo0.01Al0.05Mn1.94-O3.95F0.05作为锂离子电池正极材料具有优良的循环性能。

2.2.3 循环伏安测试
由图5可以看出,样品LiCo0.01Al0.05Mn1.94O3.95F0.05有两对明显的氧化还原峰,且氧化峰和还原峰对称性比较好,表明Li+在材料中的脱嵌可逆性良好,主要原因是Co3+、Al3+取代Mn3+进入晶格之后晶胞收缩,引起Mn-Mn键和Mn-O键的键长缩短,使得Li+在脱出和嵌入过程中晶胞的变形减少。阴离子半径 F-(0.133 nm)比 O2-(0.140 nm)小,F-的电负性比 O2-的电负性大,形成的Mn-F键键能比Mn-O键大,所以通过Co3+、Al3+和F-掺杂之后,材料晶体结构的稳定性增加,在充放电过程中材料的结构破坏程度降低,从而提高了Li+迁移的可逆性[19]。

3 结论
本方法合成的LiCo0.01Al0.05Mn1.94O3.95F0.05表现出较高的电化学比容量和较好的电化学特性,能够较好抑制锰酸锂尖晶石材料的可逆容量在充放电过程中的衰减,循环性能有了较大的改善,在室温(25℃)和高温(55℃)下恒流充放电,首次放电比容量为122.9 mAh/g和120.8 mAh/g,循环40次后容量保持率高达94.9%和89.5%。作为锂离子电池的正极材料,该多元复合掺杂材料将是众多取代钴酸锂的材料中最具竞争力的材料之一。
[1]TU J,ZHAO X B,ZHUANG D G,et a1.Studies of cycleability of LiMn2O4and LiLa0.01Mn1.99O4as cathode materials for Li-ion battery[J].Physica B,2006,382:129-134.
[2]刘心宇,吕罡,蒙冕武.合成条件对尖晶石型LixMn2O4正极材料结构的影响[J].湖南科技大学学报(自然科学版),2007,22(3):31-34.
[3]LI X F,XU Y L.Spinel LiMn2O4active material with high capacity retention[J].Applied Surface Science,2007,253(21):8592-8596.
[4]HIBINO M,NAKAMURA M,KAMITAKA Y,et a1.Improvement of cycle life of spinel type of lithium manganese oxide by addition of other spinel compounds during synthesis[J].Solid State Ionics,2006,177:2653-2656.
[5]AMATUCCI G G,SCHMUTZ C N,BLYR A,et al.Materials effects on the elevated and room temperature performance of C/LiMn2O4Li-ion batteries[J].Journal of Power Sources,1997,69(1/2):11-25.
[6]CUMMOW R J,KOCK A,THACKERAY M M.Improved capacity retention in rechargeable 4 V lithium/lithium-manganese oride(spinel)cells[J].Solid State Ionics,1994,69:59-67.
[7]SON J T,KIM H G.New investigation of fluorine-substituted spinel LiMn2O4-xFxby using sol-gel process[J].Journal of Power Sources,2005,147:220-226.
[8]BAO S J,LIANG Y Y,ZHOU W J,et al.Enhancement of the electrochemical properties of LiMn2O4through Al3+and F-co-substitution[J].Journal of Colloid and Interface Science,2005,291:433-437.
[9]XIAO J,ZHU H L,CHEN Z Y,et al.Preparation and property of spinel LiMn2O4material by co-doping anti-electricity ions[J].Trans Nonferrous Met Soc China,2006,16:467-472.
[10]李运姣,常建卫,李洪桂,等.富锂型掺钴尖晶石锂锰氧化物的结构与电化学性能[J].中南大学学报(自然科学版),2004,35(3):381-385.
[11]姚耀春,戴永年,杨斌,等.F-Cr复合掺杂LiMn2O4的合成及性能研究[J].电池,2005,35(6):411-413.
[12]张娜,唐致远,卢星河.二元掺杂尖晶石LiMn2O4的合成与性能研究[J].现代化工,2005,25(增刊):201-203.
[13]唐致远,卢星河,张娜.阴阳离子复合掺杂对尖晶石型正极材料的影响[J].物理化学学报,2005,21(8):934-938.
[14]卢星河,唐致远,韩冬,等.尖晶石型Li-Mn-O多元素掺杂的高温电化学性能[J].中山大学学报(自然科学版),2005,44(2):26-29.
[15]童庆松,杨勇.掺钛、钴、镍的Li-Mn-O尖晶石的电化学性能研究[J].电源技术,2006,30(1):28-34.
[16]LI R H,GONG F Y,LIN H,et a1.Co-precipitation synthesis and characterization of multiple subsituted lithium manganese oxides in lithium ion batteries[J].Ionics,2005,5:343-351.
[17]FENG J J.Dissertation[D].Tianjin:Tianjin University,2004.
[18]AMATUCCI G G,PEREIRA N,ZHENG T,et al.Failure mechanism and improvement of the elevated temperature cycling of LiMn2O4compounds through the use of the LiAlxMn2-xO4-xFxsolid solution[J].J Electrochem Soc,2001,148(2):A 171-A 182.
[19]林志鹏,李荣华,王文继,等.LiCoxNixMn2-2xO4-xFx(x=0.05,0.1)的合成与性能研究[J].功能材料,2005,36(8):1220-1222.
