数字化微创技术在肝胆胰外科的应用
2011-06-21方驰华
方驰华 项 楠
(南方医科大学附属珠江医院肝胆外科,广州 510282)
黄志强院士指出,到了 20世纪,传统外科的手术技术已经成熟,限制着外科发展的已不是手术技巧本身,而是围绕着外科的“软件”[1]。随着数字医学及微创外科的发展,数字化微创技术应运而生,是指将三维重建、可视化仿真手术等数字医学技术应用于外科临床工作,实现外科微创化。自 20世纪90年代起,综合了计算机图像处理与分析、真实感计算机图形学、虚拟现实等技术的医学影像的三维可视化技术一直是国内外研究与应用的热点,在近10年的时间里有了突飞猛进的发展。在术前疾病诊断、手术设计及教学和仿真手术训练等方面是数字医学技术应用的一个重要领域。
国外数字虚拟人的研究计划始于 1989年美国国立医学图书馆(NLM)的“可视人计划”(Visible Human Project,VHP),于 1994年和 1996年分别获得了一男一女两组包括 CT、MRI和切片图像的数据集,拉开了数字医学与人体解剖相结合的新纪元[2,3]。2000年韩国亚洲大学医学院报道了可视韩国人计划(Visible Korean Human,VKH)[4]。日本2001年启动了为期 10年的人体测量国家数据库建造计划。现在国外已经开发了新的计算机人体解剖模拟学习系统,如华盛顿大学开发的数字解剖学家系统,德国汉堡大学开发的交互式解剖学图谱Voxel-Man[5],美国伦斯利尔理工大学建立的成年男子全身模型 VIP-Man[6]。
随着计算机图形技术及虚拟仿真技术的不断发展,虚拟手术系统的开发工作也取得了很大的进展。美国加利福尼亚 San Francisco大学外科系与伯克利学院的电子工程与计算机科学系合作进行了虚拟腹腔手术的研究。在欧洲,法国国家信息和自动化研究所(INRIA)、德国国家信息技术研究中心(GMD)等研究机构对虚拟手术及相关技术进行了深入的研究[7]。从研究现状来看,日本欧美等国家的研究起步较早,目前有些公司已经着手开发成型的手术模拟系统[8]。
中国 2001年 11月在北京召开的香山科学会议第 174次学术讨论会,开创了我国数字医学研究的篇章。我国经过 1年多的努力,首先完成了虚拟人体有关关键技术的研究任务。在钟世镇院士带领下,第一军医大学、第三军医大学首先建立了中国数字化虚拟人女性Ⅰ号和中国数字化虚拟人男性Ⅰ号。目前,我国上海、重庆和广州等地的解剖学专家们,已先后提供了 12套虚拟人切片数据的获取工作,为后续的多学科研究发展提供了有中国人特点的数据集[9,10]。与国外研究情况相比,国内关于虚拟手术方面的研究始于 20世纪 90年代,目前清华大学、浙江大学、国防科技大学、中科院自动化研究所、中科院计算机所、南方医科大学、华南师范大学等单位对虚拟手术系统进行了初步研究[11~14]。国内近年也开始研发自主知识产权的医用可视化软件,主要有中科院自动化研究所研发的 3D MED、复旦大学医学院数字医学研究中心研发的 3D重建及虚拟分割软件以及南方医科大学方驰华和华南师范大学鲍苏苏研究团队研发的腹部医学图像三维可视化系统(Medical Image 3D Visualization System,MI-3DVS)等。
怎样将数字医学技术应用于外科微创化,指导临床工作,让患者受益,是外科医师需要面对的一个问题。“微创”一直是外科学追求的境界,但以往无法克服小切口与显露不充分的矛盾。腹腔镜技术引进了一个新的概念:小入路、有限制地充分显露。完善的外科需要手术野的完善显露,并不是需要大切口。腹腔镜解决了手术入路并不改变外科实质。所以微创外科概念应该并非只是限于腹腔镜技术,而应有更广阔的视野。外科学的发展总是离不开当时的科技背景,在信息时代,传统的外科操作可能被微创的、准确的器械操作所代替。例如:当前发展很快的虚拟技术和三维立体可视技术,由计算机控制的机器人辅助手术比单纯外科医生实施的手术更为轻松和准确,并且创伤小[1]。数字医学技术指导下的外科微创化有着广泛的应用前景,其趋势将是从“尝试”到“广泛使用”的发展。
在虚拟中国数字人的基础上,我们利用虚拟现实技术手段,将现代影像学、计算机图像处理、肝脏解剖学和肝胆胰外科学相结合,进行了一系列的跨学科和交叉学科的研究,先后建立了中国虚拟人数字化肝脏、胰腺模型、肝脏管道灌注后冰冻铣切数字化虚拟肝脏、肝脏管道灌注后薄层 CT扫描数字化肝脏、基于 64排螺旋 CT多期扫描数据的数字化虚拟肝脏等,并在这些虚拟数字化肝脏和胰腺的基础上进行了初步的虚拟仿真手术的研究与尝试[12~14];目前已完成了对肝癌、肝血管瘤、肝移植、胆囊结石、肝胆管结石、胰头癌等疾病手术过程的个体化可视化仿真手术[15~21],并逐步将可视化仿真手术系统应用于指导真实手术进程。课题组首次开发完成了具有自主知识产权的腹部医学图像三维可视化系统(MI-3DVS),成功突破活人体腹部脏器亚毫米图像数据获取的瓶颈。并应用该软件对肝胆胰外科疾病进行快速的三维重建、指导正确的诊断和术前进行仿真手术、指导准确的手术治疗。在我国真正地实现了活人体个体化解剖数字化、诊断程序化和手术可视化。
在此基础上,建立基于 MI-3DVS的数字化微创技术在肝胆胰外科疾病的临床诊疗路径,从而为类似疾病的术前诊断和外科治疗提供一个有效的临床工具,实现肝胆胰外科疾病的数字化微创化快速诊断和治疗。现将数字化微创技术在肝胆胰外科应用的病例列举一二。
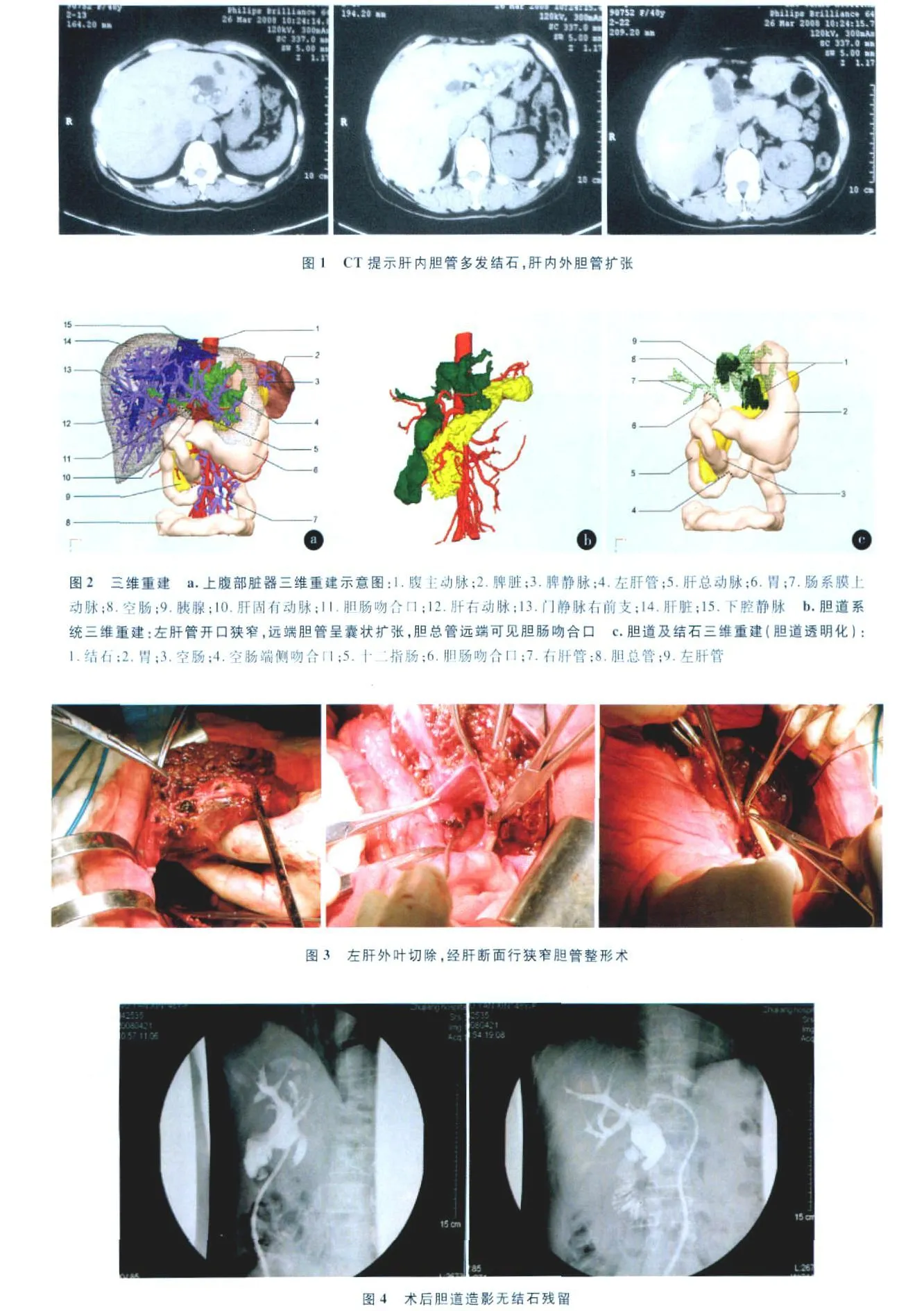
病例 1:女,48岁,因反复上腹部疼痛 6月余入院,曾行 3次胆道手术。64排 CT检查提示肝内胆管多发结石,肝内外胆管扩张(图1)。将 CT获取的数据导入 MI-3DVS,对程序分割后的图像数据进行三维重建,在Free Form Modeling System中对重建模型的各个部分进行放大、缩小、旋转、透明化等处理,并通过多角度观察结石、胆管的形态,明确结石分布范围、数量、大小等形状特点,胆管系统狭窄或畸形,肝内血管走行特征以及肝实质病变等情况。参照中华医学会外科学分会胆道外科学组制定的《肝胆管结石诊断治疗指南》,诊断为Ⅱ型肝胆管结石,结石分布于肝脏Ⅱ、Ⅲ段,左肝管开口狭窄,远端胆管呈囊状扩张,胆总管远端可见胆肠吻合口(图 2)。
根据 CT提供的影像信息并结合病史,常规需行左半肝切除,切除狭窄段胆管,原胆肠吻合口切开取石或吻合口切除。但三维重建提示患者结石局限于肝脏Ⅱ、Ⅲ段,左肝管开口狭窄,狭窄段肝管周围远离肝左动脉及门静脉左支,可以通过狭窄肝管纵行切开整形,通畅引流。三维重建提示胆肠吻合口通畅,如经肝断面取尽结石,解除狭窄,可以保留原胆肠吻合口。以 MI-3DVS三维重建为指导成功进行左肝外叶切除,狭窄胆管整形、支撑引流术(图3)。手术过程与术前规划一致,术后造影无结石残留,无胆管狭窄,胆肠吻合口通畅(图 4)。数字化微创技术应用于该病例的治疗,具有明显的优势:①术中经肝断面胆管探查肝内胆管及原胆肠吻合口无结石残留,行狭窄胆管切开整形,保留原胆肠吻合口,减少术中不必要的探查,节约手术时间,减少出血及创伤;②手术切除左肝外叶,保留肝脏Ⅳ段,肝脏断面及狭窄段胆管连续 3次活检,确保无癌变,保留了更多的正常肝脏组织。
肝胆管结石疾病本身具有相当大的复杂性,结石残留、术后复发、胆管狭窄是影响彻底治愈的主要因素。目前肝胆管结石的诊断主要依靠 CT、MRCP和 ERCP,这些现代化的手段仍不能突破三维重建技术瓶颈问题。通过对 CT片的连续阅读可确定患者肝胆管结石的简单分布分型,却无法直观地明确胆道狭窄部位,需要有经验阅片者的思维再现。
怎样把结石取尽,解除狭窄,通畅引流,保留更多的肝脏组织,实现肝胆管结石手术微创化,是肝脏外科医师需要思考的问题。我们利用 MI-3DVS进行 64排螺旋 CT数据进行三维重建,对肝胆管结石分布及胆道扩张/狭窄进行了大量的研究。MI-3DVS可完成真正意义上的胆道三维重建,在明确结石分布的位置,结石的形态、大小、数量之余,对胆管狭窄的空间位置及程度也有相当准确的显示,并且其显示方式更接近于手术的解剖位置,对肝胆管结石的分型诊断和手术指导具有重大意义。通过术前三维重建及仿真手术研究结果,结合术中探查所见,选择个体化的手术方式及手术入路,并做了相应的统计学分析,结果提示三维重建及仿真手术研究有利用缩短肝内胆管结石手术时间,减少术中出血及术后结石的残余率。与现代先进 CT相比较,使肝胆管结石残石率从过去文献报道 25% ~30.25%降低到 1.0%以下[20]。
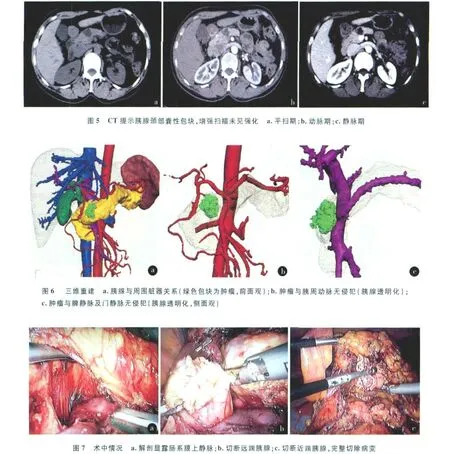
病例 2:女,52岁,因反复上腹部隐痛 20余年,加重 1个月入院。64排 CT检查提示胰腺颈部囊性占位病变,直径约 3.5 cm,增强扫描无强化(图 5)。MI-3DVS对程序分割后的图像数据进行三维重建后,再利用 Free Form Modeling System进行平滑、去噪,修整重建后的三维图像立体感强,形态逼真,真实反映患者腹部脏器解剖结构。通过不同组合方式可以同时显示腹部肝脏、胰腺及其肿瘤,脾脏和双肾等脏器,以及肝内的动脉、静脉、门静脉分支,腹主动脉,下腔静脉,腹腔动脉及其分支,肝外门静脉系统及分支等血管系统。对重要解剖结构可以通过两两显示进一步明确相互间的解剖关系,如通过肝脏透明度设置为零,隐去肝脏,可显示胰腺及肿瘤与周围血管的关系。为进一步明确肿瘤与血管有无侵犯,还可隐去肝脏和不同程度透明化胰腺,仅观察胰腺肿瘤与门静脉系统或腹腔干动脉系统,通过对三维模型进行放大、缩小、旋转等观察,可以进一步明确肿瘤与上述血管主干及其分支是否侵犯或压迫等解剖关系。从而明确肿瘤能否切除,周围血管能否保留,进而确定手术方式。
通过上述三维可视化图像的旋转立体观察,明确了患者胰腺肿瘤与周围血管关系,主要是门静脉及其分支肠系膜上静脉和脾静脉,腹腔干及其分支脾动脉等血管无侵犯及压迫,肿瘤可以完整切除,设计了中段胰腺切除的手术方案(图 6)。按照三维可视化结果指导术中解剖,顺利施行了腹腔镜下中段胰腺切除术(图 7)。数字化微创技术应用于该病例的术前诊断和手术规划具有明显的优势:①肿瘤体积较小,术前三维重建明确了肿瘤位于胰腺实质内,与肠系膜上动、静脉,脾动、静脉等胰周血管均无侵犯,解剖清晰,采用腹腔镜中段胰腺切除,使患者获得了腹腔镜手术的机会。②术前确定了术中需保留的胰腺周围动脉和门静脉系统分支,术中仅快速分离肠系膜血管和胰腺后壁间粘连,沿肿瘤包膜切除,而对其他部分未进行大范围的可切除性探查,不仅节约了手术时间,而且减少了术中出血和手术创伤。
术后免疫组化病理为潴留性囊肿,伴局部导管上皮乳头状增生。患者术后无胰漏、消化道出血、腹腔感染及糖尿病等并发症。
胰腺外科发展至今,许多方面的研究进展落后于腹部其他脏器疾病的研究。究其原因主要是胰腺的解剖特殊、供血复杂。传统的实质脏器解剖学研究主要针对固定的尸体标本,由于没有进行灌注,管道塌陷,柔软的胰腺及脏腹膜本身的立体和空间构象改变,所获得的解剖信息与活体胰腺不符。在实际临床工作中,由于手术前未能明确血管的走行和肿瘤的可切除性而在术中盲目探查,导致手术复杂化、风险扩大化。因此,熟悉和掌握胰腺及周围器官和结构的解剖和毗邻关系是提高手术技能和成功率的关键。此外,近 10年腹腔镜在胰腺外科的治疗中的应用日益广泛。与经腹手术不同,腹腔镜手术中医师通过监视屏幕的二维图像,双手操纵手术器械进行手术。如果医师缺乏通过屏幕的二维图像获得的有限信息了解整个解剖结构的三维空间关系的经验,操作就容易失误[22]。
现代影像学(螺旋 CT、MRI等)的发展,将胰腺解剖研究和肿瘤研究推向了一个新的阶段。64层以上螺旋 CT能够提供亚毫米级的影像信息,使得研究胰周血管的细小变异、大血管的精确形变和肿瘤的准确可切除性评估成为可能。基于 64层螺旋CT数据的 MI-3DVS三维重建技术,可以清晰显示胰腺血供,肿瘤与周围脏器的关系,进行准确的可切除性评估,指导术前规划和选择正确的手术方案。与现代先进 CT相比较,胰腺肿瘤可切除率提高了10%[21]。
综上所述,人体计算机三维重建及仿真技术在医学上的应用起源于医务人员对复杂的三维医学解剖数据的可视化需求,在它的基础上建立可供手术和手术前制定手术方案的三维立体仿真环境,在外科手术微创化方面具有令人鼓舞的应用前景。
1 黄志强.微创外科与外科微创化——21世纪外科的主旋律.中华外科杂志,2002,40(1):9-11.
2 Hohne KH,Pflesser B,Pommert A,et al.A realisticmode of human structure from the visible human data.Methods Inf Med,2001,40(2):83-89.
3 Spiter VM,Whitlock DG.The visible human dataset:the anatom ical platform for human simulation.Anat Rec,1998,253(2):49-57
4 Chung MS,Kim SY.Three-dimensional image and virtual dissection program of the brain made of Korean cadaver.Yonsei Med J,2000,41(3):299-303.
5 Pflesser B,Petersik A,Pommert A,et al.Exploring the visible human's inner organs with the VOXEL-MAN 3D navigator.Stud Health Technol Inform,2001,81:379-385.
6 Xu XG,Chao TC,Bozkurt A.VIP-Man:an image-based wholebody adultmalemodel formulti-particlemonte carle caluculations.Hwalth Phys,2000,78(5):476-486.
7 王勇军,赵 龙,郭光友,等.虚拟手术仿真器技术.系统仿真学报,2005,13(3):271-273.
8 邢英杰,张少华,刘晓冰.虚拟手术系统技术现状.计算机工程与应用,2004,7:88-90.
9 钟世镇,原 林,唐 雷,等.数字化虚拟中国人女性一号(VCH-F1)实验数据集研究报告.第一军医大学学报,2003,23(3):196-200.
10 张绍祥,刘正津,谭立文.首例中国数字化可视人体完成.第三军医大学学报,2002,24(10):1231-1232.
11 范毓东,董家鸿.虚拟手术系统在肝脏手术方案设计中的应用.外科理论与实践,2004,9(4):272-274.
12 方驰华,周五一,黄立伟,等.虚拟中国人女性一号肝脏图像三维重建和虚拟手术的切割.中华外科杂志,2005,43(11):748-752.
13 方驰华,周五一,虞春堂,等.肝脏管道系统灌注后薄层 CT扫描和三维重建的研究.中华外科杂志,2004,42(9):562-565.
14 Zhou ZM,Fang CH,Huang LW,et al.Three dimensional reconstruction of the pancreas based on the virtual Chinese human—female number 1.Postgrad Med J,2006,82(968):392-396.
15 方驰华,唐云强,鲁朝敏,等.胆囊切开取石和胆囊切除术的可视化研究.南方医科大学学报,2008,28(3):356-359.
16 方驰华,刘宇斌,唐云强,等.胰体尾肿瘤的可视化仿真手术研究.南方医科大学学报,2008,28(6):926-929.
17 方驰华,常 旭,鲁朝敏,等.肝内外胆管结石 64排CT数据三维重建及其临床意义.南方医科大学学报,2008,28(3):370-372.
18 朱新勇,方驰华,鲍苏苏,等.基于 64排螺旋 CT扫描数据的肝脏图像分割和三维重建.南方医科大学学报,2008,28(3):345-347.
19 方驰华,鲁朝敏,黄燕鹏,等.数字医学技术在肝癌外科诊治中的应用价值研究.中华外科杂志,2009,47(7):523-526.
20 方驰华,黄燕鹏,鲁朝敏,等.数字医学技术在肝胆管结石诊治中的应用价值研究.中华外科杂志,2009,47(12):909-911.
21 方驰华,刘宇斌,黄燕鹏,等.64排螺旋CT三维重建和胰腺可视化仿真手术的应用研究.中国实用外科杂志,2008,28(9):757-760.
22 Fernandez-Cruz L,Martinez I,Gilabert R,et al.Laparoscopic distal pancreatectomy combined with preservation of the spleen for cystic neoplasms of the pancreas.JGastrointest Surg,2004,8(4):493-501.
