TP、TC与NP方案治疗晚期非小细胞肺癌的系统评价
2011-06-15胡世莲孙玉蓓徐维平
方 向,胡世莲△,沈 干,吴 蕾,孙玉蓓,徐维平
(1.安徽医科大学附属省立医院老年医学科,合肥230001;2.安徽省循证医学中心,合肥230001;3.安徽省立医院肿瘤科,合肥230001)
肺癌是中国最常见的恶性肿瘤之一,非小细胞肺癌(nonsmall cell lung cancer,NSCLC)占75%~80%;由于早期诊断技术的局限性以及缺乏早期特异性临床表现,临床确诊时约2/3NSCLC患者已处于中晚期,大多失去手术机会,故以化疗为主的综合治疗是晚期NSCLC的重要治疗方法[1];在一定程度上可延长患者的生存期,提高生活质量。有研究认为以铂类为基础的联合化疗较未用铂类化疗明显提高了治疗有效率及1年生存率[2]。过去的 10年,第3代化疗药物多西紫杉醇、吉西他滨以及长春瑞滨的出现使NSCLC治疗有了更多选择,虽然何种方案更佳存在一定争论,但均显示了较好的结果[3]。本研究采用Cochrane系统评价的方法比较紫杉醇联合顺铂(TP)、卡铂(TC)与长春瑞滨联合顺铂方案(NP)的临床疗效和安全性。
1 资料与方法
1.1 一般资料 (1)所有病例均是经病理学或细胞学检查证实为晚期(Ⅲ~Ⅳ期)NSCLC患者;(2)年龄大于或等于18岁,性别不限;3)美国东部肿瘤协作组(Easlern Cooperation Oncology Group,ECOG)评分为 0~2分,或 Kamofsky评分大于或等于60分;(3)治疗前肝、肾功能,血液学,心电图检查无明显异常者;(4)近1个月内未接受抗肿瘤治疗。排除标准:(1)同时患2种恶性肿瘤者;(2)1个月内接受其他的抗癌治疗;(3)NSCLC为转移病灶者。
1.2 研究方法 按照检索策略,检索 Cochrane图书馆、Pubmed、中国生物医学文献数据库、中国知识资源总库和万方数据库,检索时间截至2010年4月;从所获文献中按照一般资料标准纳入TP或TC方案与NP方案治疗晚期非小细胞肺癌的随机对照试验和半随机对照试验。
1.3 结局测量指标 (1)中位生存期;(2)有效率[(完全缓解+部分缓解)/总病例数];(3)生存率;(4)不良反应。纳入随机对照试验的方法学质量评价采用Jadad评分标准[4],评价包括以下内容:(1)随机分配方法(2分,恰当;1分,不清楚;0分,不恰当);(2)盲法(2分,恰当;1分,不详,0分:非盲法);(3)失访与退出(1分,具体描述了撤除与退出的数量和理由;0分,未报告撤除或退出的数目或理由)。如果试验报告的资料不可使用,将进一步与作者联系后决定是否剔除该试验。
1.4 检索策略 按Cochrane协作网肺癌研究组的要求制定检索策略。英文检索词为:paclitaxel,vinorelbine,cisplatin,advanced non-small cell lung cancer,中文检索词为:紫杉醇、长春瑞滨、顺铂和晚期非小细胞肺癌。试验报告不全时与主要作者联系获得资料及纳入试验参考文献。
1.5 纳入试验的筛选和偏倚控制 两位研究者独立阅读所获文献题目和摘要,在排除明显不符合纳入标准的试验后,对可能符合纳入标准的试验阅读全文,以确定是否符合纳入标准。两位研究者交叉核对纳入试验,对有分歧而难以确定其是否纳入的试验通过讨论或由第3位研究者决定是否纳入。发表偏倚的控制包括进行文献检索时尽可能将所有的研究搜集齐全,包括未发表的阴性研究报告、会议论文摘要、各种研究简报、学位论文以及进行Pubmed检索时不限时间及语种等,并手工检索中文肿瘤类专科杂志;通过漏斗图及敏感性分析帮助判断是否存在发表偏倚。引用偏倚的控制包括制定明确、严格、统一的文献纳入和剔除标准;由两人采用独立进行试验筛选,对筛选结果不一致的文献请第3方专家评议;通过敏感性分析考察不同的文献纳入标准对Meta分析结果是否有影响,判断是否存在偏倚。
1.6 统计学处理 采用Cochrane协作网提供的RevMan5.0软件进行Meta分析,计数资料采用RR或OR及其95%CI。首先分析纳入研究的统计学异质性(显著性水平设计为α=0.05),当结果不存在异质性时,以固定效应模型进行Meta分析;存在异质性时,进一步分析异质性产生的原因,并采取亚组分析和敏感性分析,尽可能消除异质性,若未找到产生异质性的原因,则采用随机效应模型进行Meta分析。反之,若数据不适合Meta分析则进行定性分析,采用描述性方法总结。
2 结 果
2.1 文献检索结果及纳入随机对照试验(randomized controlled trial,RCT)基本特征 按照检索策略检索获得266篇文献,经阅读标题、摘要后排除177篇(综述107篇,重复发表文献33篇及非 RCT临床研究37篇),初步纳入89篇,阅读全文后排除70篇(包含放疗或化疗方案不符30篇,基础研究和费用比较40篇),共纳入19篇随机对照试验[5-23];其中4个英文研究[5-8],15个研究为中文研究[9-23],共 2 593例晚期NSCLC。
2.2 统计结果分析
2.2.1 中位生存期 8个研究均报道了中位生存期,其中,TP方案与NP方案的中位生存期分别为11.7vs15.4,8.8 vs 8.5,10.2 vs 10.7,13 vs 11,8.6 vs 8.4个月[7,11,14-15,18];TC方案与NP方案的中位生存期分别为8.6 vs 8.1,10.0 vs 9.5,12.3 vs 11.4个月[5-6,8]。5个研究报道其差异无统计学意义[6-7,11,15,18],3个研究未报道统计学结果[5,8,14]。
2.2.2 治疗有效率(CR+PR) 19个研究均报道了治疗有效率,各研究组间无异质性(P=1.00,I2=0%),采用固定效应模型,Meta分析结果显示TP和TC方案的有效率与NP方案差异无统计学意义[RR1.03,95%CI(0.93,1.13)],见表1。亚组分析TP方案与NP方案及TC方案与NP方案差异均无统计学意义,表2。TC方案3~4级血小板减少发生率高于NP方案,3~4级白细胞、中性粒细胞减少和恶心呕吐发生率低于NP方案,见表3。
2.2.3 生存率 纳入 9个研究均报道 1年生存情况[5-8,11,14-15,18,23],各研究间无异质性(P=0.77,I2=0%),采用固定效应模型.两方案在1年总生存率方面的差异无统计学意义[RR=1.04,95%CI(0.93,1.17)],亚组分析TP方案与NP、TC与NP方案差异亦无统计学意义(表1~3);2个研究比较了2年生存率[5,8],Meta分析结果显示 TC与NP方案的有效率差异无统计学意义[RR1.07,95%CI(0.79,1.45)],见表3。
2.2.4 不良反应 本研究主要分析3~4级血液学不良反应及消化道反应,合并结果显示:TP和TC方案中患者3~4级血小板减少发生率高于NP方案;3~4级白细胞减少、中性粒细胞减少、贫血、恶心、呕吐发生率低于NP方案,见表1。亚组分析显示:TP和NP方案3~4级血液学不良反应及消化道反应差异均无统计学意义,见表2。TC方案3~4级血小板减少发生率高于NP方案,3~4级白细胞、中性粒细胞减少和恶心、呕吐发生率低于 NP方案,见表3。
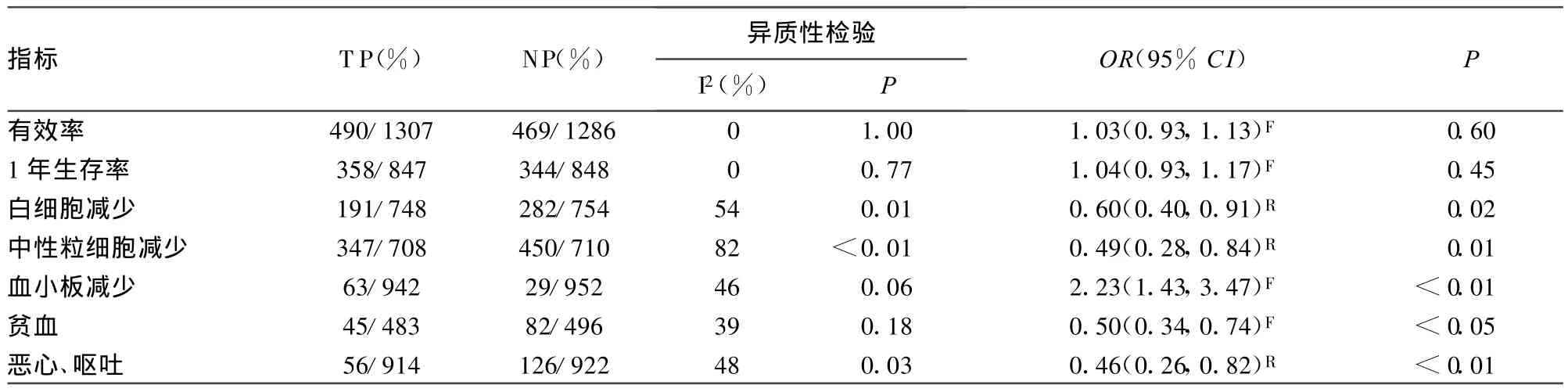
表1 TP、TC方案与NP方案治疗晚期NSCLC疗效和3~4级不良反应的 Meta分析

表2 TP与NP方案治疗晚期 NSCLC疗效和3~4级不良反应的Meta分析

续表2 化疗T P与NP方案治疗晚期NSCLC疗效和3~4级不良反应的Meta分析
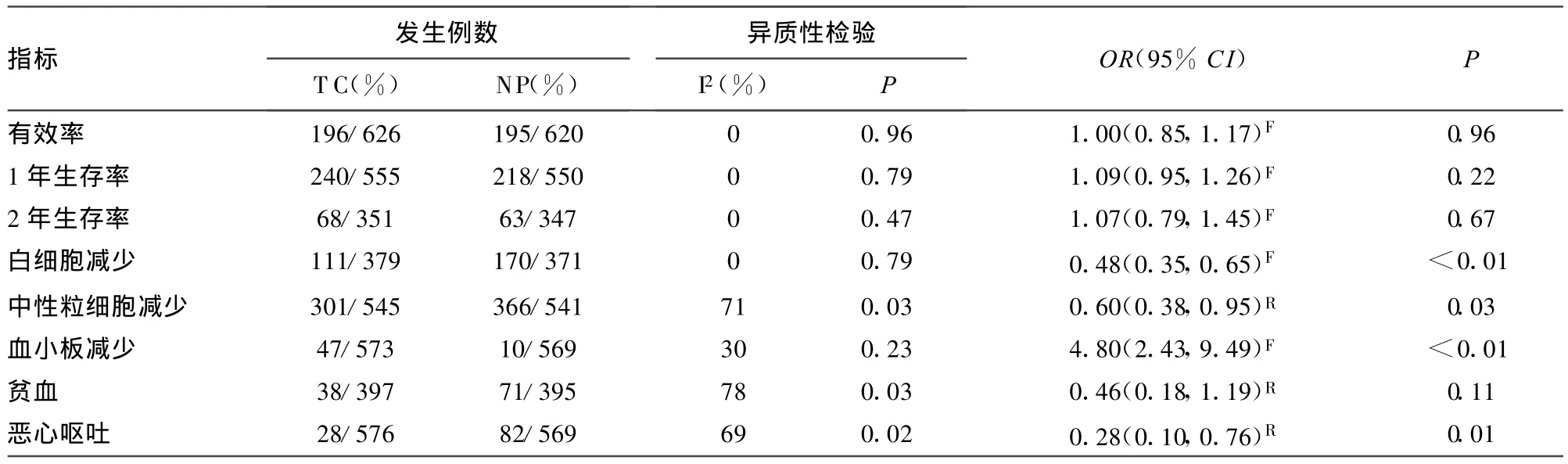
表3 化疗TC方案与NP方案治疗晚期NSCLC疗效和3~4级不良反应的Meta分析
2.2.5 敏感性分析与发表偏倚评价 当分别在有效率、1年生存率两项主要观察指标的Meta分析中逐一剔除单个独立研究时,其剔除前后的结果并无显著性差异,说明该两项观察指标的Meta分析结果较为可靠。另外,通过对漏斗图(插Ⅲ图1、2)的观察发现,以上两项观察指标Meta分析的漏斗图对称性均较好,提示发表偏倚对Meta分析结果的影响较小。
3 讨 论
NSCLC是一种高度恶性的疾病,晚期患者生存时间较短,改善晚期NSCLC的治疗极具挑战性。在过去十几年,数个关于晚期NSCLC化疗Meta分析的公布,帮助确立了以铂类为基础的双药方案作为晚期NSCLC的标准治疗方案;随第3代化疗药物的发展,铂类联合第3代化疗药物的两药方案已成为目前晚期NSCLC化疗的标准一线方案[2,24-26]。紫杉醇是治疗NSCLC最有效的药物之一,通过促进微管蛋白聚合,抑制微管解聚,使游离小管的数量减少,对处于有丝分裂间期的肿瘤细胞有细胞毒作用;临床使用时多与铂剂合用以取得协同作用。长春瑞滨是半合成长春碱类抗癌药物,通过阻止微管蛋白聚合形成微管和诱导微管解聚,使细胞分裂停止于有丝分裂中期,从而阻止细胞分裂增殖;NP方案因其临床疗效较好、价格低廉,目前在临床广为应用。
本研究显示在晚期NSCLC患者的一线治疗中,TP、TC与NP方案在有效率、1年生存率方面差异均无统计学意义;TP与NP,TC与NP方案分析差异亦无统计学意义。在不良反应方面,均显示了常见的血液学毒性及消化道反应,T P和TC方案血小板减少发生重于NP方案,白细胞减少、中性粒细胞减少、贫血和恶心、呕吐发生轻于NP方案;亚组分析显示TP与NP方案差异均无统计学意义,TC方案白细胞减少、中性粒细胞减少及胃肠道反应小于NP方案,血小板抑制重于NP方案,但贫血在TC方案中发生率与NP方案差异无统计学意义。虽然亚组分析显示TP或TC方案贫血发生低于NP方案(P>0.05),但至少没有证据显示NP方案更有利;本研究认为TP和TC方案贫血毒性较小,存在一定风险,尚需更多更大规模的高质量临床试验来证明。
近年来伴随肿瘤细胞信号转导研究的发展,在细胞受体、细胞信号转导等分子靶向治疗方面取得了很大进展。Goss等[27]研究显示,TC方案联合西地尼布或安慰剂能提高有效率和延长无进展生存期。Pirker等[28]在1 125例表皮生长因子表达的患者进行的Ⅲ期随机对照试验中,NP方案联合或不联合西妥昔单抗,并报道了西妥昔明显延长了患者的生存期。因此,化疗联合靶向治疗将会在未来晚期NSCLC治疗中发挥重要的作用。
本系统评价存在一定的局限性:(1)通过漏斗图评估发表偏倚风险结果显示,发表偏倚风险对meta分析结果的影响不大,但仍然可能存在因阴性结果而未能公开发表的研究,目前已实行的全球临床试验注册制度对控制发表偏倚十分重要;(2)因化疗很难达到完全双盲,故各纳入研究均未采用盲法,存在偏倚的可能性,尚无有效的解决办法;(3)部分测量指标报道不充分或随访时间短,导致纳入数量少,使论证强度受影响;(4)纳入一些小样本研究包含的结果可能不可靠。
TP、TC或 NP方案治疗晚期NSCLC患者时,在有效率和生存率相近的情况下,不良反应在选择TP、TC或NP方案时可提供参考,因此,在前面研究的基础上认为:在有效控制血小板减少的情况下,可能TP和TC方案(尤其是TC方案)的耐受性更强,将会有助于提高患者生活质量及治疗的依从性;但对不能耐受血小板减少的患者,NP方案可能相对理想。总之,在充分考虑预期疗效和不良反应的基础上对患者个体耐受能力进行评估,从而选择和制定出个体化的最佳化疗方案;同时需要更多的大样本、多中心、随机对照试验进一步提供更可靠的证据。
[1] 王果兵,熊光明,罗小平.支气管肺癌肿瘤滋养动脉超选择性插管化疗栓塞的临床价值[J].重庆医学,2008,37(10):1067-1069.
[2] D'Addario G,Pintilie M,Leighl NB,et al.Platinum-based versus non-platinum-based chemotherapy in advanced non-small cell lung cancer:a meta-analysis of the published literature[J].J Clin Oncol,2005,23(13):2926-2936.
[3] Grossi F,Aita M,Defferrari C,et al.Impact of third-generation drugs on the activity of first-line chemotherapy in advanced non-small cell lung cancer:a meta-analytical approach[J].Oncologist,2009,14(5):497-510.
[4] Kelly K,Crowley J,Bunn PA,et al.Randomized phase III trial of paclitaxel plus carboplatin versus vinorelbine plus cisplatin in the treatment of patients with advanced Nonsmall-cell lung cancer:A Southwest Oncology Group T rial[J].J Clin Oncol,2001,19(13):3210-3218.
[5] Scagliotti GV,Marinis FD,Rinaldi M,et al.Phase III randomized trial comparing three platinum-based doublets in advanced Non-small-cell lung cancer[J].J Clin Oncol,2002,20(21):4285-4291.
[6] Jadad AR,Moore RA,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary?[J].Control Clin Trials,1996,17(1):1-12.
[7] Chen YM,Perng RP,Shih JF,et al.A randomised phase II study of weekly paclitaxel or vinorelbine in combination with cisplatin against inoperable non-small-cell lung cancer previously untreated[J].British Journal of Cancer,2004,90(2):359-365.
[8] Ohe Y,Ohashi Y,Kubota K,et al.Randomized phase III study of cisplatin plus irinotecan versus carboplatin plus paclitaxel,cisplatin plus gemcitabine,and cisplatin plus vinorelbine for advanced non-small-cell lung cancer:Four-Arm Cooperative Study in Japan[J].Annals of Oncology,2007,18(2):317-323.
[9] 林燕蓉,赵玉亮,于晶琳,等.NP方案与TP方案治疗晚期非小细胞肺癌临床分析[J].中国肿瘤临床与康复,2004,11(5):409-412.
[10]施亚斌,朱雪红,何景生,等.TC与NP方案治疗晚期非小细胞肺癌的疗效对比观察[J].实用癌症杂志,2005,20(6):622-629.
[11]刘联,王秀问,黎莉,等.含顺铂的三组联合化疗方案治疗晚期非小细胞肺癌的随机对照临床研究[J].癌症,2006,25(8):990-994.
[12]谢伟敏,周文献,刘志辉,等.TC方案与NP方案治疗非小细胞肺癌的随机对照研究[J].肿瘤研究与临床,2006,18(1):32-34.
[13]辛亮,谢广茹.NP与TP及GP方案治疗晚期非小细胞肺癌的近期疗效观察[J].中华肿瘤防治杂志,2006,13(23):1808-1810.
[14]郭守俊,曾红学,康昭洵,等.长春瑞滨联合顺铂与紫杉醇联合顺铂方案治疗晚期非小细胞肺癌的疗效比较[J].赣南医学院学报,2006,26(4):507-509.
[15]张清君,翟成凯,张祥杰,等.长春瑞滨联合顺铂与紫杉醇联合顺铂治疗晚期非小细胞肺癌临床对照研究[J].中原医刊,2007,34(1):36-37.
[16]安煜致,王新华,张欣.TP与NP方案治疗晚期非小细胞肺癌的比较观察[J].中华肿瘤防治杂志,2007,14(5):399.
[17]江波,赵金奇,涂长玲,等.晚期非小细胞肺癌不同化疗方案的疗效比较[J].实用癌症杂志,2008,23(2):161-172.[18]赵亚超,朱长亮,张志培,等.铂类为基础的三种化疗方案治疗晚期非小细胞肺癌的临床研究[J].现代肿瘤医学,2008,16(3):375-377.
[19]田伶伶.TP方案与NP方案治疗晚期非小细胞肺癌的临床疗效分析[J].中国现代医生,2008,46(11):150.
[20]马英.TP与NP方案治疗晚期非小细胞肺癌比较观察[J].中外医疗,2008,27(29):65.
[21]欧传活,吴建语,刘有滕,等.NP方案与TP方案治疗晚期非小细胞肺癌48例疗效观察[J].广西医学,2009,31(5):659-661.
[22]侯恩存,张海燕.NP方案与TP方案治疗晚期非小细胞肺癌的临床研究[J].重庆医学,2009,38(3):323-324.
[23]李新权.NP方案和TP方案治疗晚期非小细胞肺癌的临床观察[J].中国医药导报,2009,6(11):29.
[24]Non-small cell lung cancer collaborative group.Chemotherapy in non-small cell lung cancer,a meta-analysis usings updated data in individual patients from 52 randomized trials[J].BMJ,1995,311(7010):899-909.
[25]Baggstrom MQ,Stinchcombe TE,Fried DB,et al.Thirdgeneration chemotherapy agents in the treatment of advanced non-small cell lung cancer:ameta-analysis[J].J Thorac Oncol,2007,2(9):845-853.
[26]Goffin J,Lacchetti C,Ellis PM,et al.First-line systemic chemotherapy in the treatment of advanced non-small cell lung cancer a systematic review[J].J Thorac Oncol,2010,5(2):260-274.
[27]Goss GD,Arnold A,Shepherd FA,et al.Randomized,double-blind trial of carboplatin and paclitaxel with either daily oral cediranib or placebo in advanced Non-small-cell lung cancer:NCIC Clinical T rials Group BR24 Study[J].J Clin Oncol,2010,28(1):49-55.
[28]Pirker R,Pereira JR,Szczesna A,et al.Cetuximab plus chemotherapy in patients with advanced non-small-cell lung cancer(FLEX):an open-label randomised phase III trial[J].Lancet,2009,373(9674):1525-1531.


