水稻秸秆木质纤维素水解物中糖的测定方法比较
2011-06-14王明远苏小军熊兴耀
张 薇,姚 青,王明远,苏小军,熊兴耀
(1湖南农业大学理学院,长沙 410128;2湖南轻工业研究所,长沙 410002;3湖南省作物种质创新与资源利用重点实验室,长沙 410128)
水稻秸秆木质纤维素经辐照加酶处理转化的糖组成很复杂,已知的成分由木糖、果糖、葡萄糖、鼠李糖、半乳糖、麦芽糖、纤维二糖、半乳糖醛酸、葡萄糖醛酸等组成。其中糖的种类与含量是将其发酵成燃料乙醇的参考指标[1~6]。目前,有关其糖的测定方法有很多,常用的方法有滴定法、旋光法、薄层法、液相色谱法、气相色谱法、气质联用法、毛细管电泳法、离子色谱法等[7~9]。本文比较了采用液相色谱法、气相色谱法、毛细管电泳法、离子色谱法分离测定木糖、果糖、葡萄糖、鼠李糖、半乳糖、麦芽糖、纤维二糖、半乳糖醛酸、葡萄糖醛酸等组成的混合物。
1 实验材料与仪器
1.1 实验材料
葡萄糖 (AR)、木糖 (GR)、果糖 (AR)、鼠李糖(GR)、半乳糖 (AR)、麦芽糖 (AR)、葡萄糖醛酸 (AR)、半乳糖醛酸(AR)、纤维二糖 (AR)、蔗糖 (AR)、乳糖(AR)等购于天津基准化学试剂有限公司;纤维素酶购于湖南鸿鹰祥生物工程公司;实验所用水都为超纯水。
1.2 实验仪器
离子色谱仪 ICS-3000,美国戴安公司;HP5890气相色谱仪;Agilent HPLC1200液相色谱仪;Beckman P/AGETMMDQ(Beckman公司 )。
2 实验方法
2.1 标准溶液的配制
混合糖溶液 A:精确称取葡萄糖、果糖各 0.0450 g,蔗糖、麦芽糖各 0.0900 g于容量瓶中,用超纯水定容至25 mL,即为 10 mmol/L混合工作对照糖溶液。
混合糖溶液 B:蔗糖、麦芽糖、乳糖各 0.0900 g,葡萄糖0.0450 g于容量瓶中,用超纯水定容至25 mL,即为 10 mmol/L混合工作对照糖溶液。
缓冲液:精密称取吲哚-3-乙酸 0.0175 g,磷酸钠0.0950 g,加入适量超纯水,缓慢滴加 1 mmol/L氢氧化钠,同时搅拌控制 pH值在 11.0以下至吲哚-3-乙酸完全溶解,定容至 50 m L,4℃冰箱备用。
标准溶液:准确称取葡萄糖、鼠李糖、半乳糖、木糖、果糖、纤维二糖、麦芽糖、半乳糖醛酸、葡萄糖醛酸各 0.0500 g于容量瓶中,用超纯水定容至 10 mL,摇匀,再取其中1.00 mL到10 mL容量瓶中,以超纯水稀释至刻度线,摇匀配成 5 mg/L的 9种混合糖标准溶液。
2.2 气相色谱法测定条件
仪器:SP6890气相色谱仪。检测器:FID。分析柱:Agilent HP-1 30 m×0.25 mm×0.25μ m。 载气:N2:40 m L/min,H2:40 mL/min,Air:400 mL/min。柱温:230℃,进样口温度 280℃,检测温度 300℃。
2.3 高效液相色谱法测定条件
仪器:Agilent HPLC1200液相色谱仪。检测器:ELSB-3300(蒸发光散色检测器),要求流动相不含不挥发盐。色谱柱类型尺寸:ZORBAX Eclipse XPB-C18 4.6 mm×250 mm。流动相:乙腈 /水63%/37%。柱温:35℃。 气体流速:1.5 L/min,检测温度 50℃。
2.4 毛细管电泳法测定条件
仪器:Beckman P/AGETMMDQ,二极管矩阵检测器,Beckman System Gold软件,320-pH计。
2.5 离子色谱法测定条件
戴安离子色谱仪 ICS-3000,安培检测器。波形:糖四电位波形。色谱柱类型尺寸:CarboPac PA20分析柱,150 mm× 3 mm,CarboPac PA20保护柱,50 mm×3 mm。电极:Au电极,Ag-AgCl参比电极。淋洗液组成及流速:NaOH/NaOAc,梯度:0~15 min,NaOH 10 mM;25~ 33 min,NaOH 100 mM;35~ 50 min,NaOH 100 mM,NaOAc 120 mM;50.1~ 55 min,NaOH 200 mM;55.1~65 min,NaOH 10 mM 0.48 m L/min。柱温:30℃。进样体积:25μ L。进样方式:自动进样。
3 结 果
3.1 气相色谱法结果
取0.2 mL的标准溶液于20 mL的黑塞管中,加入2 mL硼氢化钠 /二甲亚砜 (2 g/100 mL)溶液,放于40℃水浴90 min。取出加入0.2 mL冰醋酸终止反应,加入 2 mL醋酸酐,0.2 mL1-甲基吲哚反应 10 min,加10 m L双蒸水,然后加入 1 mL二氯甲烷,摇 1 min,静置分层,取出二氯甲烷层,于-20℃冰箱中,待上气相色谱分析。
结果表明,气相色谱法是测单糖的较好方法,但二糖不好气化不好测。
3.2 高效液相色谱法结果
取20 m L的标准溶液于20 mL的容量瓶中,过滤,进样20μL,在上述色谱条件下进行 HPLC分析。
结果表明,高效液相色谱法定量上有优势,进样量能控制,但分离效果不理想。
3.3 毛细管电泳法结果
在电压 29 kV,毛细管内径 50μ m,样品槽温度25℃,毛细管温度25℃,缓冲体系pH12.31条件下对混合糖溶液 A、混合糖溶液 B进行分离。检测波长 254 nm。
由于在 pH12.31条件下混合糖 B不能完全分离,对pH条件进行进一步摸索。
以 1 mmol/L氢氧化钠调节缓冲液至 pH12.25,pH12.31,pH12.36,pH12.40,pH12.46,用 0.22 μ m的水膜过滤后对混合糖溶液 B进行电泳分析。
缓冲液 pH12.31条件下,混合糖溶液 A分离图谱如图 1。缓冲液 pH12.31条件下,混合糖溶液B分离图谱如图 2。
在这一条件下虽然大部分糖类可较好分离但仍有部分重合现象,特别是麦芽糖和葡萄糖这两个稻秆木质纤维素水解液中常会出现的糖无法分离。
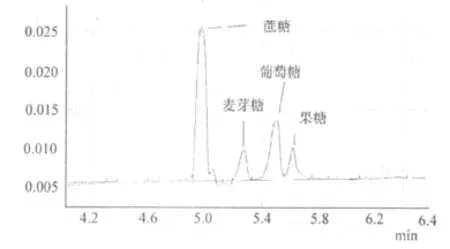
图1 混合糖磷酸缓冲体系分离图谱Fig.1 Seperation of sugars in phosphate buffer
缓冲体系 pH改变实验中,直到 pH达到 12.46,混合糖溶液B中的各种糖才得到完全分离,图谱如图 3。
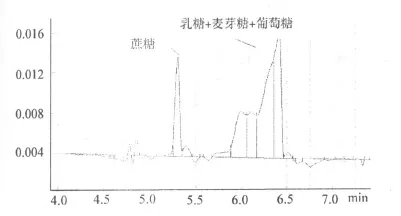
图2 磷酸缓冲体系pH12.31下蔗糖、麦芽糖、乳糖、葡萄糖分离图谱Fig.2 Seperation of sugars in phosphate buffer(pH12.31)
比较图 2、图 3可以看出,适当提高 pH值至pH12.46分离效果有所改善,但是其峰对称性差等问题仍无法解决,而且分离过程中电流明显加大。

图3 磷酸缓冲体系pH12.46下蔗糖、麦芽糖、乳糖、葡萄糖分离图谱Fig.3 Seperation of sugars in phosphate buffer(pH12.46)
3.4 离子色谱法结果
取标准溶液,经过 0.22μ m尼龙滤膜和OnGuard II RP柱(2.5 cc,经甲醇和水活化),弃去初始 6 mL后收集1 mL流出液,在NaOH/NaOAc梯度程序直接进样分析。结果见图 4。

图4 标准溶液的离子色谱图Fig.4 The chromatogram of 9kinds of sugar 5mg/L mixed standard solution
离子色谱法结果表明,在同一根色谱柱 (如CarboPac PA20)、同一个梯度程序中,可同时检测单糖、二糖等,分离效率高。
4 结 论
目前对糖类化合物定性定量的测定方法,主要有气相色谱法、液相色谱法、毛细管电泳法、离子色谱法等,这些方法在测定低含量的糖类化合物时,除离子色谱法外,需对样品进行柱前衍生或柱后衍生,操作步骤繁琐,所需时间较长,人力和物力成本较高。气相色谱法是测单糖的较好方法,但二糖不好气化不好测。高效液相色谱法定量上有优势,进样量能控制,但分离效果不理想。毛细管电泳法具灵敏度高、选择性好、分离效率高等特点,但需对样品进行柱前衍生。而离子色谱法使用了脉冲安培检测器,这种检测器可对糖类化合物直接进行检测,无需衍生,可直接进样,样品处理方法非常简单,安培检测法具有非常高的灵敏度,且具有选择性,可同时检测多种糖,在测定中,同时分离了鼠李糖、半乳糖、葡萄糖、木糖、果糖、纤维二糖、麦芽糖、葡萄糖醛酸、半乳糖醛酸,几种糖之间的分离度均大于1.5,实现了基线分离,本方法对于糖的检测限可低至pmol水平。故毛细管电泳法、离子色谱法可用于稻秆木质纤维素水解液中糖组分的分离测定。
[1]韩鲁佳,闫巧娟,刘向阳,等.中国农作物秸秆资源及其利用现状 [J].农业工程学报,2002,18(3):87-91.
[2]陈静萍 ,王克勤,熊兴耀,等.γ射线对稻草纤维组织及酶解效果的影响[J].核农学报,2005,22(3):304-309.
[3]彭 维,向志明.水稻秸秆的纤维素酶水解研究 [J].四川食品与发酵,2007,43(3):11-15.
[4]曲音波.纤维素乙醇产业化 [J].化学进展,2007,19(7/8):1098-1108.
[5]孙多志,许庆利,王 复,等.木质纤维素制取燃料乙醇水解工艺技术进展 [J].河南化工,2008,25(4):114.
[6]龚大春,田毅红,李德莹,等.纤维素乙醇的研究进展 [J].化学与生物工程,2007,24(1):4-6.
[7]余兆楼,常理文,胡喜章,等.单糖的高效毛细管电泳间接紫外检测法研究 [J].分析化学,1994,22(8):755-758.
[8]林雁飞,何 进,操丽丽,等.高效毛细管电泳法测定蜂蜜中的多种糖 [J].分析测试学报,2005,24(4):74-76.
[9]赵 燕,刘 莉,杨兴斌,等.高效毛细管电泳法测定唐古特大黄多糖中单糖的组成 [J].医药导报,2005,24(11):981-983.
