雷公藤红素逆转K562/A02细胞多药耐药的实验研究
2011-06-07马保根翟亚萍李玉龙
胡 婕 张 茵 马保根 翟亚萍 李玉龙 程 薇
白血病是造血系统常见的恶性肿瘤,目前常用的治疗方法是化疗,虽然化疗能使多数患者达到缓解,但仍有大部分患者因为化疗失败而死亡。导致化疗失败的原因有很多,其中最主要的是白血病细胞的多药耐药(MDR)性的产生。这也是国内目前研究的热点。
雷公藤红素(celastrol)是1种三萜类天然化合物,又名南蛇藤素,具有免疫抑制、抑制血管内皮细胞体外增值、抑制HMC-1细胞的黏附及其黏附分子表达,雷公藤红素还能体外诱导非小细胞肺癌细胞株H1299、人急性髓系白血病细胞株HL-60、恶性胶质细胞瘤株、视网膜母细胞瘤等肿瘤的凋亡。最近有报道雷公藤红素为1种蛋白酶体抑制剂[1]。本实验对雷公藤红素逆转K652/A02细胞多药耐药进行探讨。
1 材料与方法
1.1 细胞株来源
人慢性粒细胞白血病红白血病急粒变耐阿霉素K562/A02细胞株由山东大学齐鲁医院纪春岩教授惠赠。人慢性粒细胞白血病红白血病急粒变K562细胞株由郑州大学干细胞中心常规传代培养。
1.2 主要仪器和试剂
雷公藤红素(Celastrol,Solarbio 纯度>98%)以DMSO(Sigma公司)助溶为1 mmol/L浓度保存于-20℃冰箱备用;CCK-8试剂盒为武汉博士德生物工程有限公司产品;P-gp抗体为上海晶天生物科技有限公司产品;阿霉素(ADM)为浙江海正药业有限公司产品;维拉帕米为上海禾丰制药有限公司产品;RPMI-1640培养基为GIBCOBRL公司产品;新生牛血清为杭州四季青产品;流式细胞仪(FACSCalibur )为美国BD公司产品;酶标仪(Bio-RAD680)。
1.3 方法
1.3.1 细胞培养和实验分组 K562细胞培养于含10%新生牛血清、100 U/ml青霉素和100 μg/ml链霉素的RPMI-1640培养液中,K562/A02细胞培养于含阿霉素(1 μmol/L)的上述培养基中,将2种细胞置于37℃、5%CO2培养箱中常规培养,2~3天传代1次,其中K562/A02细胞在实验前两周改用无阿霉素的培养基培养。取对数生长期细胞用于实验。实验分组如下:①K562细胞+ADM; ② K562细胞+雷公藤红素;③K562/A02细胞+ADM;④ K562/A02细胞+雷公藤红素;⑤ K562/A02细胞+ADM+雷公藤红素。
1.3.2 CCK-8法检测ADM、雷公藤红素的细胞毒性及耐药细胞的耐药倍数 取对数生长期的K562和K562/A02细胞(2~3×104cell/孔)于96孔板中,由高到低浓度分别加入ADM(160、80、40、20、10、5、2.5、1.25 μmol/L),雷公藤红素(320、160、80、40、20、10、5、2.5 μmol/L),每孔设3个平行孔,终体积为150 μl。在37℃、5%CO2培养箱中培养72 h后,每孔加入CCK-8试剂10 μl,继续培养2 h,以空白孔调零,全自动酶标仪于450 nm处测吸光度值,参比波长为650 nm,采用SPSS16.0软件计算生长抑制率50%时的药物浓度即半数抑制率(IC50)[2,3]。抑制率(%)=(1-实验组OD值/对照组OD值)×100%;耐药倍数=(耐药细胞的IC50/敏感细胞的IC50)。实验重复3次,取平均值。
1.3.3 CCK-8法检测雷公藤红素耐药逆转性 取对数生长期的K562/A02细胞(2~3×104个细胞/孔)于96孔板中。实验分组:①K562/A02,②K562/A02+雷公藤红素,③K562/A02+VLP。所加ADM等药物浓度同上,每孔设3个平行孔,终体积为150 μl。并用维拉帕米(VLP)组5 μg/L作为阳性对照[4]。在37℃、5%CO2培养箱中孵育72 h后加入10 μl CCK-8,继续培养2 h后,以空白孔调零,检测波长同上。计算半数抑制率(IC50)。实验重复3次。逆转倍数=(耐药细胞逆转前的IC50/耐药细胞逆转后的IC50)。
1.3.4 流式细胞术检测K562和K562/A02细胞内的ADM浓度 取对数生长期细胞于24孔板中,实验分6组:① K562/A02,② K562/A02+ADM,③ K562/A02+ADM+雷公藤红素(IC10),④ K562/A02+ADM+雷公藤红素(IC50),⑤ K562,⑥K562+ADM。第③、④组分别先加入IC10和IC50的雷公藤红素,24 h后在第②③④⑥组中再加入ADM10 μg/ml,药物作用3 h,收集细胞1×106个细胞,冷PBS(4℃,0.01 mol/L,PH7.4)洗涤2次,再重悬于冷PBS液中,4℃保存至上样进行流式细胞仪检测(激发波长Ex=488 nm,发射波长Em=575 nm)[5]。
1.3.5 流式细胞术检测P-gp表达 取对数生长期细胞于24孔板中,实验分4组分别为:①K562/A02,②K562/A02+ADM(IC50),③K562/A02+雷公藤红素(IC50),④K562/A02+ADM(IC50)+雷公藤红素(IC50);置培养箱孵育48 h后,收集细胞,约3×105个细胞,用冷的PBS液洗2遍,按操作说明加入P-gp抗体,室温下避光孵育30 min后上流式细胞仪检测,并给出相应的P-gp表达率。
1.4 统计学处理
2 结果
2.1 雷公藤红素对K562、K562/A02细胞的增殖抑制作用
雷公藤红素对K562及K562/A02抑制率见表1。雷公藤红素对K562和K562/AO2细胞的IC50分别为(411.59±26.551)μmol/L和 (295.58±23.288)μmol/L,两者差异明显(P<0.05),说明K562/A02细胞对雷公藤红素不具有耐药性。ADM对K562、K562/A02的IC50分别为(0.749±0.741)μmol/L、(59.755±6.883)μmol/L,耐药倍数为79.78倍,说明K562/A02对ADM有明显的耐药性(P<0.05)。细胞毒剂量的雷公藤红素可降低ADM对K562/A02细胞的IC50,提高对ADM的敏感性,应用雷公藤红素后,IC50为(0.507±0.070)μmol/L,与单用ADM组比较明显下降(P<0.05),耐药性逆转倍数(RF)为117.860倍;而加入5 μg/L维拉帕米后的IC50为(17.196±6.303)μmol/L,也明显低于单用ADM组(P<0.05),RF为3.745,见表2。
2.2 雷公藤红素对K562/A02细胞内阿霉素浓度的影响
应用流式细胞仪(FCM)检测K562/A02细胞内的ADM浓度。由表3可见加入雷公藤红素后,细胞内的ADM浓度明显增加,加入IC10浓度的雷公藤红素和IC50浓度的雷公藤红素后,细胞内阿霉素浓度差异显著(P<0.05)。

表1 雷公藤红素和阿霉素对K562、K562/A02细胞的增殖抑制作用
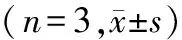
表2 雷公藤红素对K562/A02细胞耐药性的逆转
注:与K562/A02+ADM组比较,△、☆为P<0.05

表3 雷公藤红素对K562/A02细胞内ADM荧光强度的影响
注:与第②组比较,※、#为P<0.05;与第③组比较,★为P<0.05
2.3 流式细胞仪(FCM)检测P-gp表达
从图1中可见,单用阿霉素对P-gp表达无明显影响;但应用雷公藤红素能明显减弱P-gp的表达,且加用ADM后,P-gp表达也明显下降。
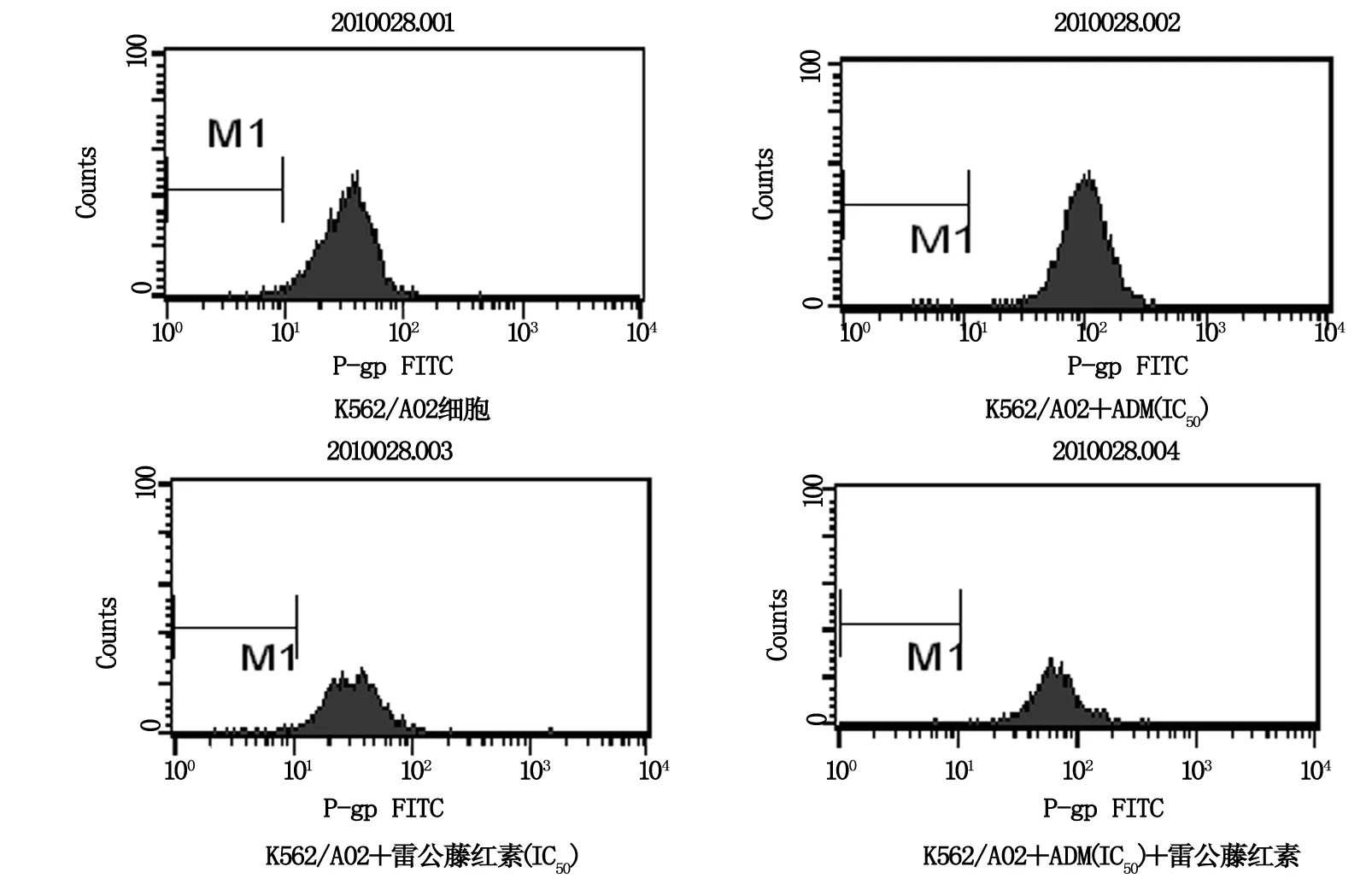
图1 流式细胞仪检测P-gp表达结果图中波峰高度为P-gp的表达强度
3 讨论
多药耐药(multidrungresistance,MDR)是指肿瘤细胞对1种抗肿瘤药物产生耐药性的同时,对结构和作用机制完全不同的其他多种抗肿瘤药物产生交叉耐药性。肿瘤对化疗药物产生多药耐药性(MDR)是导致治疗失败的主要原因之一。目前研究表明MDR的产生有多种机制,主要有[6]:①肿瘤细胞表面ATP结合膜蛋白的表达增加或活性提高,包括P糖蛋白( P-gp)、多药耐药相关蛋白(MRP)、肺抗药性相关蛋白(LRP)、乳腺癌抗药性相关蛋白(BRCP)等几类;②谷胱甘肽S转移酶(glutathione S transferase)的表达增加或活性增强;③TOPOⅡ含量减少及活性降低;④蛋白激酶C(protein kinase C,PKC)的表达增加或活性增强;⑤肿瘤细胞抗凋亡能力增强。其中P-gp介导的MDR是研究最多最为广泛的机制之一,被称为多药耐药的经典途径[7]。
P糖蛋白(P-glycoprotein,P-gp)是由位于人7q21.1的多药耐药基因1(MDR1)编码,Juliano在1976年发现P-gp后,已经证实P-gp高表达为MDR的主要机制。P-gp可以通过它的疏水位点与疏水性抗肿瘤药物结合,通过ATP水解供能,逆浓度梯度将药物泵出细胞外;还可以使从而使药物浓度低于杀伤浓度;还可以使药物在细胞内再分布,导致药物聚集于与药物作用无关的细胞器如溶酶体内,从而使肿瘤细胞发生MDR[8]。P-gp蛋白的荧光强度与细胞膜上蛋白的表达量成正比。
雷公藤红素对多种肿瘤细胞有杀灭作用和对肿瘤血管的生成有直接抑制作用,其抑瘤率达65%~93%,已超过紫杉醇[9]。但是其阻滞细胞周期[10]、激活经典凋亡途径的毒性也限制了它的使用[11]。本研究显示雷公藤红素对K562/A02细胞有抑制作用,为进一步观察雷公藤红素逆转的机制,运用流式细胞仪对MDR1所表达的P-gp及其功能进行了研究,结果显示细胞毒剂量的雷公藤红素能明显降低P-gp的表达,而且用雷公藤红素后,细胞内的ADM浓度明显增加,并与所加雷公藤红素的剂量呈正相关,提示雷公藤红素由于下调了P-gp的表达,使其将化疗药泵出细胞的功能受抑,使化疗药在白血病细胞内能达到有效地浓度,从而可以杀死白血病细胞,达到逆转白血病细胞耐药的目的。但是经典的抗肿瘤药物或低毒的中药制剂在临床应用中仍受到剂量的限制。本研究实验结果表明雷公藤红素在体外可以达到很好的逆转效果,为临床应用提供了一个实验依据,但体内能否达到类似的逆转效果有待进一步的工作。
[1] Yang HJ,Chen D,Cui QZ,et al.Celastrol,a Triterpene Extracted form the Chinese“Thunder of God Vine,”Is a potent Proteasome inhibitor and Suppresses Human Prostate Cancer Growth in Nude Mice 〔J〕.Cancer Res,2006,66(9):4758.
[2] 赵 斌,葛金芳,朱娟娟,等.小议在MTT法测细胞增殖抑制率中IC50的计算方法〔J〕.安徽医药,2007,11(9):834.
[3] 周一平.用SPSS软件计算新药的LD50〔J〕.药学进展,2003,27(5):314.
[4] 孙海英,李德志,徐开林,等.硼替佐米对白血病K562/A02细胞药物增敏效应的实验研究〔J〕.中华血液学杂志,2009,30(1):58.
[5] 王 婷,双跃荣,庄小捷,等.川芎嗪联合三氧化二绅逆转K562/ADM细胞多要耐药的实验研究〔J〕.实用癌症杂志,2009,24(2):121.
[6] 于 韬,赵桂森,臧恒昌,等.肿瘤多药耐药逆转剂研究进展〔J〕.中国药物化学杂志,2003,13:172.
[7] Norgaard JM,Hokland P.Biology of multiple drug resistance in acute leukemia〔J〕.Int J Hematol,2000,72:290.
[8] 陈孝堂,陈 筠.P糖蛋白介导的多药耐药及其逆转的研究进展〔J〕.山西医药杂志,2007,11:1005.
[9] 徐铮奎.开发雷公藤单体成分新药市场前景广阔〔J〕.中国医药工业杂志,2006,37(10):130.
[10] 周幽心,孙成法,许期年,等.雷公藤红素抑制血管内皮细胞株增值的体外研究〔J〕.实用癌症杂志,2004,19(6):564.
[11] 冯继明,余燕敏,安增梅,等.雷公藤多甙对成人隐匿性自身免疫性糖尿病患者谷氨酸脱羧酶抗体和B细胞功能的影响〔J〕.中国医药,2006,1(8):468.
