甲基红褪色光度法测定自来水中的二氧化氯
2011-04-07陈梅梅李凤月刘晓庚
陈梅梅,高 梅,董 晗,李凤月,刘晓庚*
(南京财经大学,江苏 南京 210003)
甲基红褪色光度法测定自来水中的二氧化氯
陈梅梅,高 梅,董 晗,李凤月,刘晓庚*
(南京财经大学,江苏 南京 210003)
探讨以二氧化氯(ClO2)氧化甲基红(MR)褪色光度法测定自来水中ClO2的新方法。在c(MR):c(ClO2)=6.4:1、pH4.0~4.5、温度25℃、反应时间40min条件下,以λmax=518nm测定ΔA518。结果其线性方程为ΔA518=-1.7845c(ClO2)+1.5228(r=0.992),表观摩尔吸光系数ε=1.2×105L/(mol·cm),适用测定范围为0.0004~0.80mg/L,DL为0.0036mg/L;ClO2氧化MR褪色反应具有一级反应的特点,在25℃的动力学方程为ln[c∞/(c∞-c)]=-0.000689t+2.263669、Ea为87.3kJ/mol、t1/2为16.8min。本法经自来水和消毒剂中ClO2含量的测定结果表明,相对标准偏差为2.43%~3.83%,加标回收率为98.2%~103.2%。经F检验和t检验,本法与对氨基-N,N-二乙基苯胺(DPD)光度法不存在显著差异(P=0.05),测定结果符合分析的要求。
自来水;杀菌消毒剂;二氧化氯;甲基红;褪色光度法
二氧化氯(ClO2)是一种新型安全广谱高效杀菌消毒剂,不仅杀菌效果比一般含氯消毒剂高2.5倍,而且杀菌消毒过程中不使蛋白质变性,对动物的细胞无影响,不产生致癌、致畸、致突变等副作用[1]。因此,它被广泛用作水的处理、果蔬和肉品等食物的消毒保鲜、面粉的增白、食品用具及食品生产场地的杀菌消毒等[1-3]。沈丽娜等[4]综述了测定ClO2的方法,主要有碘量法、电流滴定法、光度法、流动注射分析、电化学法、生物法、色谱法等,其中碘量法为标准方法之一[5]。褪色光度法测定ClO2虽有操作简便快捷等优点而倍受关注[6-9],但有的方法存在重现性不好或灵敏度不高或显色剂不易得等。甲基红(methyl red,MR)褪色光度法测定ClO2尚未见报道,且该方法保持了褪色光度法的优点又可以克服其不足,本实验采用甲基红褪色光度法测定自来水中的二氧化氯,实样测定结果令人满意。
1 材料与方法
1.1 试剂与仪器
稳定型二氧化氯液 南京挪亚化工有限公司;二氧化氯消毒粉 南京理工水夫环保科技有限公司;实验所用其他试剂均为分析纯;水为蒸馏水。
UV1102紫外-可见分光光度计 上海天美科学仪器有限公司;722N可见分光光度计 上海精科仪器有限公司;THZ-82A水浴恒温振荡器 金坛市荣华仪器制造有限公司;BS224S 电子分析天平 北京赛多利斯仪器系统有限公司;HH-4型数显恒温水浴锅 国华电器有限公司;QY-200A移液器 北京青云卓立精密仪器有限公司。
1.2 方法
1.2.1 测定原理
何尤琥等[10]、刘作华等[11]研究表明,在偶氮染料的氧化降解过程中,偶氮旁边的C-N键比N=N本身具有更高的活性而首先断裂,偶氮键一直保留到最终生成N2。MR属偶氮化合物,其氧化降解过程如图1所示。因此,MR因降解而褪色,而且实验表明这种褪色程度与氧化剂的量有确定的函数关系,故可用于ClO2的定量分析。
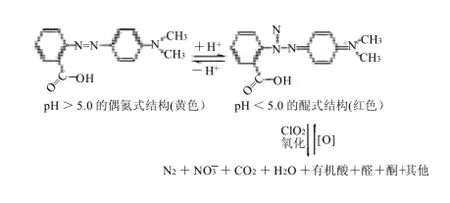
图1 偶氮染料的氧化降解过程示意图Fig.1 Schematic diagram for oxidative degradation of azo dyes
1.2.2 测定方法
在洁净的25mL具塞比色管中,依次加入一定量酸度调节液、0.1000g/L MR-乙醇混合液(其中含干扰离子消除剂EDTA质量浓度为0.60g/L),混匀后,再准确加入一定量ClO2溶液,迅速混匀且用蒸馏水定容至25.00mL,恒温(25℃)条件下反应一段时间。以ClO2试样空白为参比,用1.0cm比色皿于λmax=518nm(图2)处测定其吸光度(A518nm)。

图2 甲基红测定二氧化氯吸收曲线Fig.2 Absorption spectra of MR in solutions with different ClO2concentrations
2 结果与分析
2.1 测定条件的选定
2.1.1 吸收光谱
按实验方法加入不同量ClO2溶液(以试剂空白为参比),在紫外-可见分光光度计上扫描,测得光谱图如图2所示,可知MR的最大吸收波长为518nm,加入ClO2后该特征峰明显下降甚至消失。
2.1.2 甲基红加入量的选定
按实验方法,在只改变MR和ClO2加入量的条件下进行实验,其结果见表1。结果表明,在MR混合液加入量不高于1.40mL时,518nm处的特征吸收峰消失,而MR加入量不高于1.60mL时,518nm波长处又出现波峰,但ΔA518(A未加ClO2-A加ClO2)以MR加入量为1.60mL
(即MR与ClO2浓度比为6.4:1)时最大。因此,实验选用MR用量为1.6mL[即c(MR):c(ClO2)=6.4:1]为佳。

表1 甲基红加入量对测定的影响Table 1 Effect of methyl red dosage on ΔA518
2.1.3 反应体系中pH值的选定
按实验方法,在只改变反应体系pH值条件下,测定pH1.9~5.2内ΔA518值,结果见表2。结果表明,当溶液pH4.0~4.5时,褪色最完全,即ΔA518达到最大。由于酸度较高时,对ClO2有破坏作用,在pH值小于3.5时,ClO2来不及与MR反应就被H+分解了,所以pH值小于3.5时ΔA518值较小;但当体系pH值大于MR变色点(pKHIn=5.1)时,吸收曲线的特征吸收峰会位移,因此ΔA518值导致下降。故在本实验选用反应体系pH值应控制在既保证H+对ClO2破坏最小,又不使MR特征吸收峰产生严重位移。即以先加1.5mL HAc-NaAc缓冲液,待加入MR的混合液后再加0.1mol/L硫酸调控的pH4.0~4.5为宜。

表2 pH值对测定结果的影响Table 2 Effect of pH on ΔA518
2.1.4 反应温度的影响
按实验方法,在只改变体系温度条件下,测定5、10、15、20、25、30、40、50℃条件下ΔA518值,结果见表3。结果表明,温度不高于20℃时,反应速率较慢,褪色不明显。温度大于等于40℃时,反应速率过快,反应时间不易控制。所以温度以25~30℃为宜,本实验选用2 5℃。2.1.5 反应时间的影响

表 3 反应温度对测定结果的影响Table 3 Effect of temperature on ΔA518
按实验方法,在只改变反应体系时间的条件下,测定1~40min内ΔA518值,结果见表4。结果表明,该褪色反应时间达到40min后,褪色已完全。所以本实验时间以40min为宜。

表4 反应时间对测定结果的影响Table 4 Effect of reaction time on ΔA518
2.1.6 稳定性实验
按实验方法在加入ClO2前后反应体系中,每隔一定时间分别测得A518值,经过10d连续不断测定(图3),其溶液的A518值无明显改变。可见甲基橙溶液颜色很稳定,加入ClO2后溶液体系褪色后不出现返色,该褪色反应是不可逆的。因此,此褪色法测定是相当稳定的。

图3 反应体系的稳定性Fig.3 Coloration stability of reaction system.
2.1.7 干扰实验
按实验方法,在加入ClO2前向反应体系中分别加入一定量的干扰组分,混匀后再加ClO2定容,测定A518值,在允许相对误差小于等于5%时,测定体系中ClO2100倍量的NaCl、KCl,50倍量的MgCl2、CaCl2、Na2SO4、K2SO4,等量的AlCl3、CuSO4、Na2SO3、Fe2(SO4)3、Cr2(SO4)3,0.2倍量的Fe(NO3)3、Na2CO3、K2CO3,0.08倍量的NaIO3、NaBrO3、KClO3、NaClO,结果对ClO2的测定无干扰。但是即使是0.01倍量的Cr2O62-对ClO2的测定也会产生严重不良影响,其机理有待进一步探明。因此,测定体系中不能有Cr(Ⅵ)的存在,若有应先用Na2SO3或H2O2等还原成无干扰的Cr(Ⅲ)从而掩蔽之。
2.2 线性范围与检出限
在上述选定的实验条件下,通过ClO2质量浓度c/(mg/L)与ΔA518的关系绘制工作曲线,ClO2的线性方程为ΔA518=1.7845c-0.0569(r=0.992)(图4),且适用ClO2质量浓度在0~0.80mg/L范围内。表观摩尔吸光系数为ε=1.2×105L/(mol·cm);测定11批空白样溶液得δ=0.00216mg/L,DL=tf·δ/S,通常在测定次数10~15次时置信因子tf=3,本实验回归方程的斜率为1.7845,于是计算检出限DL=0.0036mg/L。

图4 ClO2质量浓度测定标准曲线Fig.4 Standard curve for ΔA518measurement.
2.3 ClO2降解甲基红的动力学模型的测定
据报道ClO2氧化降解MR这种偶氮苯类化合物使其偶氮双键断裂是符合宏观一级反应动力学模型[14]。一级反应动力学方程为:ln[c∞/(c∞-c)]=-kt+A[c∞为反应平衡时ClO2质量浓度/(g/L),c为反应时间t时ClO2质量浓度/(g/L),t为反应时间/s,A、k为常数]。实验测得在25℃条件动力学方程为 ln[c∞/(c∞-c)]=-0.000689t+2.263669,根据Arrhenius公式可算得该反应活化能Ea=87.3kJ/mol,反应的半衰期为t1/2=(ln2)/k=1006s=16.8min,该t1/2与实验得到的平衡时间(35~40min)的一半十分接近。
2.4 实际样品测定
先将固态的二氧化氯消毒粉和液态稳定性ClO2水处理剂准确配制成约0.5g/L的溶液。分别准确移取一定量试样溶液(自来水样、消毒剂样),按1.2.2节方法测定ClO2含量、加标回收率和精密度等,并与采用对氨基-N,N-二乙基苯胺(N,N-diethyl-p-phenylendiamine,DPD)法测定的结果进行对照。其结果见表5。

表5 自来水和消毒剂中ClO2含量的测定结果(n=5)Table 5 Determination of chlorine dioxide in running water and disinfectant by both MR and DPD method (n=5)
由表5可知,本法的测定结果与被推荐为标准方法的DPD光度法[7-8]的结果完全吻合,经F检验得F=SD大2/SD小2在2.87~5.42范围内,小于临界值F0.05,(4,4)=6.39;而t检验得t=0.056~2.23,小于临界值t0.05,4=2.776;由此可见,两种方法不存在显著差异,因此,本法应用自来水及消毒剂中的ClO2含量测定是成功的。所测定的实验室自来水和水厂自来水中含ClO2量分别为0.0503、0.2098mg/L,均符合出厂水ClO2限值小于等于0.8mg/L、出厂水ClO2余量大于等于0.1mg/L、管网末梢水ClO2余量大于等于0.02mg/L的我国自来水卫生标准[12]。二氧化氯消毒粉(固体稳态二氧化氯)有效二氧化氯含量的测定结果为5.661%~6.860%,平均值为6.168%。
3 结 论
在c(MR):c(ClO2)=6.4:1、pH4.0~4.5、温度25℃、反应40min、λmax=518nm条件下测定ΔA518,用MR褪色分光光度法测定ClO2是可行的,且本法ClO2测定适用范围为0.0004~0.80mg/L,其方程为ΔA518=-1.7845c+1.5228(r=0.992),DL为0.0036mg/L。ClO2氧化MR褪色反应具有一级反应的特点,在25℃的动力学方程为ln[c∞/(c∞-c)]=-0.000689t+2.263669,Ea=87.3kJ/mol,t1/2=16.8min。本法用于不同自来水和消毒剂的测定结果表明,RSD为2.43%~3.83%,加标回收率为98.2%~103.2%。经F检验和t检验,本法与DPD分光光度法不存在显著差异(P≥0.05),测定符合分析测定之要求。本方法具有操作简捷、灵敏、快速、干扰少等优点,能满足水和消毒剂中ClO2的测定。可见本方法用于水和消毒剂中ClO2含量的测定是可靠且可行的。
[1] 马小燕, 刘秀英. 二氧化氯的应用研究与进展[J]. 环境与健康杂志, 1998, 15(2): 95-96.
[2] 傅茂润, 杜金华. 二氧化氯在食品保鲜中的应用[J]. 食品与发酵工业, 2004, 30(8): 113-116.
[3] FU Yucheng, ZHANG Kaili, WANG Niya, et al. Effects of aqueous chlorine dioxide treatment on polyphenol oxidases from Golden Delicious apple[J]. LWT - Food Science and Technology, 2007, 40(8): 1362-1368.
[4] 沈丽娜, 朱明新, 赵贤广, 等. 二氧化氯检测分析方法的进展[J]. 工业水处理, 2010, 30(1): 4-7.
[5] GB/T 20783—2006 稳定性二氧化氯溶液[S].
[6] 赵金玉, 张鑫. 退色型间接分光光度法测定水中二氧化氯含量[J]. 安徽农业大学学报, 1994, 21(2): 206-209.
[7] 杨卫权, 胡锋平. DPD光度法测定二氧化氯[J]. 华东交通大学学报, 1996, 13(3): 28-31.
[8] 刘希东. 氯酚红褪色光度法测定痕量二氧化氯[J]. 西南师范大学学报: 自然科学版, 2001, 26(4): 424-426.
[9] 梁爱惠, 蒋治良. 吖啶橙分光光度法测定水中痕量二氧化氯[J]. 桂林工学院学报, 2007, 27(1): 125-127.
[10] 何尤琥, 杨银堂. 催化氧化有机染料甲基红脱色的研究[J]. 江西科学, 2005, 23(1): 78-80.
[11] 刘作华. 微波促进含铬矿物催化氧化甲基橙的研究[D]. 重庆: 重庆大学, 2005.
[12] GB 5749—2006 生活饮用水卫生标准[S].
Spectrophotometric Determination of Chlorine Dioxide in Tap Water Using Methyl Red
CHEN Mei-mei,GAO Mei,DONG Han,LI Fen-yue,LIU Xiao-geng*
(Nanjing University of Finance and Economics, Nanjing 210003, China)
A new spectrophotometric method for the determination of chlorine dioxide (ClO2) in tap water was developed based on methyl red (MR) oxidation and discoloration. Wavelength scanning showed that MR had maximal absorption at 518 nm. Under the experiment conditions of c(MR)/c(ClO2) = 6.4, pH 4.0-4.5, 25 ℃ and reaction time of 40 min, a linear equation was obtained as ΔA518= -1.7845c(ClO2) +1.5228 (r = 0.992) in the range of 0.0004-0.80 mg/L, the apparent molar absorptivityε = 1.2 × 105L/(mol·cm), and the detection of limit 0.0036 mg/L. MR discoloration by ClO2 oxidation was a first-order reaction. The dynamic equation at 25 ℃ was ln[c∞/(c∞-c)] =-0.000689t + 2.263669 with the activation energy Ea = 87.3 kJ/mol and the half-time t1/2= 16.8 min. The average recoveries for ClO2in tap water and ClO2disinfectant were 98.2%-103.2% (n = 5) with a relative standard deviation of 2.43%-3.83%. This method and the recommended standard N,N-diethyl-pphenylendiamin (DPD) method showed no significant difference (P = 0.05) according to F-test and t-test. Furthermore, satisfying determination results were obtained from this method.
tap water;disinfectant; chlorine dioxide;methyl red;discoloration;spectrophotometry
TS207.3
:A
1002-6630(2011)20-0240-04
2011-03-12
江苏省高校科研成果产业化推进项目(ZL10001)
陈梅梅(1963—),女,馆员,学士,主要从事粮油食品情报研究。E-mail:mmchen6263@126.com
*通信作者:刘晓庚(1962—),男,教授,硕士,主要从事食品化学研究。E-mail:lxg_6288@163.com
