微孔聚氨酯泡沫超声强化化学镀铜的研究
2011-02-07田庆华郭学益
田庆华,郭学益
(中南大学 冶金科学与工程学院 冶金工程博士后流动站,湖南 长沙,410083)
微孔聚氨酯泡沫超声强化化学镀铜的研究
田庆华,郭学益
(中南大学 冶金科学与工程学院 冶金工程博士后流动站,湖南 长沙,410083)
为研制金属泡沫材料电沉积制备所需的导电泡沫基体,以孔径为0.3 mm的微孔聚氨酯泡沫为基体进行化学镀铜新工艺研究。探讨镀液组成、温度、pH及超声强化对化学镀铜工艺的影响,得出化学镀铜优化工艺条件如下:硫酸铜质量浓度为16 g/L,酒石酸钾钠质量浓度为30 g/L,Na2EDTA质量浓度为20 g/L,α,α′-联吡啶质量浓度为25 mg/L,亚铁氰化钾质量浓度为25 mg/L,PEG-1000质量浓度为1 g/L,甲醛含量为5 mL/L,镀液pH为12.5~13.0,温度为50 ℃。在此条件下,镀液稳定性好,镀层光亮平整,镀速可达0.102 mg/min;超声强化可有效提高镀速20%~30%;化学镀铜后的导电泡沫基体经电沉积工艺可制备得到孔隙率为92.2%的三维网状金属泡沫材料。
化学镀铜;微孔;聚氨酯泡沫;超声波;泡沫金属
金属泡沫材料(以下简称泡沫金属)由于具有孔隙率高、比表面积大、质量均匀、活性强等优异性能,被广泛用于催化基体、过滤分离器、热交换器及电极材料等制备领域[1]。电极材料的泡沫金属常采用电沉积法制备,即以聚氨酯泡沫为基体材料,通过表面金属化使其表面导电,并经电沉积制备得到三维网状结构、孔隙率高、结构均匀和机械性能好的泡沫金属[2]。泡沫金属孔径取决于泡沫基体材料的孔径,孔径直接影响泡沫金属电极的性能。当泡沫金属孔径大时,电池的欧姆内阻增大,充放电不完全,需要在电极活性物质中加入导电微粒来降低电池的内阻;加入导电微粒后,会减少电极活性物质;当泡沫金属孔径小时,电池的内阻减小,但孔径过小时,电极活性物质填不进去而集中在电极表面。根据实际生产经验,一般宜选用孔径为 0.2~0.4 mm 的微孔聚氨酯泡沫作为基体材料,最大孔径不宜超过0.6 mm[3]。电沉积法制备泡沫金属的工艺流程为:聚氨酯泡沫→预处理→表面金属化→电沉积→泡沫金属。电极材料一般采用铜集流体,因此,表面金属化可考虑在泡沫基体表面镀覆一层导电性良好的金属铜[3]。表面金属化过程是决定后续电沉积质量的关键,其主要方法有蒸镀(如真空蒸镀)、离子镀(如电弧离子镀)、阴极溅射、化学镀和涂覆导电胶法等多种[4−6]。其中蒸镀、离子镀和涂覆导电胶法的沉积金属与非金属表面为物理吸附,附着力小,容易脱落,一般适用于平面镀覆。化学镀法的沉积金属与基体表面为化学吸附,附着力大,不易脱落[7−10],可用于表面形状复杂的基体镀覆,即使表面形状复杂的基体也可获得均匀镀层。本文作者选用中温碱性化学镀铜体系,研究了各工艺条件对微孔化学镀铜镀速及镀层形貌的影响,并进一步制备得到泡沫金属。
1 实验
1.1 试剂、仪器及主要原材料
主要试剂:CuSO4·5H2O,NaKC4H4O6·4H2O,Na2EDTA,HCHO,亚铁氰化钾,α,α′-联吡啶,PEG-1000,以上试剂均为分析纯。
主要仪器:pHS−3C型精密pH计,DZKW−4型电子恒温水浴锅,FA2004型电子分析天平,KQ−400GQDV型超声波清洗器和JSM−6360LV型扫描电子显微镜。
主要原材料:聚氨酯泡沫(日本 BRIDGESTONE公司生产,平均孔径为0.3 mm,孔隙率为96%)
1.2 实验原理与方法
广义的表面金属化包括脱脂、粗化、敏化−活化和化学镀等步骤。首先,采用有机溶剂脱脂和化学脱脂相去除聚氨酯泡沫表面的脱模剂及污垢,以确保非金属制件表面能均匀地进行表面活化。然后,选用KMnO4(1 g/L)和H2SO4(0.05 mL/L)组成的粗化剂使聚氨酯泡沫骨架表面呈显微粗糙,以利提高金属镀层与非金属基体的结合力。敏化−活化的作用是使基体表面形成一层非连续的催化活性颗粒,使基体表面具有催化还原铜的能力,从而使化学镀铜反应在催化处理过的基体表面顺利进行。
化学镀铜反应是在有催化活性物质(如钯)的表面上,使溶液中的硫酸铜与还原剂甲醛发生氧化还原反应,从而使铜离子还原析出,其总反应为[11]:

化学镀后可采用电沉积法在导电性良好的铜镀层上电镀加厚金属以制备得到泡沫金属。
1.3 微孔泡沫镀速的测定
由于聚氨酯泡沫表面形状复杂,难以计算表面积,故不能采用常规镀速进行定义。本文采用单位时间、单位质量的聚氨酯泡沫上的铜沉积量来定义化学镀铜镀速,计算公式为:

其中:ν为镀速;m1为基体镀前质量;m2为基体镀后质量;t为镀液稳定时间(即活化后的聚氨酯泡沫自放入化学镀液中开始计时,到化学镀液开始变浑浊的时间)。
1.4 孔隙率的测定
泡沫锌的孔隙率计算公式为
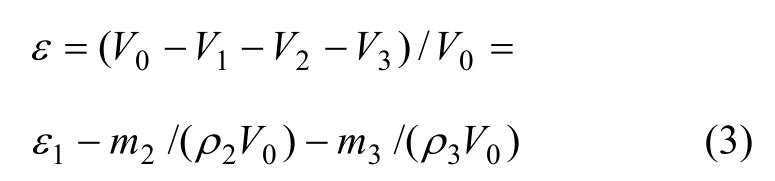
其中:ε为泡沫锌孔隙率;V0为泡沫锌总体积;V1为聚氨酯泡沫所占体积;V2为铜化学镀层所占体积;V3为锌电沉积层所占体积;m2为化学镀铜实际镀铜质量;m3为电沉积锌质量;ρ2和ρ3分别为铜和锌的金属密度;ε1为聚氨酯泡沫基体材料孔隙率。
2 结果与讨论
2.1 硫酸铜质量浓度对化学镀铜的影响
溶液组成为:甲醛5 mL/L,酒石酸钾钠30 g/L,Na2EDTA 20 g/L,α,α′-联吡啶 25 mg/L,亚铁氰化钾25 g/L和PEG-1000 1 g/L。当控制pH为12.5,镀液温度50 ℃时,不同硫酸铜质量浓度对镀速的影响如图1所示。由图1可知:化学镀铜的镀速随着硫酸铜质量浓度的提高而增加。在实验研究中,当硫酸铜质量浓度为8 g/L时,沉铜速度慢,镀层外观暗;当硫酸铜质量浓度为16 g/L,沉铜速度快,镀层外观光亮;但当硫酸铜质量浓度达到20 g/L以后,虽然沉铜速度快,但镀液稳定性极差,镀层粗糙。故本实验研究选用硫酸铜质量浓度为16 g/L。
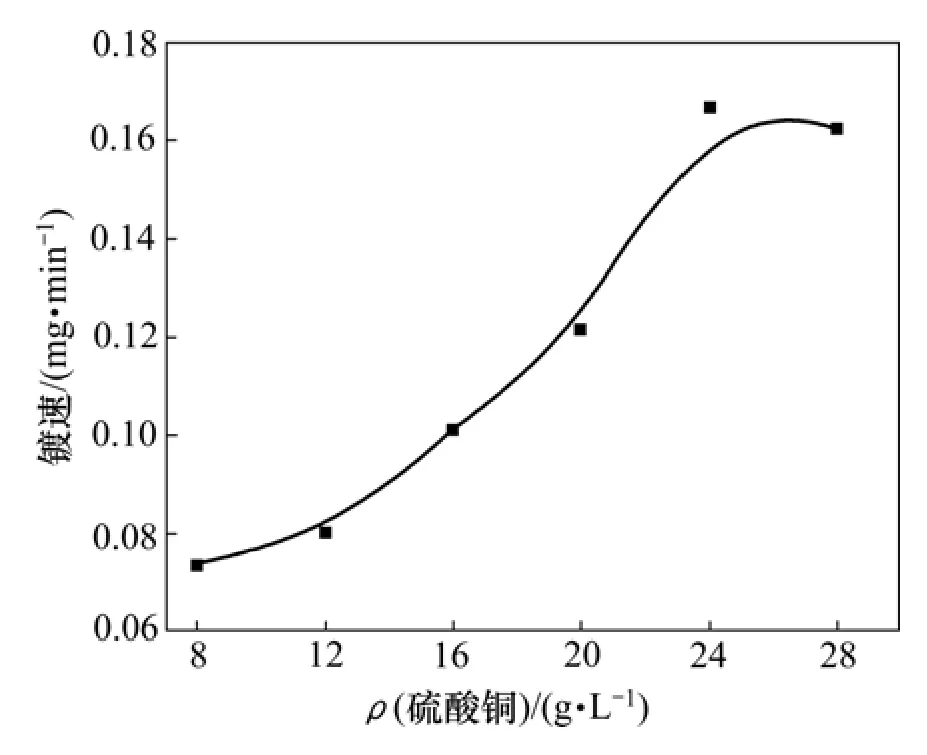
图1 硫酸铜质量浓度对镀速的影响Fig.1 Effect of CuSO4 mass content on plating rate
2.2 甲醛质量浓度对化学镀铜工艺的影响
溶液组成为:硫酸铜16 g/L,酒石酸钾钠30 g/L,Na2EDTA 20 g/L,α,α′-联吡啶 25 mg/L,亚铁氰化钾25 mg/L和PEG-1000 1 g/L。当控制pH为12.5,镀液温度50 ℃时,不同甲醛含量对镀速的影响如图2所示。由图2可见:随着甲醛含量的增加,化学镀铜的镀速明显加快;当甲醛含量为2 mL/L时,沉铜速度慢,镀层表面有暗纹;当甲醛含量为5 mL/L时,沉铜速度较快,镀液稳定,镀层外观光亮;同样,当甲醛含量达到6 mL/L以后,虽然沉铜速度快,但镀液极不稳定,镀层结晶粗糙。故本实验研究选用甲醛含量为5 mL/L。

图2 甲醛含量对镀速的影响Fig.2 Effect of HCHO content on plating rate
2.3 镀液pH对化学镀铜的影响
溶液组成为:硫酸铜16 g/L,甲醛5 mL/L,酒石酸钾钠 30 g/L,Na2EDTA 20 g/L,α,α′-联吡啶 25 mg/L,亚铁氰化钾25 mg/L和PEG-1000 1 g/L,控制镀液温度为50 ℃。由于甲醛必须在pH>11的碱性条件下才具有还原铜的能力,同时,由于化学镀铜过程将产生氢气,使得镀液pH不断降低,必须定期调整镀液pH以维持化学镀铜的进行[11]。本文通过加入NaOH溶液调整镀液pH在11.5~13.5范围内,不同镀液pH对镀速的影响见图3。由图3可见:化学镀铜镀速随镀液pH的增大而加快;当pH≤12时,镀速慢,镀层发暗;当pH为12.5~13.0时,镀液稳定,沉铜速度较快,镀层外观光亮;当pH≥13.5时,由于镀液开始自动分解,镀液中有红色 Cu2O析出,镀层表面粗糙。所以,本实验控制pH为12.5~13.0。
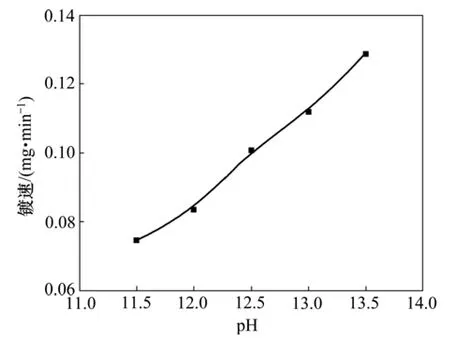
图3 镀液pH对镀速的影响Fig.3 Effect of bath pH on plating rate
2.4 镀液温度对化学镀铜的影响
溶液组成为:硫酸铜16 g/L,甲醛5 mL/L,酒石酸钾钠 30 g/L,Na2EDTA 20 g/L,α,α′-联吡啶 25 mg/L,亚铁氰化钾25 mg/L和PEG-1000 1 g/L,控制pH为12.5。不同镀液温度对镀速的影响如图4所示。从图4可看出:化学镀铜镀速随着温度增加而呈直线增长;当反应温度为20~30 ℃时,沉积铜的速度较慢,镀层发灰暗;当反应温度高于 50 ℃以后,镀液分解速度加快,镀液中产生大量红色 Cu2O粉末;当反应温度控制在40~50 ℃之间时,镀速较快,镀层呈红铜色,且镀液稳定。因此,本实验选用 50 ℃作为化学镀液体系温度。
2.5 双络合剂对化学镀铜的影响
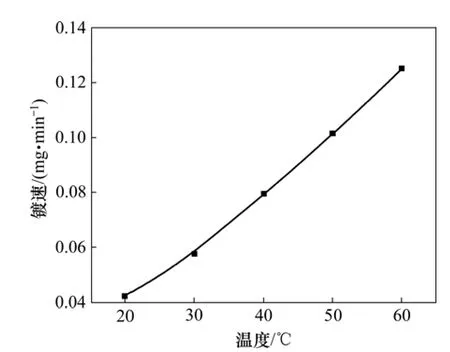
图4 镀液温度对镀速的影响Fig.4 Effect of bath temperature on plating rate
除主盐和还原剂外,镀液中最重要的组成部分是络合剂[12]。镀液中加入适量的络合剂以形成稳定的络合物,有利于细化晶粒,也有利于提高沉积速度及溶液的稳定性,改善化学镀层的性能。本文选用酒石酸钾钠和 Na2EDTA双络合剂体系,溶液组成为:硫酸铜 16 g/L,甲醛 5 mL/L,酒石酸钾钠 30 g/L,α,α′-联吡啶25 mg/L,亚铁氰化钾25 mg/L,PEG-1000 1 g/L。当控制pH为12.5,镀液温度50 ℃时,不同Na2EDTA质量浓度对镀速的影响如图5所示。其他组成及工艺条件不变,保持Na2EDTA质量浓度为20 g/L时,不同酒石酸钾钠质量浓度对镀速的影响见图6。
从图 5和图 6可见:化学镀铜镀速都随着Na2EDTA和酒石酸钾钠质量浓度的增加而减少,当两者质量浓度分别达到20 g/L和30 g/L时,镀速较快,且镀层光亮,镀液较为稳定;当两者的质量浓度过小时,镀速虽然快,但镀液稳定性差,镀层质量差;反之,则镀速很慢。本研究选择质量浓度为 20 g/L Na2EDTA和30 g/L酒石酸钾钠作为双络合剂。

图5 Na2EDTA质量浓度对镀速的影响Fig.5 Effect of Na2EDTA mass content on plating rate
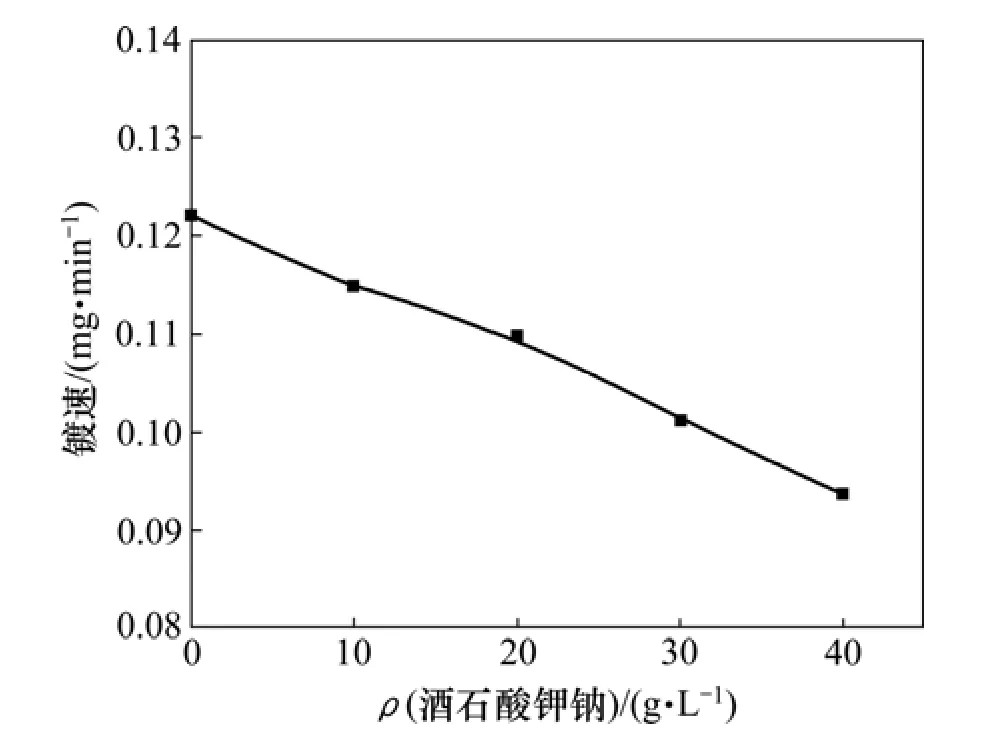
图6 酒石酸钾钠质量浓度对镀速的影响Fig.6 Effect of NaKC4H4O6 content on plating rate
2.6 添加剂对化学镀铜的影响
为了提高镀液稳定性、改善镀层质量等,在镀液中同时加入了亚铁氰化钾、α,α′-联吡啶和 PEG-1000等添加剂。实验结果表明:亚铁氰化钾和α,α′-联吡啶不仅具有稳定镀液的能力,而且可改善镀层的外观,无添加剂时镀层呈褐色;加入亚铁氰化钾镀层呈红褐色;α,α′-联吡啶的加入可使镀层显得红亮。由于化学镀铜过程伴随着氢气的析出,镀层中吸附氢气引起“氢脆”现象而导致镀层质量下降[11],PEG-1000的加入将减少“氢脆”发生,有利于提高镀层质量。本文作者选择质量浓度为25 mg/L的α,α′-联吡啶、质量浓度为25 mg/L的亚铁氰化钾和质量浓度为 1 g/L的PEG-1000作为混合添加体系。
2.7 超声强化对微孔化学镀铜的影响
由反应式(1)可知:化学镀铜的过程伴随氢气产生,生成大量气泡。由于本实验选用的微孔聚氨酯泡沫呈三维网状结构,平均孔径仅为0.3 mm,产生于微孔聚氨酯泡沫大量气泡如不及时排出,不仅大大降低镀速,同时将会造成泡沫深处产生“漏镀”现象,导致后续电沉积出现缺陷[13]。本文作者探索了外加超声场强化化学镀过程,在溶液组成及其他操作条件不变的情况下,将预镀3 min后的聚氨酯泡沫放入功率为400 W的超声场中进行化学镀铜。对比实验结果表明:超声强化可提高化学镀铜镀速20%~30%。既通过超声空化“震碎”原有的气泡而形成微小的气泡,增加了两相接触面积;又利用超声波产生的高速微射流强化了溶液的搅拌,加强了微气泡与镀液金属离子的流动。
2.8 泡沫金属电沉积制备
电极材料常用的泡沫金属主要有泡沫镍、泡沫铅和泡沫锌。作者选择硫酸盐镀液体系进行导电化聚氨酯泡沫的金属锌电沉积研究,镀液配方为:ZnSO4250 g/L,Al2(SO4)320 g/L,KAl(SO4)245 g/L,Na2SO430 g/L,以及硫锌-30光亮剂10 mL/L。以纯锌板作为阳极,在阴极表观电流密度为0.04 A/dm2,电镀液温度为30 ℃,pH为3.5,异极距为4 cm的条件下进行电沉积操作制备泡沫锌。
聚氨酯泡沫及经过化学镀铜−电沉积锌的泡沫锌材料结构形貌用 JSM−6360LV型扫描电子显微镜观察,如图7所示。从图7可见:泡沫锌材料基本上保持了原有聚氨酯泡沫基体的结构形貌,呈三维网状结构,平均孔径为0.3~0.4 mm,组成泡沫锌材料的骨架纵横交错,每一个接点一般由3~5根骨架交叉形成。根据选用聚氨酯泡沫基体初始孔隙率为96%,按式(3)测定估算,泡沫锌孔隙率为92.2%。

图7 泡沫材料制备各阶段扫描电镜照片Fig.7 SEM photos of foam material on different phases
3 结论
(1) 选用平均孔径为0.3~0.4 mm的微孔聚氨酯泡沫作为基体材料进行化学镀铜研究,化学镀铜镀速随着硫酸铜质量浓度、甲醛含量、镀液温度和 pH的增加而增加,随着络合剂酒石酸钾钠和 Na2EDTA质量浓度的增加而降低;镀速越高,铜镀层越松散,镀层表面越粗糙。添加剂 α , α′-联吡啶、亚铁氰化钾和PEG-1000对镀速的影响不大,但对镀层的质量及外观有较大影响。
(2) 确定优化配方和工艺条件为:硫酸铜16 g/L,甲醛5 mL/L,酒石酸钾钠30 g/L,Na2EDTA 20 g/L,α , α′-联吡啶 25 mg/L,亚铁氰化钾 25 mg/L,PEG-1000 1 g/L,控制pH为12.5~13.0,镀液温度为50 ℃。在优化条件下,镀液稳定性好,镀层光亮平整,镀速可达0.102 mg/min。
(3) 聚氨酯泡沫预镀后外加超声强化,可强化溶液搅拌,加强微气泡与镀液金属离子的流动,有效提高镀速20%~30%。
(4) 采用化学镀铜后的导电泡沫基体经电沉积工艺可制备得到呈三维网状结构的金属锌泡沫材料,孔隙率为92.2%。
[1] 田庆华, 李钧, 郭学益. 金属泡沫材料的制备及应用[J]. 电源技术, 2008, 32(6): 417−420.
TIAN Qing-hua, LI Jun, GUO Xue-yi. Preparation and application of foam metal material[J]. Chinese Journal of Power Sources, 2008, 32(6): 417−420.
[2] TIAN Qing-hua, GUO Xue-yi, XUE Ping, et al. Electrodeposition for foamed zinc material from zinc sulfate solution[J].Materials Science Forum, 2007, 561/565(3): 1669−1672.
[3] 田庆华. 电沉积法制备金属锌泡沫材料[D]. 长沙: 中南大学冶金科学与工程学院, 2007: 22−23.
TIAN Qing-hua. Electrodeposition for manufacturing foamed zinc material[D]. Changsha: Central South University. School of Metallurgical Science & Engineering, 2007: 22−23.
[4] 朱若英, 滑均凯, 黄故. 涤纶纺织品真空蒸镀法金属整理的研究[J]. 天津工业大学学报, 2005, 24(6): 23−26.
ZHU Ruo-ying, HUA Jun-kai, HUANG Gu. Research on metallic finishing of polyester textiles by vacuum evaporation[J].Journal of Tianjin Polytechnic University, 2005, 24(6): 23−26.
[5] 骆瑞雪, 李争显. Al2O3陶瓷片上沉积钛膜的研究[J]. 稀有金属快报, 2005, 25(7): 25−27.
LUO Rui-xue, LI Zheng-xian. Investigation of titanium film deposited by arc ion processing on Al2O3ceramics[J]. Rare Metals Letters, 2005, 25(7): 25−27.
[6] 田庆华, 闫剑锋, 郭学益. 化学镀铜的应用与发展概况[J]. 电镀与涂饰, 2007, 26(4): 38−41.
TIAN Qing-hua, YAN Jian-feng, GUO Xue-yi. Research progress on electroless copper plating[J]. Electroplating and Finishing, 2007, 26(4): 38−41.
[7] Harik K, John S, Srinivasan K N, et al. An overall aspect of electroless Ni-P depositions: A review article[J]. Metallurgical and Materials Transactions A: Physical Metallurgy and Materials Science, 2006, 37(6): 1917−1926.
[8] 李开华, 罗江山, 刘颖, 等. 泡沫镍制备中化学镀镍研究[J].强激光与粒子束, 2007, 19(7): 1158−1162.
LI Kai-hua, LUO Jiang-shan, LIU Ying, et al. Electroless plating in synthesizing nickel foams[J]. High Power Laser and Particle Beams, 2007, 19(7): 1158−1162.
[9] 徐智谋, 郑家燊, 刘宏芳, 等. 化学镀制备功能梯度材料的实验研究[J]. 复合材料学报, 2000, 17(4): 66−70.
XU Zhi-mou, ZHENG Jia-shen, LIU Hong-fang, et al.Investigation of production of functionally gradient material by electroless plating[J]. Acta Material Compositae Sinica, 2000,17(4): 66−70.
[10] Khoperia T N. Investigation of the substrate activation mechanism and electroless Ni-P coating ductility and adhesion[J].Microelectronic Engineering, 2003, 69(2/4): 391−398.
[11] 李宁. 化学镀实用技术[M]. 北京: 化学工业出版社, 2004:252−262.
LI Ning. Practical electroless plating technology[M]. Beijing:Chemical Industry Press, 2004: 252−262.
[12] 郑雅杰, 邹伟红, 易丹青, 等. 酒石酸钾钠和EDTA·2Na盐化学镀铜体系[J]. 中南大学学报: 自然科学版, 2005, 36(6):971−976.
ZHENG Ya-jie, ZOU Wei-hong, YI Dan-qing, et al. Electroless copper plating system of potassium sodium tartrate and EDTA·2Na[J]. Journal of Central South University: Science and Technology, 2005, 36(6): 971−976.
[13] 赵鹏, 浦玉萍, 黄春晖, 等. 超声波对聚氨酯泡沫塑料化学镀铜的影响[J]. 材料工程, 2008(4): 43−46.
ZHAO Peng, PU Yu-ping, HUANG Chun-hui, et al. Effect of adding ultrasonic on copper electroless plating of polyurethane foam[J]. Journal of Materials Engineering, 2008(4): 43−46.
(编辑 张曾荣)
Ultrasonic enhanced electroless copper plating on microporous polyurethane foam
TIAN Qing-hua, GUO Xue-yi
(School of Metallurgical Science & Engineering, Central South University, Changsha 410083, China)
In order to get good conductive foam substrates for foam metal materials, a novel method for electroless copper plating on microporous polyurethane foam with diameter of 0.3 mm was proposed. The main factors affecting the plating rate such as the solution composition, temperature, pH and adding ultrasonic were investigated comprehensively.The results show that the optimal conditions are 16 g/L CuSO4, 5 mL/L HCHO, 30 g/L NaKC4H4O6, 20 g/L Na2EDTA,25 mg/L α,α′-Dipyridyl, 25 mg/L K4Fe(CN)6, 1 g/L PEG-1000, at pH 12.5−13.0, temperature 50 ℃. Under above conditions, the process has efficient bath stability with the plating rate up to 0.102 mg/min. The result shows that adding ultrasonic on the process can elevate the plating rate of copper by 20%−30%. Foam metal material with a porosity of 92.2%, and a three-dimensional network structure can be fabricated by electrodeposition after electroless copper plating.
electroless copper plating; microporous; polyurethane foam; ultrasonic; foam metal
TQ153.3
A
1672−7207(2011)01−0011−06
2009−09−06;
2010−01−05
湖南省科技计划项目(2010FJ3117);长沙市科技计划重点项目(K0802027-11)
田庆华(1981−),男,四川宜宾人,博士后,讲师,从事有色金属资源循环利用研究;电话:0731-88877863;E-mail: qinghua@mail.csu.edu.cn
