SOFC复合阳极中的Cu在CeO2表面上沉积的密度泛函研究
2011-02-06余婷吴也凡
余婷 吴也凡
(景德镇陶瓷学院材料学院,江西333001)
0 引言
目前国内外关于SOFC阳极的抗积碳研究往往侧重于对阳极积碳的显微结构表征和电化学性能分析以及材料的配方和工艺方面,而较少对其机理进行深入研究[1],这样就不易从本质上解决中温SOFC阳极的抗积碳等关键技术问题。多组分的Cu、CeO2/ YSZ复合阳极对多种碳氢化合物的直接电化学氧化具有一定的催化活性[2-5]在含Ce的催化剂中,CeO2起着双重作用,它不仅对碳氢化合物有催化作用,而且还起到电子和离子的导电作用。但在Cu-Ce间是否具有协同催化作用的研究上,却有两种不同的观点。不同的观点将导致对阳极进行优化时采取不同的制备工艺。一种观点认为CuO/CeO2复合催化剂对CO和烃类具有极好的催化氧化性能,具有协同作用[6]。另一种观点认为在Cu-CeO2/YSZ复合阳极材料中,Cu仅仅起到电子导体的作用,对碳氢化合物并没有催化作用[7,8]。Gorte等[2-5]在使用Cu-CeO2/YSZ复合阳极方面做了很多创新的工作。氧化铈的晶格中含有高浓度可移动的氧空位,这可为催化剂表面发生的反应提供所需的氧[9]。CeO2还在催化剂中起分散剂的作用,可提高催化剂中金属组分的分散度,增进催化剂的热稳定性和抗烧结能力。同时,CeO2还具有阻止碳沉积和催化碳的燃烧反应的能力。我们注意到多元过渡金属氧化物(含稀土)阳极的多氧化态、多种价态共存的情况不但有助于电子的迁移,还可调节催化剂活性中心的原子与原子之间的几何间距(调节催化剂活性相的表面原子骨架),其电催化剂的活性往往高于固定价态的电催化剂。由于掺杂原子的电负性及半径的不同,可改变原催化剂中原子与原子之间的几何间距和电荷密度,具有改变活性中心的催化活性的作用。由于铈、铜离子半径差别不大,在一定浓度范围内应倾向于生成固溶体。而在实验上能否观察到Cu-Ce间是否存在协同作用,这可能与催化剂的制备方法有关。如果氧化铜、氧化铈的制备原料较粗化,就不易观察到其协同作用。基于Ce4f、O2p和Cu3d轨道上电子的相互作用,Ce的存在还极大地改善了Cu基催化剂对CO的氧化活性。由于Cu2+的价态低于Ce4+,为了保持电荷的平衡,形成了氧离子空穴。EXAFS数据分析显示Cu2+周围存在氧空穴,CeO2具有稳定Cu+的作用。因此关于CuO/ CeO2的催化剂结构、Cu-Ce之间的电子相互作用及氧化还原性能的研究倍受关注[10]。固溶体催化剂中,由于大量氧空穴的存在,降低了氧物种迁移的势能,表面晶格氧与CO反应是反应速率控制步骤。晶格氧的活泼性是对CO催化氧化的关键因素[11]。Cu2+有利于燃烧反应,CuO是重整反应的活性中心,而Cu+是Cu2+到CuO转化的中间态,Cu2+/Cu+和Ce4+/Ce3+之间存在协同作用。在固溶体催化剂中由于Cu能够进入CeO2晶胞,这为电子的传输提供了方便。而在目前关于SOFC中Cu-CeO2/YSZ阳极的研究中,通常过分强调铜主要是起到电子导体的作用[2,3,4,5,7,8],而忽略了Cu-Ce之间的协同相互作用等对提高催化剂的活性的影响,因此有必要加强这方面的研究。本文报道固体氧化物燃料电池中的Cu-CeO2/YSZ复合阳极中的Cu在CeO2表面上沉积的密度泛函研究。
1 实验
所有计算工作都是基于密度泛函方法的从头算量子力学程序,在Materials studio软件包中CASTEP (Cambridge Sequential Total Energy Package)模块上完成的[12],它是一个可以模拟固体、界面和表面的性质,适用于多种材料体系,包括陶瓷、半导体和金属等。在所用的数学模型中,离子实被膺势(即只作用于系统价电子的有效势)所替代。电子波函数通过平面波基组扩展,包括电子与电子相互作用中的交换和相关效应通过局域密度近似(LDA)。CASTEP的高效并行版本甚至可以对含有数百个原子大的体系进行处理。测试内容包括计算单点时SCF的收敛标准,结果发现在2.0×10-6eV/atom已足够好。同样,我们测试出优化时两步之间能量差异为2.0×10-5eV/atom,最大位移为2.0×10-3Å时结果已经足够好。
2 结果与讨论
CeO2具有萤石型晶体结构,其中Ce4+按面心立方排列,O2-则占据由Ce4+构成的全部四面体空隙,而且由Ce4+构成的八面体空隙则全部留空。CeO2经还原可形成非化学计量的缺氧化合物CeO2-x(0<X≤0.5),大量的晶格氧是缺位的,呈现出明显的结构缺陷,其表面氧与体相氧有较高的活动性。尽管大量氧从CeO2晶格中失去,但其萤石结构保持不变。单纯的金属Cu是没有催化活性的,而单一的CeO2氧化活性也并不高,CeO2之间应该存在某种协同作用。XRD、EPR和XPS的结果表明铜的取代形式是离子性取代,离子半径小的Cu2+(离子半径0.072nm)进入CeO2晶胞取代了Ce4+(离子半径0.092nm)的位置,导致了CuO/CeO2固溶体中的CeO2晶胞参数的减小[13]。CuO/CeO2催化剂的相关结构参数见表1。
根据从头计算(abinitio)的原理,在合适的模型下,只需不多的参数,便可计算出体系的能量,可以推断出催化剂在原子层次下的形貌(几何优化)。为考察沉积Cu与CeO2的协同作用,将Cu与CeO2的作用能作了划分,方案分为三步:
(1)计算沉积的所有Cu原子在CeO2表面的总吸附能;

其中,Eads为吸附能;ECu/CeO2为沉积后Cu/CeO2体系的总能量;ECeO2为沉积前CeO2slab的能量;NECu为放置于10×10×10Å晶胞中Cu原子的能量为N则为沉积的Cu原子数目。
(2)通过Cu团簇或者层与10×10×10Å晶胞中孤立Cu原子之间的能量差,计算沉积的Cu之间金属键导致的相互作用;

其中,ECu-Cu为反映沉积的Cu之间的金属性程度。
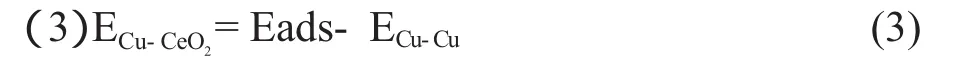
其中,ECu-CeO2为沉积的Cu与CeO2底物的总作用能。
CeO2的态密度计算结果表明,其中Ce-O键定域性较强,带有强的共价性。
关于CeO2表面Cu层的厚度,实验上一般采用的是Cu-Cu层间距2.563A的倍数。但这样的层间距只有当Cu沿其(110)方向生长方可达到(见图1)。
2.1 Cu在表面的沉积
单原子Cu在CeO2表面有三种沉积模式,分别称为在三种模式中Cu都带有正电荷。在中Cu键合于U型槽两侧Ce和O的悬挂键上。在中,Cu键合于相邻平行的两个Ce-O上,位于V型槽上方。在C中,Cu位于表面Ce-O键正上方,成键前后表面Ce-O键并未明显拉长,推测其键合模式为键合在Ce-O键的成键轨道上(见表2)。
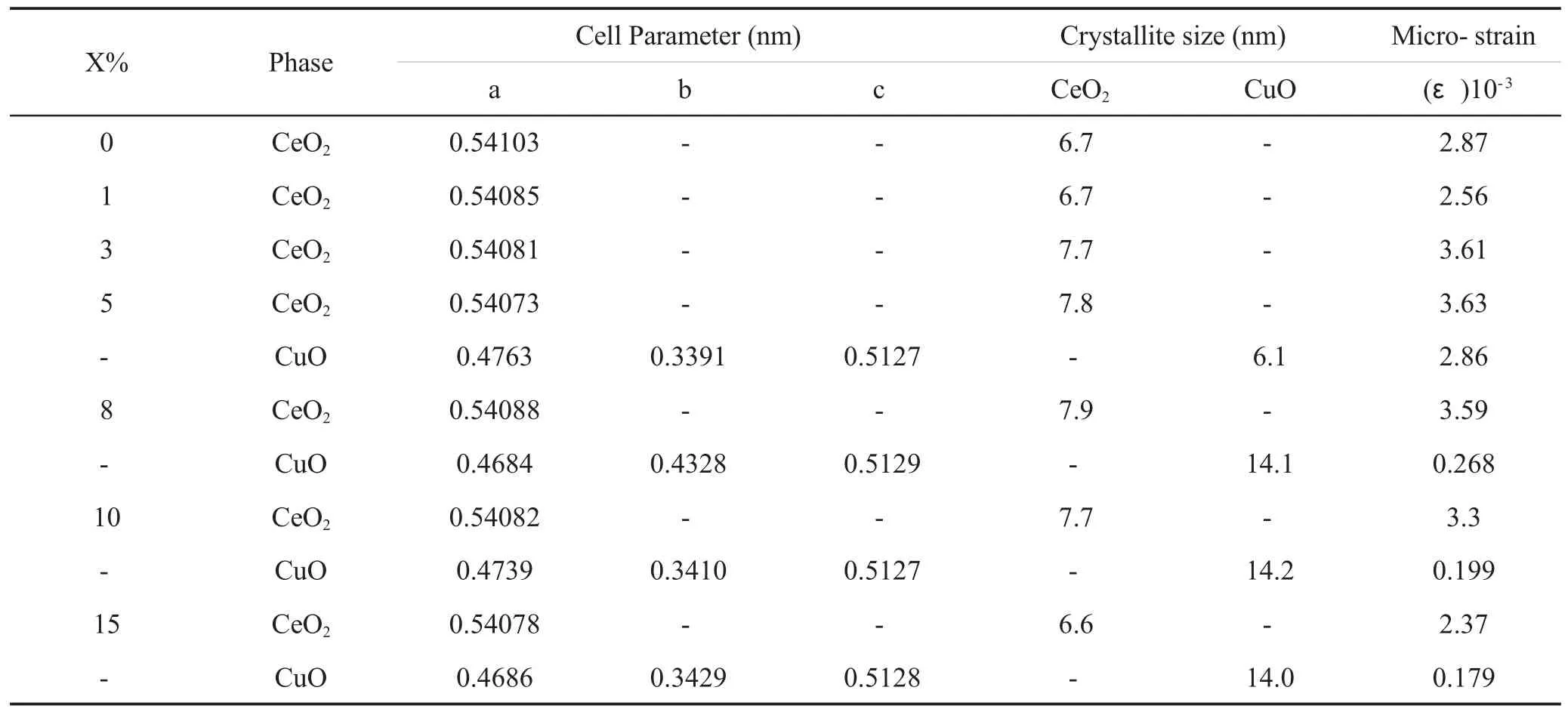
表1 CuO/CeO2催化剂的相关结构参数[14]Tab.1 Structure parameters of CuO/CeO2catalyst[14]

对于CeO2来说,由于其介于离子晶体与共价晶体之间,因此表面结构有其特殊性。在离子晶体中,表面的原子一般会向下位移以尽可能多的与电荷相反离子间相互作用,其中阳离子位移会更大一些(弛豫作用),在此弛豫作用中表面键长会变化较大。从表2中可以发现,弛豫得到了明显的校正,在和时△RB.Ce和△RB.O甚至变为正值,表明此时表面的Ce和O较体相位置还向外凸起,重构也得以减轻,在中这一项甚至减小到接近0。因此可看出,Cu与CeO2作用相当强。通过对吸附能Eads的计算表明,Cu在表面有三种沉积模式,重构减少得最多的最为稳定,为-2. 00eV,其余两个略小,均为-1.69eV,Cu在0)表面的迁移存在各向异性。
Cu的生长过程有如下规律:
(1)由于受到CeO2表面的影响,从构型上看,表面的Cu初始生长过程较规则。在晶格常数不匹配导致的重排之后,则是无方向性的Cu-Cu金属键起主导作用,从而导致Cu的紊乱、凹凸不平直至最后闭合成团簇而没有生长为平坦的Cu层。金属Cu的d电子几乎没有参与成键,即Cu的d电子绝大部分为非键,主要是靠Cu的4s电子把面心Cu晶格维系在一起。CeO2表面的Cu-Cu键长略短。

表2 Cu沉积引起的CeO2表面弛豫和重构Tab.2 CeO2surface relaxation and restructuring caused by Cu deposition
图2表明,每个Cu的沉积会导致总的Eads增加-2到-4eV,随着Cu沉积量的增加,ECu-Cu/Cu会持续增加,并以渐近线的方式逐步趋近于金属Cu中ECu-Cu/Cu的值。ECu/CeO2在达到一个极大值(在后逐步下降。由于Cu的自由价较少,导致后的电子在Cu与CeO2之间Mulliken电荷布居数减少,使得ECu-CeO2降低而ECu-Cu增加。
(3)某些沉积Cu带有正电荷,但一般都明显小于1,介于0价+1价之间。这些Cu可能是反应的活性中心。Cu的4s电子在沉积后部分转移到了附近Ce2+上。此外,由于金属Cu为软碱而易极化,在及其往后,某些沉积的Cu带有负电荷,这可能是由于诱导作用所致。
2.2 Cu在表面的沉积
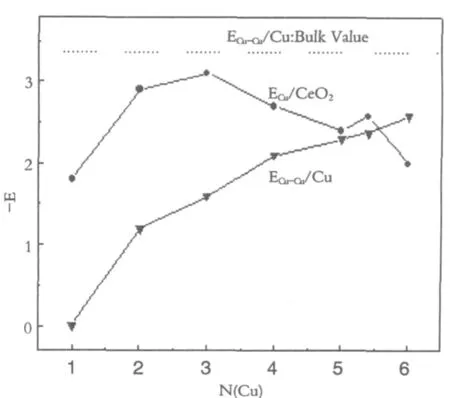
图3 在(112¯0)表面,稳定吸附构型所对应的ECu/CeO2和ECu-Cu/Cu随吸附量的变化曲线Fig.3 Variation of ECu/CeO2and ECu-Cu/Cu on the(112¯0) surface with adsorptive capacity
Cu有两种键合模式,分别称为A(1120(1120))和两者皆处于(1120)表面八面体空穴之中,并与CeO2表面悬挂键成键。其中,大致位于U型槽正中的吸附能为-1.81eV,更为稳定,而位于U型槽一侧的为-1.75Ev。此外,由于表面的单位晶胞已经足够大,单原子沉积时ECu-Cu约为-0.01eV,相当小,有利于Cu与CeO2成键。
(2)在能量方面,Cu与CeO2两个表面的键合能都相当大,并使得CeO2的弛豫和重构得以减轻。沉积Cu之间的作用能(ECu-Cu)与沉积Cu与CeO2载体之间的作用能(ECu-CeO2)存在竞争关系,导致ECu-CeO2在沉积量很小的情况下就已经达到最大值并开始逐步降低。
(3)因为Cu与CeO2之间存在很强的作用,导致沉积的Cu构型与体相有很大的不同,一般情况下其Cu-Cu键都比体相值小至少0.1Å。在同一个吸附量下,有时可能存在多种构型,沉积的Cu可在这些构型间来回迁移,其活化能一般很低,即在工作条件下Cu可能处于不断运动中。
2.3 Cu在CeO2非极性缺陷表面上沉积的密度泛函研究
在CeO2的缺陷表面,Cu的特殊键合模式包括键合于富含电子的Vo处或者凸出于表面的Cei处,也有可能与完整表面很类似。Cu的吸附能一般相当大,超出完整表面的数值,但迁移能仍旧很小。此外,Cu一般显示负价态,因为承接了Vo或者Cei处转移的电子。因此,在缺陷位的Cu可能并非燃料气CO直接的吸附位点。
3 结论
(2)在能量方面,Cu与CeO2两个表面的键合能都相当大,并使得CeO2的弛豫和重构得以减轻。沉积Cu之间的作用能(ECu-Cu)与沉积Cu与CeO2载体之间的作用能(ECu-CeO2)存在竞争关系,导致ECu-CeO2在沉积量很小的情况下就已经达到最大值并开始逐步降低。
(3)因为Cu与CeO2之间存在很强的作用,导致沉积的Cu构型与体相有很大的不同,一般情况下其Cu一键都比体相值小至少0.1Å。在同一个吸附量下,有时可能存在多种构型,沉积的Cu可在这些构型间来回迁移,其活化能一般很低,即在工作条件下Cu可能处于不断运动中。
(5)在CeO2的缺陷表面,Cu的特殊键合模式包括键合于富含电子的Vo处或者凸出于表面的Cei处,也有可能与完整表面很类似。Cu的吸附能一般相当大,超出完整表面的数值,但迁移能仍旧很小。此外,Cu一般显示负价态,因为承接了Vo或者Cei处转移的电子。因此,在缺陷位的Cu可能并非燃料气CO直接的吸附位点。
1 YE X F,WANG S R,WANG Z R,et al.Use of a catalyst layer for anode-supported SOFCs running on ethanol fuel.J.Power Sources,2008,177:419~425
2 PARK S,VOHS J M,GORTE R J.Direct oxidation of hydrocarbons in a solid-oxide fuel cell.Nature,2000,404: 265~267
3 GORTE R J,PARK S,VOHS J M,et al.Anode for direct oxidation of dry hydrocarbons in a solid-oxide fuel cell. Advanced Materials,2000,12:1465~1469
4 GORTE R J,VOHS J M.Novel SOFC anodes for the direct electrochemical oxidation of hydrocarbons. Journal of Catalysis,2003,216:477~486
5 GORTE R J,KIM H,VOHS J M.Novel SOFC anodes for the direct electrochemical oxidation of hydrocarbons,J.Power Sources,2002,106:10~15
6 LIUWei,FLYTZANI-STEPHANOPOULOSM.Totaloxidation of carbon monoxide and methane over transition metal-fluorite oxide composite catalysts.II:Catalyst characterization and reaction kinetics.Journal of Catalysis,1995,153:317~332
7 LUO Linghong,WU Yefan,WEI Fei,et al.Synthesis and characterization of flower-like NiO nano-architectures by homogeneousprecipitation.KeyEngineeringMaterials,accepted
8韦斐,吴也凡,罗凌虹,石纪军,程亮.花状NiO纳米片自组装体的制备与表征.硅酸盐学报,2009,37(12):19~25
9LIU Wei,FLYTZANI-STEPHANOPOULOSM.Total oxidation of carbon monoxide and methane over transition metal-fluorite oxide composite catalysts. I: Catalyst compositionandactivity.JournalofCatalysis,1995,153:304~316
10 DONG L,CHEN Y.Dispersion behaviors of copper oxide on the mixed"CeO2+γ-Al2O3"support.Chem.Mater.,2001,13: 4227
11吴也凡.铁硫立方烷簇合物及聚苯硫醚配合物催化剂仿生配合催化研究.directed by Cai Qirui.Xiamen University,1988
12(a)PAYNE M C,ALLAN D C,ARIAS T A,et al.Rev.Mod. Phys.1992,64:1045.(b)Milman V,Winkler B,White J A,et al.Int.J.Quantum Chem.,2000,77:895
13 SKARMAN B,WALLENBERG L R.Morphology and structure of CuOX/CeO2 nanocomposite catalysts produced by inert gas condensation:an HREM,EFREM,XPS,and high-energy diffraction study.Chem.Mater.,2002,14:3686
14 JIANG X,ZHEN X.Studies of pore structure,temperatureprogrammed reduction performance,and micro-structure of CuO/CeO2catalysts.Appl.Surf.Sci.,2001,173:208
