盐酸氮卓斯汀滴眼液无菌检查方法学验证研究
2011-02-03李旸华张映娜雷柳冰林秋凤
李旸华 张映娜 雷柳冰 林秋凤
盐酸氮卓斯汀滴眼液无菌检查方法学验证研究
李旸华 张映娜 雷柳冰 林秋凤
目的确定可行的盐酸氮卓斯汀滴眼液无菌检查方法。方法 采用薄膜过滤法对样品进行无菌检查。结果样品、阴性对照及试验组菌生长良好。结论薄膜过滤加缓冲液冲洗能去除抑菌作用,并通过验证试验保证无菌检查方法的可靠性。
盐酸氮卓斯汀滴眼液;无菌检查方法;方法验证
盐酸氮卓斯汀为一种新结构的2、3二氮杂萘酮的衍生物,为潜在的长效抗过敏化合物,具有H1受体拮抗剂特点。为确保用药安全,《中国药典》2010版规定所有眼用制剂均要求进行无菌检查。但在《中国药典》2005版只要求微生物限度检查,为确保方法的可行性和结果的准确性,在建立盐酸氮卓斯汀滴眼液无菌检查方法时,进行试验菌的验证,证明所用的方法能有效地去除抑菌活性。适合该滴眼液的无菌检查。
1 仪器与试药及菌种
智能集菌仪(天津罗根科技有限公司)、一次性全封闭集菌器(杭州泰林生物技术设备有限公司)、全自动高压消毒锅(日本三洋);盐酸氮卓斯汀滴眼液由众生药业生产,生产批号为101001、101102、101101.规格:0.05%;菌种均来自中国药品生物制品检验所:金黄色葡萄球菌[CMCC(B)26 003]、铜绿假单胞菌[CMCC(B)10 104]、大肠埃希菌[CMCC(B)10 102]、枯草芽孢杆菌[CMCC(B)63 501]、生孢梭菌[CMCC(B)64 941]、白色念珠菌[CMCC(F)98 001]、黑曲霉[CMCC(F)98 003];培养基均由北京三药科技开发公司生产:营养琼脂培养基、硫乙醇酸盐流体培养、改良马丁琼脂培养基、改良马丁培养基、0.1%的无菌蛋白胨水。聚山梨酯80、氯化钠。
2 方法与结果
2.1 菌液的制备 接种金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌、枯草芽孢杆菌的新鲜培养物至营养琼脂培养基中,30℃ ~35℃培养18~24 h;接种生孢梭菌的新鲜培养物至硫乙醇酸盐流体培养基中,30℃ ~35℃培养18~24 h;接种白色念珠菌的新鲜培养物至改良马丁琼脂培养基中,23℃~28℃培养24~48 h,上述培养物用0.9%无菌氯化钠溶液制成每1 ml含菌数<100cfu(菌落形成单位)的菌悬液。接种黑曲霉的新鲜培养物至改良马丁琼脂斜面培养基上,23℃~28℃培养7 d,加入3~5 ml含0.05%(ml/ml)聚山梨酯80的0.9%无菌氯化钠溶液,将孢子洗脱。然后,吸出孢子悬液(用管口带有薄的无菌棉花或纱布能过滤菌丝的无菌毛细吸管[1])至无菌试管内,用含0.05%(ml/ml)聚山梨酯80的0.9%无菌氯化钠溶液制成每1 ml含孢子数小于100cfu的孢子悬液。备用。具体所用菌液的稀释级及菌落数见表1。
2.2 培养基适用性检查
2.2.1 无菌性检查 取上述硫乙醇酸盐流体培养基、改良马丁培养基各制备成灭菌溶液,在相应条件下培养14 d,结果为无菌生长。
2.2.2 灵敏度检查 取每管装量为12 mI 的硫乙醇酸盐流体培养基9支,分别接种<100cfu的金黄色葡萄球菌、铜绿假单孢菌、枯草芽孢杆菌、生孢梭菌各2支,另1支不接种作为空白对照,培养3 d;取每管装量为9 mI的改良马丁培养基5支,分别接种<100cfu的白色念珠菌、黑曲霉各2支,另1支不接种作为空白对照,培养5 d,逐日观察结果。结果:空白对照管无菌生长,加菌的培养基管均生长良好,灵敏度检查符合规定[2]见表 2。
2.3 方法的选择及方法验证试验
2.3.1 直接薄膜过滤法 将供试品5瓶按薄膜过滤法过滤(每种试验菌的样品量)后。采用薄膜过滤法过滤,接种硫乙醇酸盐流体培养基或改良马丁培养基,同时加入小于100cfu的试验菌。另取一装有同体积相同培养基的容器,加入等量试验菌,作为对照,按规定温度培养3~5 d。各试验菌同法操作,并分别做阴性对照80 ml。结果见表3。
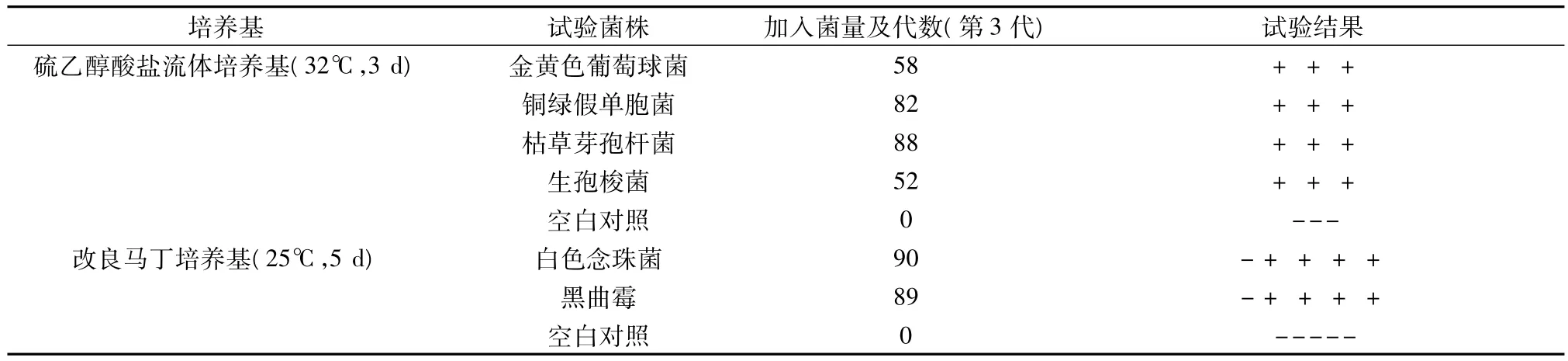
表2 培养基灵敏度检查

表3 溶解后直接过滤的试验结果
从上表可知,供试品对金黄色葡萄球菌、生孢梭菌有抑菌作用,所以不能用直接薄膜过滤法。
2.3.2 薄膜过滤法加冲洗 将供试品5瓶采用薄膜过滤法过滤(每种试验菌的样品量)后,用0.1%蛋白胨水150 ml分3次冲洗,接种硫乙醇酸盐流体培养基或改良马丁培养基,同时加入小于100cfu的试验菌。另取一装有同体积相同培养基的容器,加入等量试验菌,作为对照,按规定温度培养3~5 d。结果见表4。

表4 薄膜过滤法加冲洗试验结果
2.3.3 结论 表2显示,试验组与阳性对照组中试验菌细菌均在1 d内生长良好,试验菌真菌均在3 d内生长良好符合验证要求,则本品采用以下方法进行无菌检查:取供试品15瓶,消毒瓶外壁后,采用薄膜过滤法(一次性全封闭),集菌器,三筒/联)过滤后,用0.1%蛋白胨水450 ml分三次冲洗,每次150 ml,于两筒中加入硫乙醇酸盐流体培养基,一筒加入改良马丁培养基,以金黄色葡萄球菌为阳性菌,按规定温度培养14 d,逐日观察结果。
3 讨论
3.1 实验先将过滤前用冲洗液湿润滤膜,可减少冲洗量。
3.2 样品组及空白对照组的设置,目的在于保证实验在样品、溶剂、冲洗液、培养基及相关实验器材均为无菌的情况下进行,避免上述因素对实验结果造成干扰[3]。
3.3 盐酸氮卓斯汀对金黄色葡萄球菌和生孢梭菌有抑制作用,特别是金黄色葡萄球菌,验证实验表明,采用薄膜过滤法,冲洗量为450 ml,此法简单有效方便可行。
[1] 中国药品检验标准操作规范.2005年版.北京:国医药科技出版社,2005:313-32
[2] 国家药典委员会.《中国药典》2010年版.二部.北京:化学工业出版社,2010:附录103-107.
[3] 苏德膜,马旭荣.药品微生物学检验技术.北京:华龄出版社,2007:1.
Studies on test for sterility of azelastine hydrochloride eye drops
LI Yang-hua,ZHANG Ying-na,LEI Luibing,et al.Institute for Food And Drug Control of Dongguan,GuangDong,523109,China
ObjectiveTo establish a method for slerility test of azelastine hydrochloride eye drops.MethodsUsing membrane filtration method for sterility test of samples.ResultsThe samples,negative control samples and the growth of good bacteria.ConclusionAdd buffer to wash the membrane filter to remove the inhibitory effect,and through verification tests to ensure the reliability of sterility test method.
Azelastine hydrochloride eye drops;sterility test method;method validation
523109东莞市食品药品检验所
