Nafion膜修饰电极的制备及其通透性研究*
2011-01-22时克林王晓蕾
时克林 王晓蕾
(山东省淄博第六中学化学组,淄博 255300) (山东师范大学化学化工与材料科学学院,济南 250014)
化学修饰电极是当前电化学和电分析化学领域的一个热门研究课题[1],它通过共价、键合、吸附、聚合等手段,将具有功能性的物质引入电极表面,制得具有新的、特定功能的电极[2]。化学修饰电极由于其制备简单、灵敏度高、选择性良好和响应迅速等优点在伏安法中应用广泛[3]。膜化学修饰电极是通过滴涂、旋涂、电沉积、化学沉积、等离子聚合、电聚合等方法在电极表面制备修饰薄膜而制得的电极,借助Faraday(电荷消耗)反应可呈现修饰薄膜化学、电化学以及光学的性质。这种人为设计和制作的电极展示出独特的光电催化、电色、表面配合、富集和分离、开关和整流、分子识别、掺杂和释放等功效和功能。研究和制备这种修饰电极表面膜的微结构和其界面反应,大大地推动了电极过程动力学理论的发展,并作为化学和相关边缘学科开拓了广阔研究领域[4,5]。
Nafion是一种性质稳定、具有离子交换作用的含氟化合物,其结构式如下:
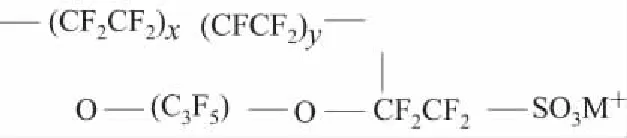
Nafion聚合物具有导电性好,对热和化学物质稳定、阻抗小、水中溶解度小等特性,是一种良好的电极修饰材料[6]。Nafion是一种优良的阳离子交换剂,用作电极修饰材料具有良好的离子选择性,它只与阳离子发生选择性交换,排斥中性分子和阴离子[2]。Nafion膜本身含有磺酸基团,Grieke在1981年提出了膜的离子簇多孔网状结构及关于离子传递的渗透理论,其孔大约为5 nm。它是由于水合作用,磺酸基团的静电力与氟碳骨架弹力平衡作用的结果。这些离子簇形成的多孔状结构,由1 nm的通道相连,提供阳离子传输的通道,并且Nafion膜具有化学惰性、耐腐蚀性,这些优点使Nafion膜有可能成为寿命长的离子选择性电极。Nafion膜广泛应用于化学修饰电极以增加修饰电极对阳离子的选择性[7]。全氟磺酸质子交换膜由于其具有优良的机械、物理、化学及电化学稳定性,广泛用于燃料电池、电解水以及其它电化学领域[8]。Nafion膜修饰电极对表面活性物质具有良好的抗干扰能力,因此伏安法中应用Nafion修饰电极可以提高分析灵敏度和抗干扰能力[6]。已有文献报道以Nafion膜修饰电极测定微量元素能提高分析的灵敏度和抗干扰能力[9]。Nafion膜修饰电极已被应用于越来越多的化学修饰电极和生物传感器的研制中[10,11],以提高测定的选择性,但对带不同电荷的物质其作用的差异研究很少。
笔者在前人研究的基础上,制备了Nafion膜修饰玻碳电极,通过测定Nafion膜对电活性物质铁氰化钾、抗坏血酸、多巴胺等在电极表面反应的阻碍程度,进一步研究了Nafion膜对几种电活性物质的阻碍作用,以及成膜方式和膜的厚度对阻碍作用的影响,对进一步推广Nafion膜修饰电极在电化学中的应用具有指导意义。
1 实验部分
1.1 主要仪器与试剂
微机电化学分析系统:LK98A型,天津兰力科化学电子有限公司;
三电极系统:Nafion膜修饰(或裸)玻碳电极作工作电极,饱和甘汞电极作参比电极,铂丝作对电极,测量均在室温下进行;
数控超声清洗器:KQ-1000E型,昆山市超声仪器有限公司;
磁力搅拌器:CLJ-2000型,天津兰力科化学电子有限公司;
分析天平:FA1104型,上海精密科科学仪器有限公司 ;
抗坏血酸(AA):分析纯,天津化学试剂一厂;
多巴胺(DA):分析纯,中国药品生物制品检验所;
无水乙酸钠、无水乙醇、Na2HPO4·12H2O、氯化钾:分析纯,国药集团化学试剂有限公司;
NaH2PO4·2H2O:分析纯,中国医药集团上海化学试剂公司;
冰乙酸:分析纯,无锡市龙吉利化工试剂有限公司;
铁氰化钾:分析纯,西安化学试剂厂;
Al2O3抛光粉:JP-3型,云南光电辅料有限公司;
Nafion溶液:将质量分数为5%的Nafion溶液(Fluka)溶于异丙醇-水(体积比1∶1),配成质量分数分别为0.5%、2%、3%、5%的Nafion溶液。
1.2 Nafion膜修饰电极的制备
Nafion膜修饰电极采用溶剂挥发法制备。依次用1 μm和0.05 μm Al2O3抛光粉将玻碳电极抛成镜面,用二次水清洗,然后分别用无水乙醇和二次水超声清洗5 min,最后用二次蒸馏水将电极表面冲洗干净,于室温下自然晾干。滴涂时,用微量加样器慢慢滴加2 μL Nafion溶液(质量分别为0.5%、2%、3%、5%)于玻碳电极表面,室温下挥发掉溶剂,即得所需修饰电极。若为蘸涂,将电极表面端竖直插入Nafion异丙醇溶液,然后取出直立,晾干。为了清除电极的记忆效应,每次测完一个数据后,重新处理电极。
1.3 循环伏安扫描
将30 mL含电活性物质的溶液加入到电解池中,插入三电极体系,以100 mV/s的扫描速度,在合适的电位范围内进行循环伏安扫描,记录其循环伏安曲线。
2 结果与讨论
2.1 Nafion膜成膜方式的影响
试验了浓度为5×10-3mol/L铁氰化钾(含1 mol/L氯化钾作支持电解质)分别在裸电极、滴涂2 μL 0.5%Nafion溶液和蘸涂1次0.5 %Nafion溶液膜修饰电极表面的电化学行为,如图1所示。Nafion溶液浓度:0.5%;滴涂量:2 μL;蘸涂次数:1次;底液:1 mol/L氯化钾;扫描速度:100 mV/s;
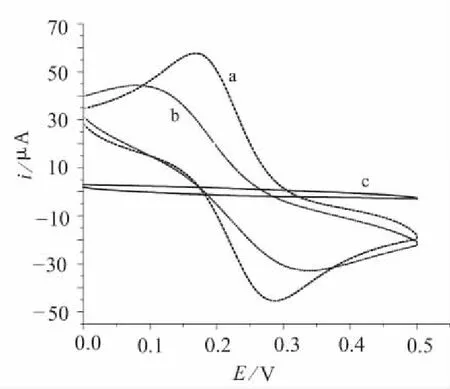
a—裸电极; b—蘸涂Nafion溶液; c—滴涂Nafion溶液
从图1看出,与裸电极明显的氧化还原峰电流(曲线a)相比,蘸涂形成的膜修饰电极在铁氰化钾中的峰电流被削弱了,但仍有一对小的氧化还原峰(曲线b);滴涂形成的膜修饰电极在铁氰化钾中已完全没有峰电流(曲线c)。峰电流小说明透过膜参与反应的铁氰化钾少,也就是受到了膜较大的阻碍。由此可见:无论是滴涂还是蘸涂成膜,都能阻碍铁氰化钾向电极表面的传质;而滴涂的阻碍效果好于蘸涂。原因是滴涂形成的膜比较致密,能有效阻碍透过,而蘸涂形成的膜较薄,只能部分阻碍。因此在制备Nafion膜修饰电极时,采用滴涂的方法。
2.2 膜厚度的影响
试验了1×10-3mol/L AA在裸电极,滴涂2 μL 2% Nafion溶液和滴涂2 μL 3% Nafion溶液形成的Nafion膜修饰电极表面的电化学行为,如图2所示。底液:pH 4.0的乙酸盐缓冲溶液;扫描速度:100 mV/s。
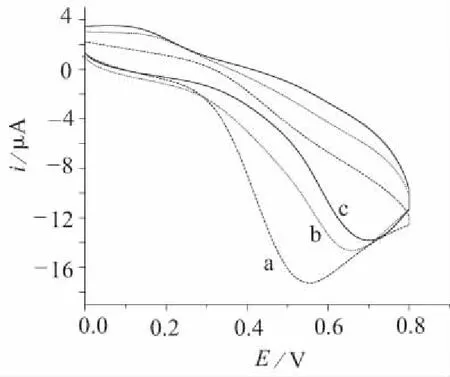
a—裸电极; b—滴涂2%Nafion溶液; c—滴涂3%Nafion溶液
图2 AA在裸电及Nafion膜修饰电极表面的循环伏安图
从图2可以看出:从裸电极到滴涂成膜的修饰电极,在1×10-3mol/L AA中均出现了峰电流,不同的是,随着滴加的Nafion溶液浓度加大,形成的Nafion膜越厚,峰电流越小,峰电位正移。因此,Nafion膜阻碍AA在电极表面的传质和反应,膜越厚,阻碍效果越明显。
2.3 铁氰化钾在Nafion膜修饰电极表面的响应
试验了5×10-3mol/L铁氰化钾(含1 mol/L氯化钾作支持电解质)在裸电极和滴涂2 μL 0.5% Nafion溶液形成的膜修饰电极表面的电化学行为,如图3所示。底液:1 mol/L氯化钾;扫描速度:100 mV/s。
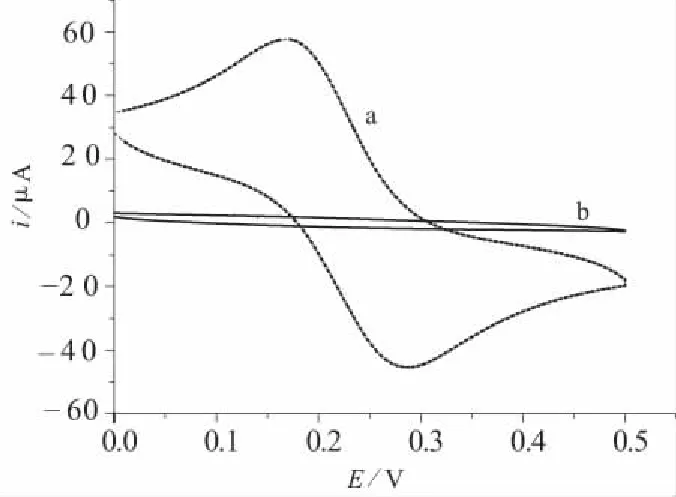
a—裸电极; b—滴涂Nafion溶液
2.4 AA在Nafion膜修饰电极表面的响应
试验了1×10-3mol/L AA在裸电极、滴涂2 μL 2% Nafion溶液、滴涂2 μL 3% Nafion溶液、滴涂2 μL 5%Nafion溶液膜修饰电极表面的电化学行为,如图4所示。底液:pH 4.0的乙酸盐缓冲溶液;扫描速度:100 mV/s。
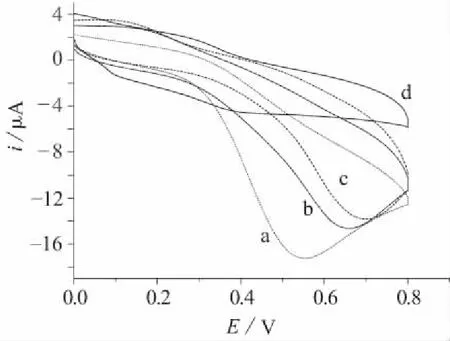
a—裸电极; b—滴涂2%Nafion溶液; c—滴涂3%Nafion溶液; d—5%Nafion溶液
从图4看出:AA在裸电极表面响应有明显的氧化峰(曲线a),而且峰型很好;滴涂2%Nafion溶液和滴涂3%Nafion溶液形成修饰电极后,明显削弱了峰电流,且峰电位明显正移(曲线b,曲线c),但氧化峰依然存在;而滴涂5%Nafion溶液电极已完全没有AA的氧化峰了(曲线d)。由此可知:滴涂低浓度Nafion溶液形成的膜只能部分阻碍AA在电极表面的反应,滴涂5%Nafion溶液形成的膜能较好地阻碍AA在电极表面的传质和反应。与铁氰化钾相比,AA所带负电荷较少,因此Nafion对AA的阻碍较小。
2.5 DA在Nafion膜修饰电极表面的响应
试验了1×10-4mol/L DA在裸电极、滴涂2 μL 2%Nafion溶液、滴涂2 μL 3%Nafion溶液、滴涂2 μL 5%Nafion溶液形成的膜修饰电极表面的电化学行为,如图5所示。底液:pH 7.6的磷酸盐缓冲溶液;扫描速度:100 mV/s。

a—裸电极; b—滴涂2%Nafion溶液;c—滴涂5%Nafion; d—滴涂3%Nafion溶液
图5 DA在裸电极及不同浓度Nafion溶液膜修饰电极表面的循环伏安图
从图5看出:DA在裸电极表面有较大氧化还原峰,而且峰形好(曲线a),滴涂2 μL 2%Nafion溶液形成膜修饰电极后,峰电流有所增大(曲线b),氧化峰电位稍负移,还原峰电位稍正移,而在滴涂2 μL 3%Nafion溶液后,电流明显减小(曲线c),滴涂2 μL 5%Nafion溶液后降至更小(曲线d)。其原因可能是DA在中性缓冲溶液中带正电荷,因此Nafion膜对DA有吸附和阻碍的双重作用。滴涂低浓度Nafion溶液,阻碍作用弱,而吸附作用占主导,会使峰电流增大;而滴涂较高浓度Nafion溶液,由于膜厚度大,阻碍作用占主导,只有少量DA能透过Nafion膜在电极表面反应,因此峰电流减小。
3 结语
Nafion膜对带有负电荷的物质有明显的排斥作用,而且随着负电荷数的增加,排斥作用增加;对带有正电荷的物质有一定的吸附富集作用,但随着Nafion膜厚度的增加,阻碍作用占主导。该研究对实验中Nafion膜的选择和使用有一定指导意义。
[1] 董绍俊.化学修饰电极在分析化学中的应用[J]. 分析化学, 1988,16(10):951-960.
[2] 向翠丽. Nafion膜修饰电极的研究与应用[D]. 华中师范大学, 2006.
[3] 杨春海,黄明泉,黄文胜,等. Nafion修饰玻碳电极伏安法测定痕量氧氟沙星的研究[J].湖北民族学院学报(自然科学版), 2002,20(4):43-46.
[4] 董绍俊,车广礼,谢远武.化学修饰电极[M].北京:科学出版社, 1995.
[5] Davis J J, Coles R J, Hill A O. Protein electrochemistry at carbon nanotube electrodes[J]. J Electroanal Chem, 1997, 440: 279-282.
[6] 金利通,崔胜云,史占玲,等. Nafion修饰电极在伏安分析中的应用[J].冶金分析, 1990,10(5):38-42.
[7] 曾蓉,黄文迎,庞志诚,等.全氟磺酸膜的离子选择性[J].分析化学, 1999,27(8):965-968.
[8] 徐麟,徐洪峰,李海燕.再铸Nafion膜的制备和性能分析[J].膜科学与技术, 2005,25(1):4-8.
[9] 朱松磊,王静,刘永民. Nafion膜修饰电极测定血清中的微量元素[J].徐州医学院学报, 1999,19(4):270-271.
[10] 梁汝萍,邱建丁,邹小勇,等.基于Nafion-L-赖氨酸-溶胶-凝胶膜的电催化型DA传感器[J].应用化学, 2003,20(4):346-349.
[11] 王明艳,许兴友,高键,等.新型双核铜配合物修饰玻碳电极对AA的电催化作用及其测定[J].理化检验:化学分册, 2006,42(12):983-993.
[12] 刘凤兰,刘艳. Nafion膜修饰电极在分析化学中的应用[J].中国卫生检验杂志, 1998,8(1):52-54.
