* 3-羟基溴代吲哚衍生物的合成研究
2011-01-11王国峰冯丽恒郭炜
王国峰,冯丽恒,郭炜
(山西大学化学化工学院,山西太原 030006)
*3-羟基溴代吲哚衍生物的合成研究
王国峰,冯丽恒,郭炜
(山西大学化学化工学院,山西太原 030006)
通过多步合成得到4个具有潜在抗肿瘤活性及解热镇痛、阻胺作用的吲哚类医药化合物.并通过 IR、1H NMR、M S和元素分析对化合物结构进行了表征.
溴代吲哚;药物中间体;药物合成
吲哚及其衍生物是重要的精细化工原料和化工产品,在工业、农业及医药等领域中有着十分广泛的重要用途,对其研究一直经久不衰,新的应用领域在不断地被开发出来[1-3].
在众多的吲哚衍生物中,3-羟基吲哚衍生物以其独有的化学结构,使其具有独特的生理抗癌活性和阻胺镇痛的作用[4].目前,虽然已得到许多3-羟基吲哚衍生物,而对于日益发展的吲哚医药领域来说是远远不够的,因而合成出空间结构不同且多个功能团纳入同一个吲哚分子中新型吲哚类化合物是势在必行的[5-7].为此,本研究工作设计并合成得到4个3-羟基溴代吲哚衍生物,所采用的合成路线具有原料易得、价格便宜、操作简便、收率高等特点.
1 实验部分
1.1 试剂与仪器
4-溴吲哚、5-溴吲哚、6-溴吲哚及7-溴吲哚(分析纯,上海西域有限公司);二碳酸二叔丁酯 [(BOC)2O],4-二甲氨基吡啶(DMAP)(分析纯,北京中远恒业化工有限公司);其它常用试剂和药品均为分析纯.
FTIR-8300红外光谱仪;Bruker ARX400超导核磁共振仪 (TM S内标);JEOL GC-M SD 300型质谱仪(以ESI为离子源,电离能为70 eV);Vario EL元素分析仪.
1.2 合成
1.2.1 合成路线

图1 目标化合物的合成路线Fig.1 Synthetic routes of the title compound
1.2.2 合成步骤
3-碘-4-溴吲哚的合成[8]
在装有电动搅拌器的500 mL三口瓶中,加入50 mL DM SO,10 g(0.051 mol)4-溴吲哚,7.15 g(0.127 mol)氢氧化钾,室温下搅拌反应30 min后,将溶有13 g(0.051 mol)碘单质的150~200 m L DM SO滴入上述体系中.室温搅拌反应2 h.TLC检测(展开剂乙酸乙酯/石油醚=1/5,V/V)反应.反应完成后,在快速搅拌下,将反应液倒入600 mL水中,析出沉淀,过滤所得固体为土黄色,干燥后得产品,产率96%.
3-乙酰基-4-溴吲哚的合成
在装有机械搅拌器和水浴的500 mL三口瓶中,加入150 mL冰醋酸,通氮气10 min后,向反应瓶中加入16.43 g(0.051 mol)3-碘-4-溴吲哚,14.3 g(0.076 mol)醋酸银.升温至90 ℃,回流2 h后,用 TLC检测反应,待反应结束后,冷却至室温,过滤除去碘化银,用四氢呋喃洗涤沉淀,将所得的滤液倒入大量的冰水中,过滤,所得固体是红棕色.干燥后,柱色谱分离(展开剂:乙酸乙酯/石油醚=1/15,V/V),产率50%.
N-BOC-3-乙酰基-4-溴吲哚的合成
在装有电动搅拌器的250 m L三口瓶中,加入80 m L二氯甲烷,4 g(0.016 mol)3-乙酰基-4-溴吲哚,4.12 g(0.019 mol)(BOC)2O,催化量的DMAP(5%mol),加热回流1 h,用 TLC检测(展开剂:乙酸乙酯/石油醚=1/7,V/V)反应.反应完毕,减压旋除二氯甲烷后,用200 m L乙醚溶解,饱和碳酸氢钠溶液200 m L洗涤3次后,用饱和氯化钠水溶液200 m L洗涤两次.然后旋除乙醚,拌硅胶,柱色谱分离(展开剂:乙酸乙酯/石油醚=1/10,V/V),产率95%.
N-BOC-3-羟基-4-溴吲哚的合成[9]
在氮气保护下,向装有机械搅拌器和水浴的250 m L的三口瓶中,加入50 m L乙醇,5 g(0.014 mol)NBOC-3-乙酰基-4-溴吲哚,加热回流.然后在回流状态下,将3.56 g(0.028 mol)亚硫酸钠溶解在100 m L热水中,通过恒压滴液漏斗滴加到上述溶液中,溶液颜色逐渐变为浅黄色.继续搅拌回流5 h,经TLC检测反应结束后.减压旋除大量乙醇,用乙醚200 m L乙醚萃取三次,合并乙醚,经饱和氯化钠溶液洗涤后,无水硫酸钠干燥,旋除乙醚,得粗品.柱色谱分离得白色固体(展开剂:乙酸乙酯/石油醚=1/10,V/V),产率64.8%.
N-BOC-3-羟基-5-溴吲哚,N-BOC-3-羟基-6-溴吲哚,N-BOC-3-羟基-7-溴吲哚的合成全部按照上述方法得到.目标化合物的结构表征如表1所示.
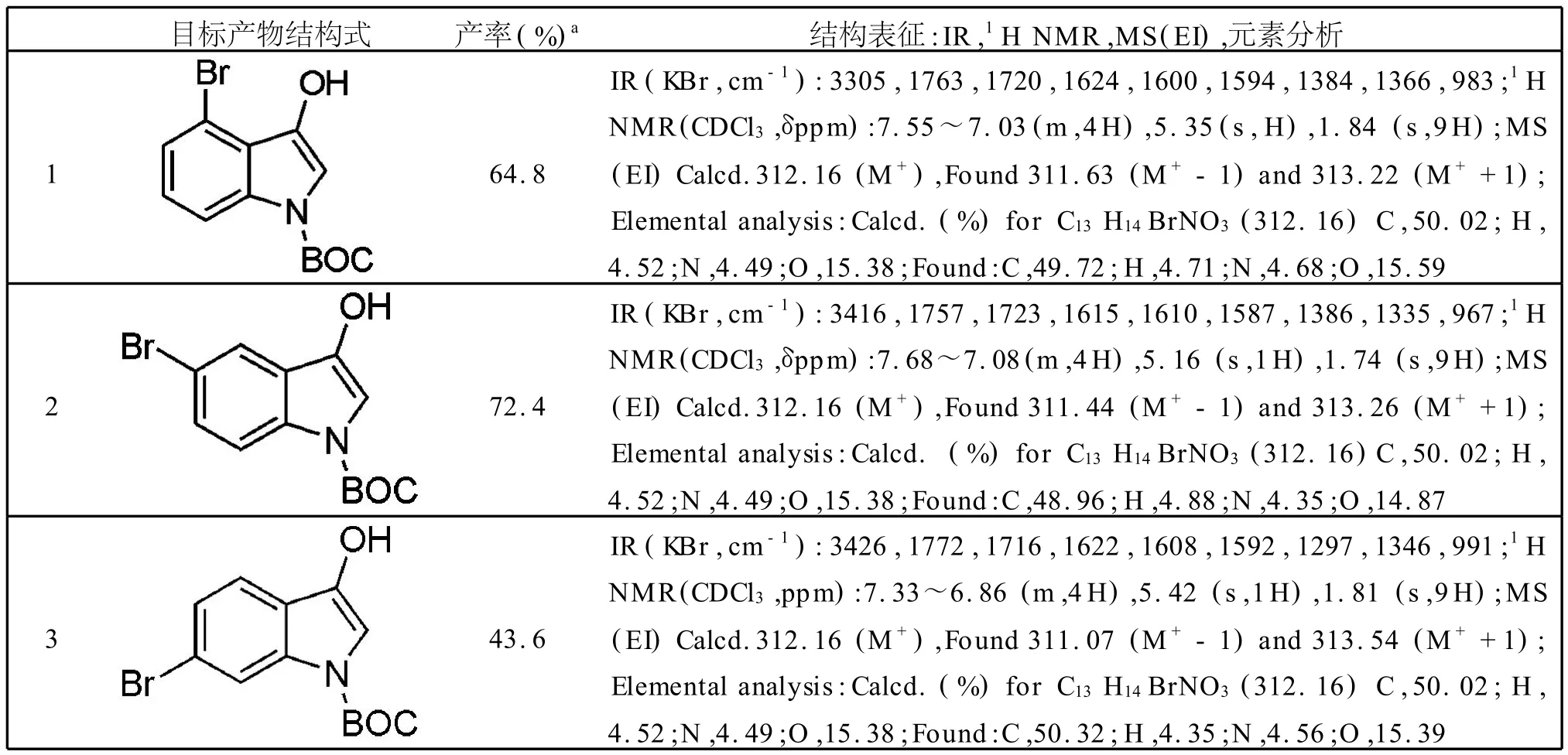
表1 目标化合物的结构表征Table 1 Structure of the title com pounds

续表1 目标化合物的结构表征Continue Table 1 Structure of the title compounds
2 结果与讨论
2.1 碘化反应
合成路线第一步反应为典型的芳香环取代反应,碘单质作为取代基在碱性条件下进行反应.一般选用溶解性优良溶剂,如DM SO、DM F、THF等.研究结果表明:DM SO>DM F>THF,在DM SO中反应的产率都大于95%.但该反应的产物不稳定,需要干燥后立即投入下一步反应.
2.2 乙酰化反应
研究合成路线,该步为取代反应,选用碘作为很好的离去基团,乙酰基作为取代基,反应生成碘化银沉淀,从溶液中析出,促进反应向正方向进行,提高产率.然而在反应中,这步反应得到的产物产率较低,而且不好分离,这可能由于原料不稳定以及柱色谱分离时硅胶吸附产品,难以洗脱下来.
2.3 脱酰基变羟基
该步是碱性条件下的水解反应,合成路线先用Boc保护来阻止吲哚烯醇式和酮式的相互转化,再在氮气保护下,防止生成的产物被氧化,避免聚合生成不溶于任何溶剂的吲哚高聚物.
3 结论
通过多步反应得到了4个鲜见文献报道的3-羟基-溴代吲哚衍生物,该合成路线选用碘作为好的亲核基团和离去基团,并通过生产碘化银沉淀,从有机相中分离出来,不仅提高反应产率,而且简化了处理方法.利用Boc保护来阻止吲哚烯醇式和酮式的相互转化,削弱吲哚2位的反应活性,减少副产物的生产.总之,本文所提供的合成路线具有原料易得、操作简单、收率高及对环境污染小等特点,为进行工业化中试生产提供可靠的理论和实验依据.下一步将对所得化合物进行抗肿瘤活性的研究.
[1] Wang Y,Gloer J B,Scottj A,et al.TerezinesA-D:New Amino Acid-derived Bioactive Metabolites from Thecoprophilous Fungus Sporormiella-teretispora[J].Journal of Natural Products,1995,58(1):93-99.
[2] Nettleton D E,Doyle T W,Kr Shnan B,et al.Isolation and Structure of Rebeccamycin:A New Antitumor Antibio tic from No Cardia Aerocoligenes[J].Tetrahedron Letters,1985,26(34):4011-4014.
[3] Chung B C,Alexander,Wolfram L J.Process for Colo ring Keratinaceous Materials with materials with Compositions Containing an Azidoindole or Aromatic Azide[P].US 4695285,1987.
[4] Meng Q C,Slassi A,Rakhit S.Preparation of Thiophene and FuranSub stituted FuranSub stituted Furan Substituted Tryptamine Analogs for Use as 5-HTID Receptor Agonists[P].WO 9743281,1997.
[5] Feng T,Li Y,Wang Y Y,Cai X H,Liu Y P,Luo X D.Cytotoxic Indole Alkaloids from Melodinus Tenuicaudatus[J].J N at Prod,2010,73(6):075-1079.
[6] Shi Z Z,Cui Y X,Jiao N.Synthesis of β-andγ-Carbolinones via Pd-Catalyzed Direct Dehydrogenative Annulation(DDA)of Indole-carboxamides with Alkynes Using Air as the Oxidant[J].Org Lett,2010,12(13):2908-2911.
[7] Yang J,Song H,Xiao X,et al.Biomimetic Approach to Perophoramidine and Communesin via an Intromolecular Cyclopanation Reaction[J].Org Lett,2006,8(10):2187-2190.
[8] Tatsuo I,Miki M,Norio M.Palladium(0)-Catalyzed Cross-Coupling Reaction of Alkoxydiboron with Haloarenes:A Direct Procedure for Arylboronic Esters[J].J Org Chem,1995,60(23):7508-7510.
[9] Ravi V,Sreelatha N,Srinivas R A.Molecular Iodine-Catalyzed Facile Procedure for N-Boc Protection of Amines[J].JOrg Chem,2006,71(21):8283-8286.
Syn thesis of 3-Hydroxyl-bromo Indoles Derivatives
WANG Guo-feng,FENG Li-heng,GUO Wei
(School of Chemistry and Chemical Engineering,Shanxi University,Taiyuan030006,China)
Indole and it’s derivates,being one of the important fine chemical p roducts,p lay important role in industry and medicine areas.Four 3-hydroxyl-bromo indole derivatives which used to antitumor activite,an-tipyretic analgesics and hindered amine were synthesized through many step s.These compounds were characterized by IR,1H NMR,MS and elemental analysis.
bromination indoles;drug intermediates;pharmaceutical synthesis
O625
A
0253-2395(2011)01-0106-04*
2010-07-10;
2010-09-15
国家自然科学基金 (20772073;20802042)
王国峰(1985-),男,山西运城人,硕士研究生,从事有机功能分子合成研究工作.
