CPA矩阵—催化动力学光度法同时测定镍和铁混合双组分的分析方法研究*
2011-01-10姬泓巍张菲菲辛惠蓁曹恒霞
姬泓巍,张菲菲,辛惠蓁,曹恒霞,李 双
(中国海洋大学化学化工学院,海洋化学理论与工程技术教育重点实验室,山东青岛266100)
铁和镍都是人和生物体新陈代谢必需的微量元素,但如果机体吸收过量的铁和镍就会导致诸多严重的病变。因此,了解水体中铁(Ⅲ)和镍(Ⅱ)的含量和分布的研究是非常有意义的。对于单组份的铁和镍,现有的分析方法主要有火焰原子吸收光谱法、荧光光度法、可见分光光度法、电感耦合等离子体发射光谱法、催化动力学分光光度法等[1-12]。催化动力学光度法[9-11]是在普通分光光度法的基础上新发展起来的一种分析方法,由于具有灵敏度高、检出限低、仪器价廉、操作简单等优点,现已被广泛应用于痕量金属的测定中。
对于多组分混合体系,可利用化学计量学方法对其实现同时分析测定。其中多元线性回归法中的反推最小二乘法,因具有对相互重叠的多组分光谱有较强的解析能力,而受到普遍重视。由于目前有关水体中铁(Ⅲ)和镍(Ⅱ)的同时测定的研究尚未见报道,因此,本文拟在已成功建立单组分铁(Ⅲ)和镍(Ⅱ)的催化动力学光度法测定方法的基础上[9-10],再进一步把催化动力学光度法与化学计量学方法相结合,从而建立起能对水体中痕量镍和铁的混合体系同时测定的分析方法,并使之能应用到实际水体系中铁(Ⅲ)和镍(Ⅱ)的测定。
1 CPA矩阵—催化动力学光度法的分析方法原理
本论文所研究的反应体系是铁(Ⅲ)-镍(Ⅱ)-高碘酸钾-弱酸艳蓝(RAWL)-1,10-菲啰啉体系,分析原理是基于铁(Ⅲ)和镍(Ⅱ)对高碘酸钾氧化弱酸艳蓝(RAWL)的褪色反应均具有催化作用,1,10-菲啰啉对铁(Ⅲ)的催化反应有活化作用。
在酸性介质中,铁(Ⅲ)和镍(Ⅱ)催化高碘酸钾氧化弱酸艳蓝(RAWL)的褪色反应可表示为:

CPA矩阵法又称反推最小二乘法,当应用于分光光度法时,它将相应量吸光度与浓度之间的关系表示成朗伯-比尔定律的反形式,即将浓度表示为吸光度的函数。对于已知校正溶液的测量波谱矩阵A及其浓度组成矩阵C,有朗伯-比尔定律的反推表达式:
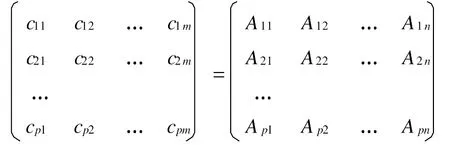
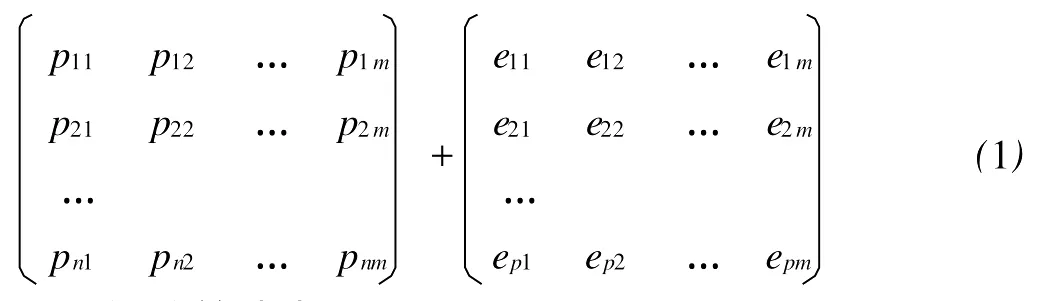
矩阵简式为:
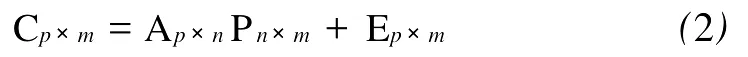
式(2)中P为n×m阶矩阵,其每一列包含有n个对应于某组分的权重系数。其它矩阵表示的内容与P矩阵的反推表达式相同。
采用最小二乘法,可得矩阵P的估计值:
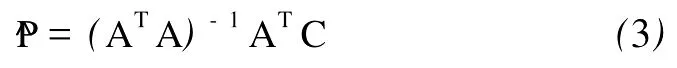
只有在校正组吸光度矩阵A满秩的情况下,才能对(AT)(n×n)进行求逆。因此只有当标准校正溶液的数目大于或等于选用的波长数时,p≥n,方程(3)才能进行计算。因此反推最小二乘法不是一种全波谱校正方法,它对波长数有较严格的限制。在采用该方法时,应选择相对“较好”的波长(通常可选择各组分的吸收峰波长,各组分吸光度之间相差较大且强度相对较大的波长,以及其他一些测量误差较小,但又含有一定信息量的波长。)。
反推最小二乘法的优点是不需知道可能存在组分的全部信息,包括待测组分和干扰组分。对于矩阵C仅需知道待测组分所对应的那一列。因此,反推最小二乘法可用于有化学干扰物存在时对待测物质进行的分析。
现有一未知溶液样品,其吸光度波谱向量为anew,则可直接求得其浓度:

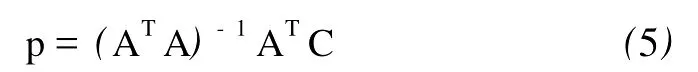
与式(3)相比较,式(5)的P矩阵已退化为一个p向量,利用该p向量对未知溶液进行浓度预报时有:

这时cnew为未知溶液中对应于p的某一组分浓度,仅为一数量而已[13]。
对于单一催化组分体系,催化褪色光度法的定量关系式为:

△A为非催化体系和催化体系的吸光度差值,c为催化组分的浓度,K为响应灵敏度。
对于有s个组分的体系,设有m个试样,在n个不同的实验条件(作为量测通道)下,得到的吸光度响应矩阵为△Anm=KnsCsm。考虑到偏离Beer定律,加入截距校正,响应矩阵△A可取为(n+1)m阶,这时灵敏度矩阵也应为(n+1)s阶。欲测灵敏度矩阵K,可在n个测量条件下,利用已知标准溶液(浓度矩阵C标sm)测得响应矩阵,求得K的广义逆阵P:
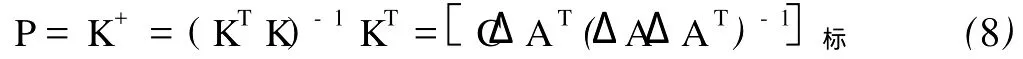
则:c样=PΔA样,据此可对待测样品进行测定[14]。
2 仪器和试剂
2.1 主要仪器
紫外-可见分光光度仪(美国惠普公司),电子分析天平(北京赛多利斯仪器系统有限公司),精密酸度计(上海精密科学仪器有限公司),电热鼓风干燥箱(淄博仪表厂),自动双重纯水蒸馏器(上海亚荣生化仪器厂),M illi-Q超纯水仪(密理博中国有限公司),恒温水浴锅(国盛实验厂),秒表(上海秒表厂)。
2.2 主要试剂
高碘酸钾(分析纯,上海试剂厂),弱酸艳蓝(青岛双桃染料厂),盐酸(分析纯,烟台三和化学试剂有限公司),硝酸(分析纯,崇明前进实业总公司),1,10-菲啰啉(分析纯,上海试剂三厂),硫酸铁(Ⅲ)铵(分析纯,国药集团化学试剂有限公司)。
2.3 实验试剂
弱酸艳蓝溶液(c=1.000×10-3mol·L-1),高碘酸钾溶液(c=1.000×10-3mol·L-1),镍(Ⅱ)标准储备液(ρ=1.000 g·L-1),盐酸溶液(c=1.0 mol·L-1),1,10-菲啰啉溶液(w=0.1%),铁(Ⅲ)标准储备液(ρ=0.1000 g·L-1),所用试剂均为分析纯,实验用水均为3次水(2次蒸馏+1次M illi-Q柱)。
3 实验方法和数据处理
3.1 实验方法
于2只10 m L比色管中分别加入0.50 m L弱酸艳蓝溶液(c=1.000×10-3mol·L-1),0.60 m L盐酸溶液(c=0.5 mol·L-1),2.00 mL 1,10-菲啰啉(w=0.1%),其中一只加入一定量的铁(Ⅲ)和镍(Ⅱ)标准溶液(吸光度为A),另一只不加铁(Ⅲ)和镍(Ⅱ)标准溶液(吸光度为A0),先用M illi-Q水稀释至约7 m L处,然后分别在2只比色管中各加入3.00 m L高碘酸钾溶液(c=1.000×10-3mol·L-1)后开始计时,再用M illi-Q水定容至刻度,摇匀。用1 cm比色皿,以M illi-Q水为参比在λ=627 nm处,测定催化和非催化反应体系的吸光度A和A0,计算吸光度的差值△A=A0-A。然后利用M atlab语言自编CPA矩阵法程序,根据所得的△A计算试液中铁和镍的含量。
3.2 测定条件的确定
3.2.1 介质的酸度、温度和RAWL浓度的影响 在利用催化动力学法测定单组份镍的实验中,已经得到最佳实验条件为:酸度p H=2.00,温度t=25.0℃,弱酸艳蓝(RAWL)溶液的浓度c=5.00×10-5mol·L-1[10]。因此当利用CPA矩阵—催化动力学光度法测定双组份镍和铁的实验时,在保持p H、温度和RAWL的浓度等条件不变的基础上,研究其他因素对镍和铁混合组分的影响。
3.2.2 1,10-菲啰啉用量的影响 1,10-菲啰啉是铁(Ⅲ)催化作用的活化剂,加入1,10-菲啰啉可有利于铁(Ⅲ)和镍(Ⅱ)的同时测定。为考察1,10-菲啰啉的含量对△A值的影响,分别加0.50,1.00,2.00,3.00,4.00,5.00 m L的1,10-菲啰啉溶液(w=0.1%)于不同的10 m L比色管中,按3.1节实验方法,得到吸光度差值△A,绘制△A与加入1,10-菲啰啉体积的关系曲线,结果如图1所示。
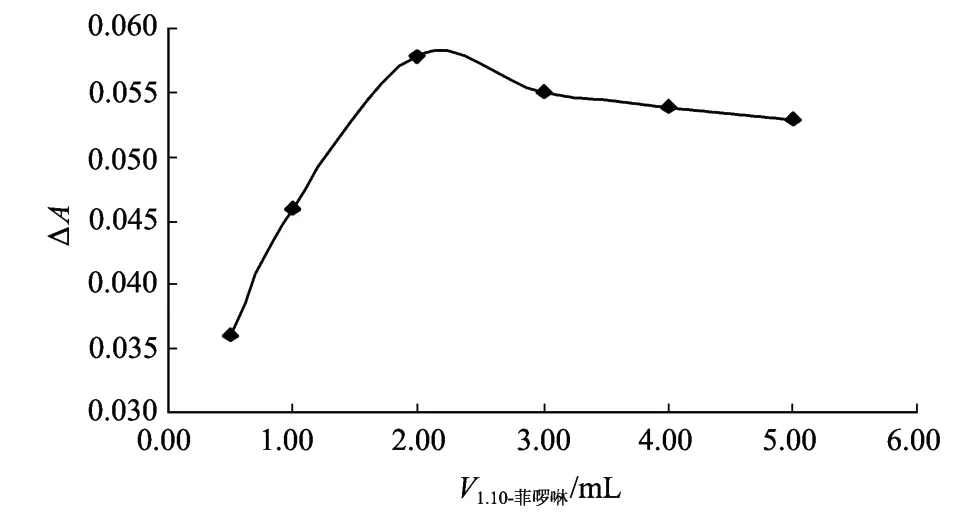
图1 1,10-菲啰啉的体积对△A的影响Fig.1 Effects of 1,10-phenanthroline’s volum added onΔA
从图1可以看出:加入的1,10-菲啰啉的体积在0.50~2.00 mL范围内时,△A随着1,10-菲啰啉加入量的增加而逐渐增加,在加入体积V=2.00 m L时,△A出现了最大值,然后△A值逐渐减小,因此选择加入1,10-菲啰啉溶液的体积为V=2.00 m L。3.2.3 KIO4浓度的影响 在p H=2.00,取1,10-菲啰啉溶液2.00 mL时,考察在KIO4浓度c=2.00×10-5~2.40×10-4mol/L范围内,c(KIO4)的变化对△A值的影响。按3.1节实验方法,得到吸光度差值△A,绘制△A与不同浓度KIO4溶液的关系曲线,结果如图2所示。

图2 高碘酸钾浓度对△A的影响Fig.2 Effects of KIO4 concentration onΔA
从图2可以看出,随着c(KIO4)的增加,吸光度差值△A迅速增加,在c(KIO4)=1.20×10-4mol/L处出现峰值。当c(KIO4)>1.20×10-4mol/L时,△A值开始明显减小。因此选择KIO4溶液的最佳浓度为c(KIO4)=1.20×10-4mol/L。
3.2.4 最佳实验条件的确定 由以上实验结果,可确定同时测定铁(Ⅲ)和镍(Ⅱ)的最佳分析条件是:p H=2.00,t=25.0℃,V(1,10-菲啰啉)=2.00 m L,c(KIO4)=1.2×10-4mol·L-1,c(RAWL)=5.00×10-5mol·L-1,反应时间t=10 m in[10]。
4 分析方法的建立
4.1 铁(Ⅲ)和镍(Ⅱ)测定的线性范围
按3.1节实验方法,固定铁(Ⅲ)质量浓度为10 ng·mL-1,分别加入不同质量浓度的镍(Ⅱ)标准溶液,绘制△A与不同质量浓度的镍(Ⅱ)标准溶液的关系曲线;再固定镍(Ⅱ)质量浓度为10 ng·m L-1,分别加入不同质量浓度的铁(Ⅲ)标准溶液,绘制△A与不同质量浓度的铁(Ⅲ)标准溶液的关系曲线。测得铁(Ⅲ)、镍(Ⅱ)的线性范围分别如图3和图4所示。
由图3和图4可以看出,铁(Ⅲ)质量浓度在0~70 ng·mL-1范围内与△A呈线性关系,线性关系为△A=0.0037ρ(Fe3+)-0.0067。镍(Ⅱ)质量浓度在0~60 ng·mL-1范围内与△A呈线性关系,线性关系为△A=0.0046ρ(Ni2+)-0.0039。
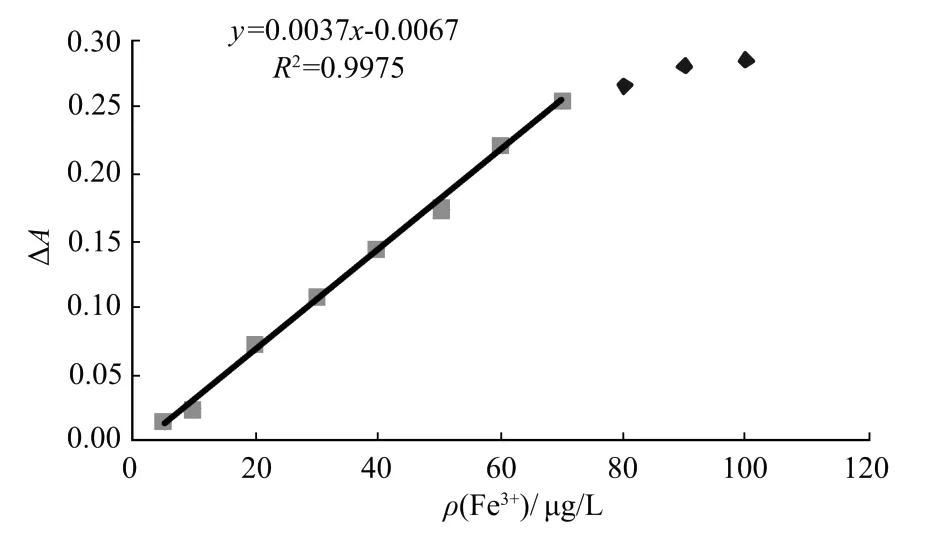
图3 ρ(Fe3+)与△A的线性关系Fig.3 Linear relation ofρ(Fe3+)and△A
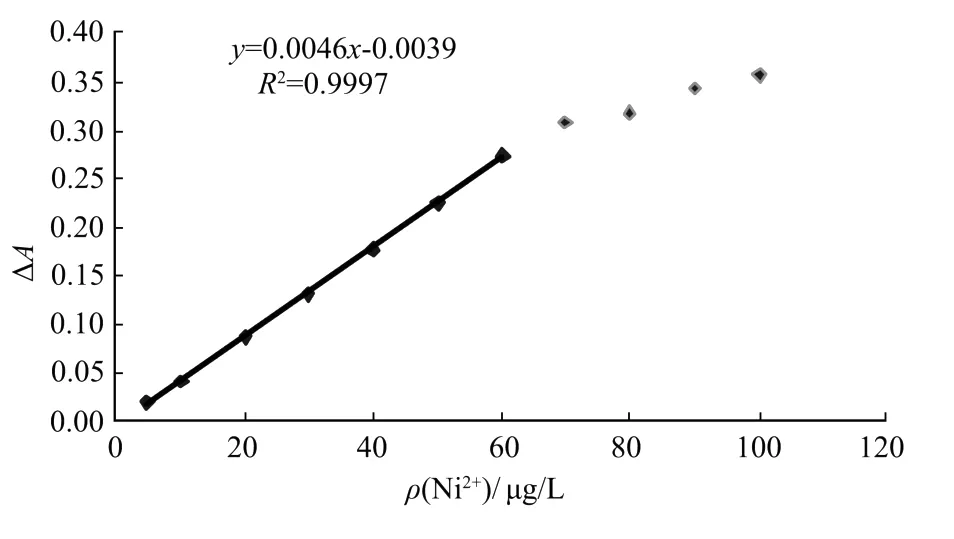
图4 ρ(Ni2+)与△A的线性关系Fig.4 Linear relation ofρ(Ni2+)and△A
4.2 校正溶液的组成
在铁(Ⅲ)和镍(Ⅱ)的线性范围内,按正交设计配制7组标准混合溶液,铁(Ⅲ)质量浓度分别为:0,20,30,40,50,60,40 ng·m L-1;镍(Ⅱ)质量浓度分别为:50,60,70,0,20,30,50 ng·mL-1。配制的原则是尽可能地提取铁(Ⅲ)和镍(Ⅱ)各自的信息以及不同浓度比时交互作用的信息。
4.3 分析方法的准确度和精密度
以ρ(Fe3+)=40.00 ng·m L-1和ρ(Ni2+)=20.00 ng·m L-1的混合液为样品,按CPA矩阵-催化动力学光度法进行测定和数据处理,检验本方法的准确度及精密度,2组共6次的实验结果如表1所示。从表1中可看出:测量结果的相对标准偏差RSD在0.61%~2.32%之间,通过加标实验测得的回收率在96.4%~103.4%之间。实验结果说明:本方法具有较高的准确度和精密度。
以空白试剂进行11次重复实验,求出相对标准偏差S,按3S/K计算出该方法对镍(Ⅱ)的检出限为0.66 ng·mL-1及对铁(Ⅲ)的检出限为0.41 ng·mL-1。
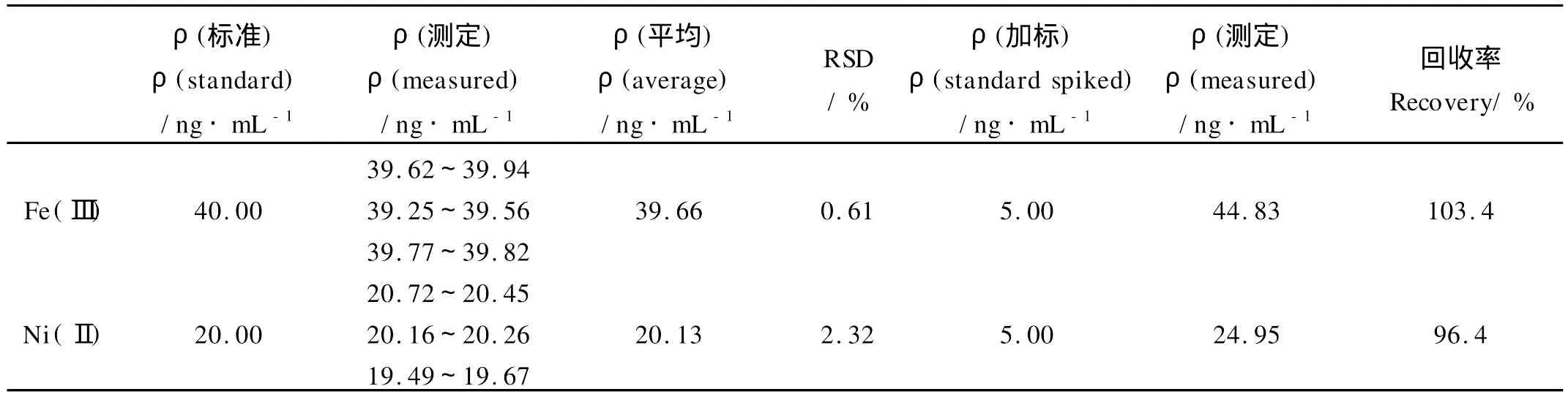
表1 准确度和精密度实验结果Table 1 The experimental results of accuracy and p recision
4.4 铁(Ⅲ)和镍(Ⅱ)混合样品的测定
对铁(Ⅲ)和镍(Ⅱ)质量浓度分别在5~60 ng·mL-1范围内的12组铁镍混合试液(Ni和Fe的质量浓度比从1∶12~12∶1)按CPA矩阵-催化动力学光度法进行测定和数据处理,测定结果见表2。
由表2中的结果可看出,铁(Ⅲ)和镍(Ⅱ)2组分的浓度均在线性范围内,浓度比在1∶12~12∶1时,可获得满意的结果。铁(Ⅲ)的回收率在95.6%~104.4%之间,回收率平均值为99.1%。镍(Ⅱ)的回收率在95.4%~104.9%之间,回收率平均值为98.7%。
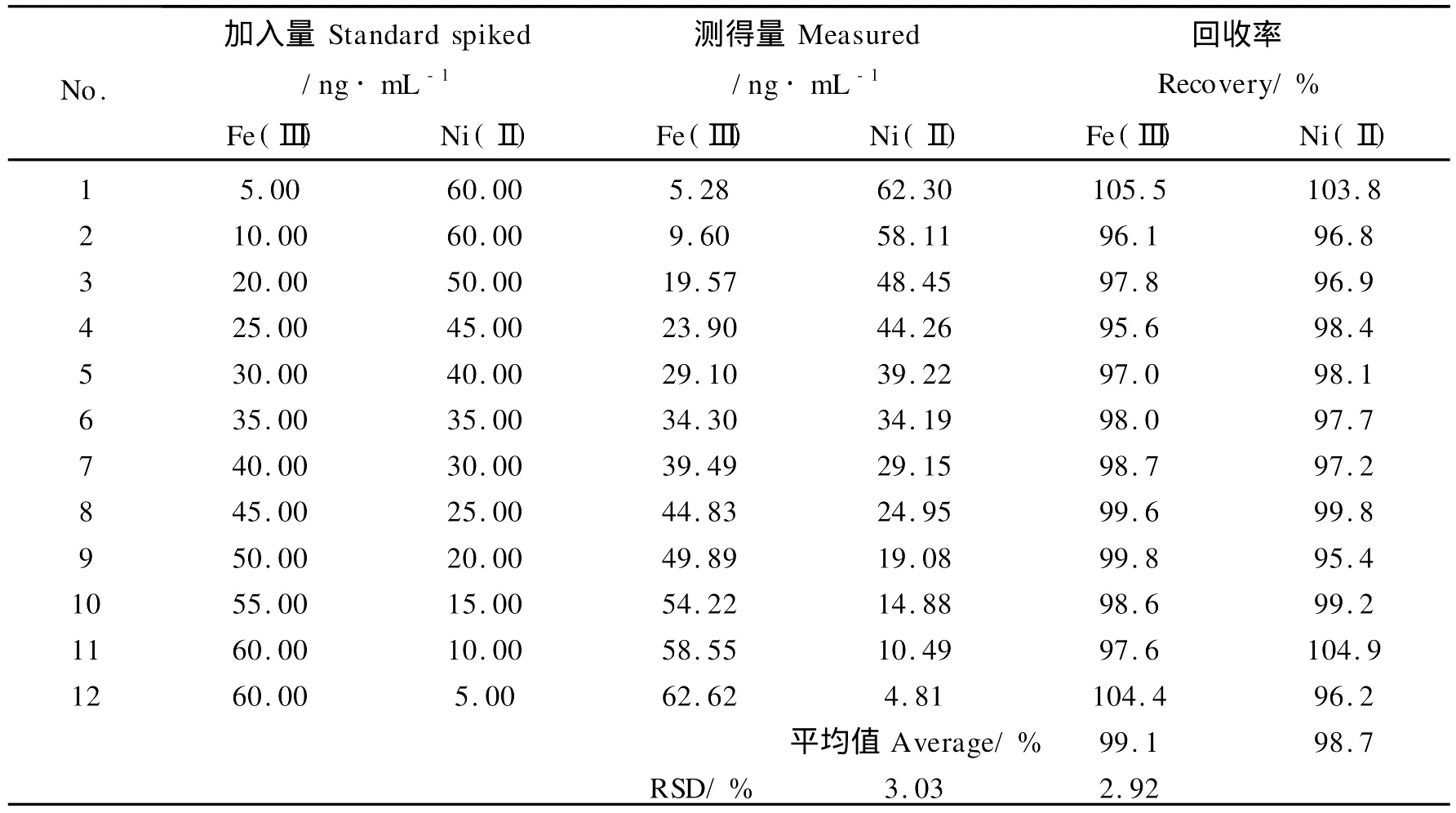
表2分析结果和回收率Table 2 The analytical results and recovery
对铁(Ⅲ)和镍(Ⅱ)质量浓度分别5,10,35,60 ng·m L-1范围内的4组铁镍混合试液(ρ(Ni2+)∶ρ(Fe3+)=1∶1)按CPA矩阵—催化动力学光度法进行测定和数据处理,测定结果及回收率见表3。
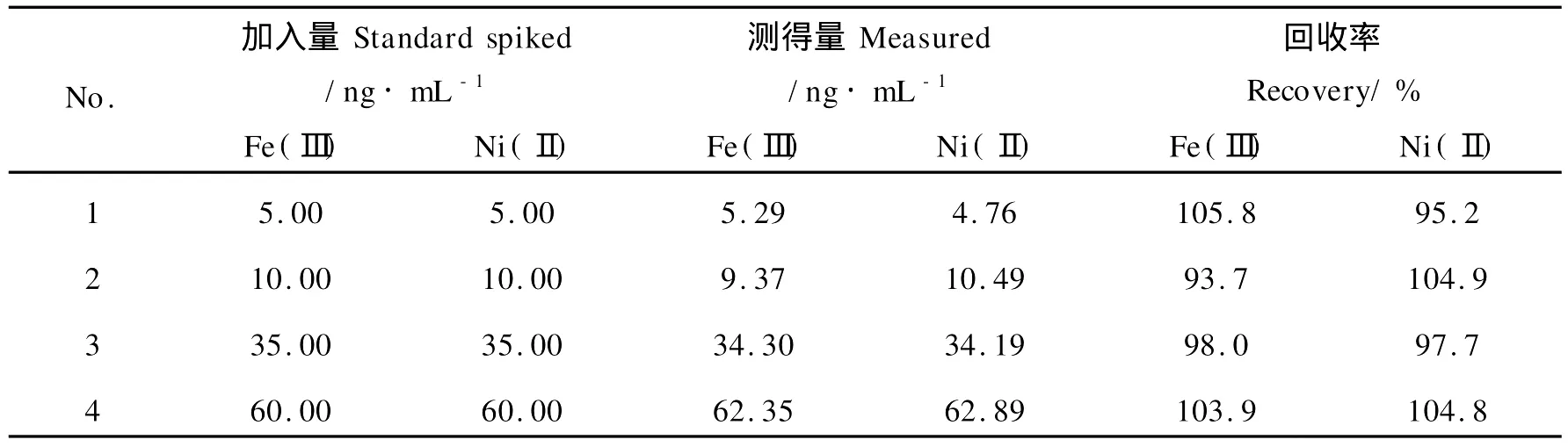
表3 测定结果和回收率Table 3 The analytical results and recovery
由表3的结果可看出,在铁(Ⅲ)和镍(Ⅱ)2组分的浓度比均为1∶1时,也均可获得满意的结果,铁(Ⅲ)的回收率在93.7%~105.8%之间;镍(Ⅱ)的回收率在95.2%~104.9%之间。
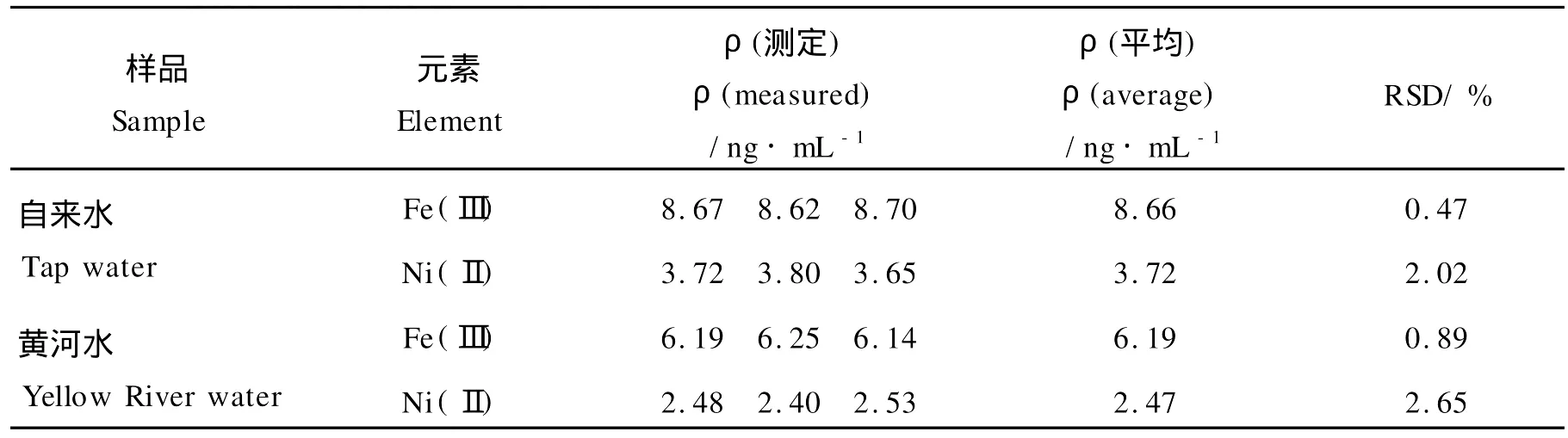
表4 淡水样品分析结果Table 4 The analytical results of freshwater samp les
5 自来水和黄河水样品的测定
5.1 样品的测定
分别移取5.00 m L自来水、利津段黄河水的水样于10 mL比色管中,按CPA矩阵—催化动力学光度法进行测定和数据处理,实验结果如表4所示。
从表4中可看出:自来水中ρ(Fe3+)为8.66 ng·mL-1和ρ(Ni2+)为3.72 ng·m L-1;黄河水中ρ(Fe3+)为6.19 ng·m L-1和ρ(Ni2+)为2.47 ng·mL-1,测定结果的相对标准偏差在0.47%~2.65%之间。
5.2 方法的准确度和精密度
分别对自来水、黄河利津段的水样加标进行回收率实验。移取5.0 m L上述淡水水样于10 m L比色管中,依次加入RAWL溶液、盐酸溶液、相同浓度的铁(Ⅲ)和镍(Ⅱ)标准溶液,再加入KIO4溶液后,用M illi-Q水定容,按CPA矩阵—催化动力学光度法进行测定和数据处理,2组实验每组平行3次的平均结果如表5所示。
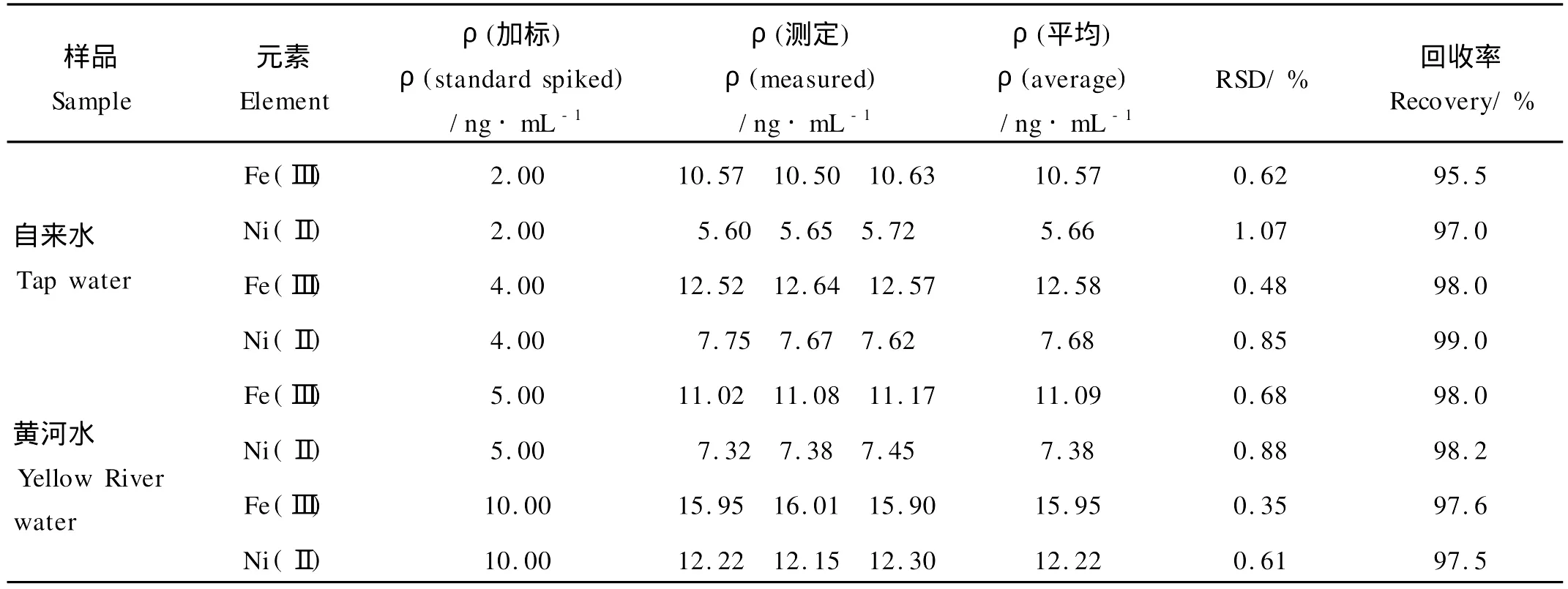
表5 准确度和精密度实验结果Table 5 The experimental results of accuracy and p recision
从表5中可看出:在淡水介质中加入相同质量浓度Ni2+、Fe3+标准溶液进行测定时,测得结果的相对标准偏差在0.35%~1.07%之间,加标回收率在95.5%~99.0%之间。
6 结语
本论文建立了能同时测定痕量铁(Ⅲ)和镍(Ⅱ)的CPA矩阵—催化动力学光度法分析方法,并将该方法应用于淡水中铁(Ⅲ)和镍(Ⅱ)含量的测定。在确定的最佳分析反应条件下,铁(Ⅲ)的线性范围为0~70.00 ng·mL-1,镍(Ⅱ)的线性范围为0~60.00 ng·mL-1。所建方法的相对标准偏差为0.61%~2.32%,对铁(Ⅲ)和镍(Ⅱ)质量浓度分别在5.00~60.00 ng·mL-1范围内的12组铁镍混合液进行测定,回收率在95.4%~104.4%。对自来水和黄河水水样的测定结果表明:铁(Ⅲ)和镍(Ⅱ)的回收率为95.5%~99.0%。
[1] 刘秀萍,陈浩汉,张志琪.反相流动注射催化光度法测定痕量铁[J].分析化学,1997,25(8):986.
[2] RUZIEKA J,HANSEN E H.Flow injection analysis[M].New York:New York Wiley,1981.
[3] KLESZCZEWSKA E.F IA-spectrophotometric determination of ascorbic acid in rat’s lung by reduction of iron(Ⅲ)[J].Journalof Trace and Microp robe Techniques,2003,21(1):85-94.
[4] W IRYAWAN A.Use of flow injection analysis for continuous mornitoring of river water quality[J].Laboratory Robotics and Autormation,2000,12(3):142-148.
[5] 王贤奕,赵云,洪陵成.水中Cr(Ⅵ)的流动注射在线监测[J].环境监测管理与技术,2007,19(2):39-40.
[6] 刘少民,潘教麦.新显色剂二甲氧基羟基苯基荧光酮双波长分光光度同时测定铝和铁的研究[J].分析科学学报,1999,15(5):398-401.
[7] 高甲友,罗丹明.荧光光度法测定痕量铁(Ⅲ)[J].理化检验-化学分册,2007,43(5):405-406.
[8] Zhang X,Shiraishi Y,Hirai T.Fe(III)-and Hg(II)-selective dual channel fluorescence of a rhodamine-azacrow n ether conjugate[J].Tetrahedron Letters,2008,49(26):4178-4181.
[9] Ji H W,Xu J,Xin H Z,et al.A Kinetic Spectrophotometric Method for the Determination of Iron(III)in Water Samp les[J].J.Ocean Univ.China(Oceanic and Coastal Sea Research),2008,7(2):161-165.
[10] Ji Hongwei,CAO Hengxia,XIN Huizhen,et al.Study on the Determination of Trace Ni(II)by the Catalytic Kinetic Spectrophotometric M ethod[J].J.Ocean Univ.China(Oceanic and Coastal Sea Research),2010,9(1):25-29.
[11] Ji H W,Sha Y Y,Xin H Z,et al.Measurement of Trace Manganese(II)by the Catalytic Kinetic Spectrophotometric Method[J].J.Ocean Univ.China(Oceanic and Coastal Sea Research),2009,8(2):127-132.
[12] 骆丽君.电镀污泥中重金属铜和镍含量的分析研究[J].天津化工,2009,23(5):52-53.
[13] 倪永年.化学计量学在分析化学中的应用[M].北京:科学出版社,2004,157-159.
[14] 刘秀萍.CPA矩阵法同时测定铁和锰的研究[J].晋中学院学报,2007,24(3):19-21.
