VC磷酸酯的HPLC分析
2011-01-05张会轻袁立国王淑华王云霞
张会轻,袁立国,王淑华,王云霞
(河北维尔康制药有限公司,河北石家庄 050031)
VC磷酸酯的HPLC分析
张会轻,袁立国,王淑华,王云霞
(河北维尔康制药有限公司,河北石家庄 050031)
建立了高效液相色谱法(HPLC)测定L-抗坏血酸-2-磷酸酯含量的分析方法。采用Agilent Eclipse XDB C18分析柱(250mm×4.0mm,5μm),以甲醇-0.1mol/L磷酸二氢钾(pH 值为4.4)为流动相,二者体积比为35∶65,流速为1.0mL/min,检测波长为254nm。在此色谱条件下,L-抗坏血酸-2-磷酸酯在0.01~0.10mg/mL质量浓度范围内呈现良好的线性关系,相关系数为0.999 9,样品平均回收率为98.24%。
VC磷酸酯;高效液相色谱法;VC
VC 磷 酸 酯 (L-ascorbic acid-2-phosphate,APP)又名L-抗坏血酸-2-磷酸酯,是 VC的稳定衍生物,是以VC为原料用现代科学技术加工而成的。VC磷酸酯耐受高温、高压、高湿等恶劣条件,其抵御饲料存贮过程中复杂环境的能力大大超过结晶VC和包膜VC。无论是在制粒过程中还是在调质膨化过程中,L-抗坏血酸-2-磷酸酯的保存率都大于90%[1]。VC磷酸酯的主要构成成分是VC和磷。VC磷酸酯具有VC的所有功效,又克服了VC易受光、热、金属离子等作用而氧化的缺点,因此在饲料中添加该产品不但不会改变饲料的质量,而且可以增加饲料的营养价值,是水产养殖的优选添加剂。但是,VC的化学活性高,不稳定,极易被氧化分解,从而失去VC的功效,在高温或光照下分解更快,在高温的酸性介质中容易脱水而失去活性[2-3]。与VC相比,VC磷酸酯具有下列优点:1)化学性质稳定,不易氧化;2)对热稳定性高;3)生物利用度高,VC磷酸酯可以被生物体内的磷酸酶分解,具有与VC相同的生物效价。
1 材料与方法
1.1 试剂与仪器
VC磷酸酯标准品(纯度>99%,北京贝丽莱斯生物化学有限公司提供);甲醇(色谱纯);纯化水。
WATERS高效液相色谱仪,2487紫外检测器。
1.2 色谱条件
色谱柱:Agilent Eclipse XDB C18分析柱(250 mm×4.0mm,5μm);流动相:甲醇-0.1mol/L磷酸二氢钾(pH值为4.4,二者体积比为35∶65);紫外测定波长为254nm;流速为1.0mL/min;进样20μL。
1.3 流动相配制
精密称取13.609g(0.1mol)磷酸二氢钾,用纯化水溶解并定容至1L,用85%(体积分数)磷酸调节pH值至4.4,即得0.1mol/L的磷酸二氢钾溶液(pH值为4.4)。用有机膜过滤,超声溶解20min,备用。
2 结果与讨论
2.1 检测波长的选择
采用流动相作为背景缓冲液,用二极管阵列检测器对L-抗坏血酸-2-磷酸酯标准液和样品溶液在190~400nm进行全波长紫外扫描。结果表明,L-抗坏血酸-2-磷酸酯在254nm处有最大吸收,且杂峰干扰少,本实验选择检测波长为254nm。
2.2 标准曲线绘制和检出限
准确称取3-环己胺-抗坏血酸-2-磷酸酯(纯度大于99.0%)标准品0.316g,用磷酸盐缓冲溶液溶解并定容在100mL棕色容量瓶中。其中L-抗坏血酸质量浓度为1.0mg/mL。分别移取上述溶液1.0,2.0,4.0,5.0,10.0mL,置于100mL棕色容量瓶中,用磷酸盐缓冲溶液溶解并定容,配成0.01,0.02,0.04,0.05,0.10mg/mL(以L-抗坏血酸质量浓度计)的标准工作溶液。按1.2色谱条件测定,以质量浓度(X)为横坐标,峰面积积分值(Y)为纵坐标,绘制工作曲线,见图1。结果表明,线性范围为0.01~0.10mg/mL时呈现良好的线性关系,回归方程为Y=8 148.3X-14.092,R2=0.999 9。

图1 标准工作曲线Fig.1 Standard curve
2.3 精密度实验
配制质量浓度为0.05mg/mL的VC磷酸酯标准品溶液,重复进样5次,每次20μL,测定其峰面积,计算RSD值为0.113%。计算结果见表1。

表1 精密度结果Tab.1 Results of precision
2.4 稳定性实验
配制质量浓度为0.05mg/mL的VC磷酸酯标准品溶液,在室温下每隔2h测定一次溶液中VC磷酸酯的含量,计算RSD值为0.503%(见表2)。结果表明:VC磷酸酯在流动相溶液中6h内是稳定的。

表2 稳定性实验Tab.2 Test of stability
2.5 加样回收率实验
取已知含量试样,向其中加入定量的标准品溶液,进行色谱分析测定,加样回收率平均值为98.24%,计算结果见表3。

表3 加样回收率结果Tab.3 Results of recovery
2.6 样品的测定
准确称取样品0.020 0g,放入100mL棕色容量瓶内,用流动相溶解,超声时间为10min,用0.45 μm的滤膜过滤,按1.2色谱条件进样,用外标法进行计算。由实验得知,标准品谱图(见图2)与色谱图(见图3)保留时间相一致。
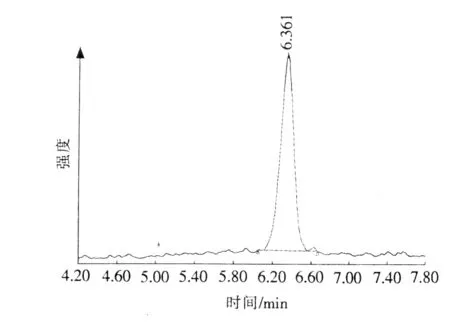
图2 L-抗坏血酸-2-磷酸酯标准品谱图Fig.2 Chromatograms of standard of L-ascorbic acid-2-phosphate
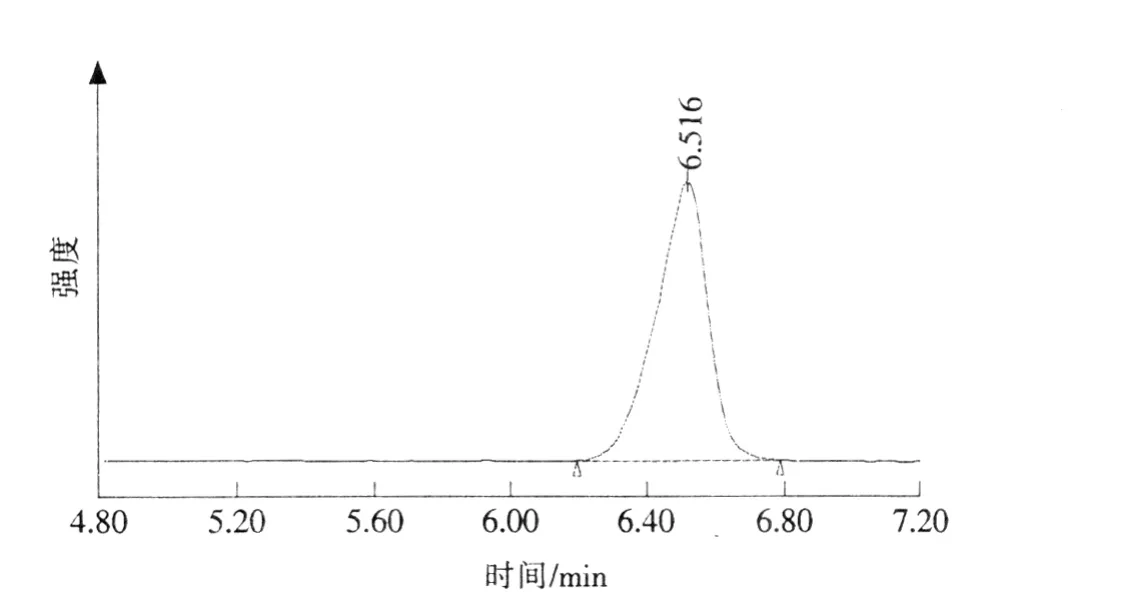
图3 L-抗坏血酸-2-磷酸酯样品谱图Fig.3 Chromatograms of sample of L-ascorbic acid-2-phosphate
[1]程 恩,宋国梁,路文江.高效价L-抗坏血酸-2-磷酸酯的稳定性研究[J].河北化工,2001(4):19-20.
[2]CHARLES W D.Method of Preparation of Phosphate Ester of AscorbicAcid[P].US:4179445,1979-06-02.
[3]CHEN L,SEIB P A,LIANG Y T,et al.Chemical synthesis of several phosphoric esters ofL-ascorbic acid[J].Carbohydr Res,1978,67(1):127-138.
HPLC analysis ofL-ascorbic acid-2-phosphate
ZHANG Hui-qing,YUAN Li-guo,WANG Shu-hua,WANG Yun-xia
(Hebei Welcome Pharmaceutical Company Limited,Shijiazhuang Hebei 050031,China)
A phase high performance liquid chromatographic method has been developed for the determination ofL-ascorbic acid-2-phosphate.Agilent Eclipse XDB C18(250mm×4.0mm,5μm)column is used and the mobile phase is the mixture of methanol-0.1mol/L phosphoricacid two hydrogen potassium buffer solution(35︰65,V/V).The flow rate is 1.0mL/min,and the detection wavelength is 254nm.The linear range is 0.01~0.10mg/mL,and the related coefficient is 0.999 9,the average recovery rate ofL-ascorbic acid-2-phosphate in the samples is 98.24%.
L-ascorbic acid-2-phosphate;HPLC;vitamin C
TQ443
A
1008-1534(2011)06-0364-02
2011-06-03;
2011-09-20
张士莹
张会轻(1977-),女,河北石家庄人,工程师,主要从事药物研发与分析方面的工作。
