纳米零价铁对γ-HCH的降解效果及机理研究
2010-12-21祝凌燕朱淑贞南开大学环境科学与工程学院教育部环境污染过程与基准重点实验室天津市城市生态环境修复与污染防治重点实验室天津300071
常 春,祝凌燕,朱淑贞 (南开大学环境科学与工程学院,教育部环境污染过程与基准重点实验室,天津市城市生态环境修复与污染防治重点实验室,天津 300071)
纳米零价铁对γ-HCH的降解效果及机理研究
常 春,祝凌燕*,朱淑贞 (南开大学环境科学与工程学院,教育部环境污染过程与基准重点实验室,天津市城市生态环境修复与污染防治重点实验室,天津 300071)
采用液相还原法制备纳米零价铁(nZVI),透射电镜表征显示,其粒径<20nm,在介质中处于团簇状态.利用所合成的nZVI对γ-HCH进行了还原脱氯研究,结果表明,nZVI具有很高的表面反应活性,当用量为0.5g/L时,反应90min,对2.5mg/L的γ-HCH去除率达90%以上.nZVI对γ-HCH的去除符合准一级反应动力学方程,其反应速率和去除率与pH值、nZVI添加量、γ-HCH初始浓度、共存离子等因素有关.反应速率随pH值的减小而增大,NO3-对反应速率有较强的抑制作用,Ca2+,Mg2+和SO42-对反应速率影响不大.利用GC-MS检测到降解产物四氯环己烯(TeCCH)和氯苯(CB)的存在,推测反应机制为双氯脱除反应和脱氯化氢反应.
nZVI;γ-HCH;脱氯;反应动力学;反应机制
HCHs曾经在我国大量使用,它具有化学性质稳定、半衰期长、不易分解和亲脂特性[1].作为HCH唯一有效成分的γ-HCH(林丹),仍然在许多国家和地区使用,在一些地区甚至有较高的检出
[2-4].虽然γ-HCH在自然条件下能被降解,但这一过程非常缓慢.因此,采用物理、化学或生物的方法对 γ-HCH进行降解具有十分重要的意义.然而,对 γ-HCH有效降解途径的研究相对较少,并主要集中在其生物降解的探讨上[5-9],而非生物降解只是偶有提及.
近年来,纳米零价铁(nZVI)被用于环境污染治理[10-11].nZVI粒径小,具有较大的表面积及表面能[12-13],因而具有优良的表面吸附和较高的化学反应活性[14],是一种有效的脱卤还原剂,可以催化还原多种有机卤化物,如卤代烷烃[15]、卤代烯烃[16]、卤代芳香烃[17]等,将这些难降解有机污染物转化为无毒或低毒的化合物.
本实验以七水合硫酸亚铁和硼氢化钾为原料,采用液相还原法制备nZVI,对其降解γ-HCH的反应动力学、影响因素、降解机制等进行探讨.
1 材料与方法
1.1 试剂与设备
试剂包括:硼氢化钾(KBH4,天津傲然精细化工研究所)、七水合硫酸亚铁(天津市北方天医化学试剂厂)、聚乙二醇-4000(上海天莲精细化工有限公司)、叠氮化钠(成都市科龙化工试剂厂)、无水乙醇(天津市北方天医化学试剂厂)、硫酸镁(天津市北方天医化学试剂厂)、硫酸钙(天津市北方天医化学试剂厂)、硝酸镁(天津市永大化学试剂开发中心),以上试剂均为分析纯.正己烷(色谱纯,天津市康科德科技有限公司)、γ-HCH (AccuStandard, New Haven,CT,USA).
设备包括:气浴恒温振荡器(TH2-C,太仓市实验设备厂)、低速大容量离心机(上海安亭科学仪器厂)、数显电动搅拌器(JJ-6A,金坛市金南仪器厂)、气相色谱(Agilent 6890N)配有ECD检测器、气相色谱-质谱联用仪(Thermo-Quest, Austin, TX,USA)、透射电镜(JEM-2010FEF,200KV,日本JEOL).
1.2 nZVI的制备
nZVI采用液相还原法合成.室温下,将0.0669mol/L KBH4水溶液通过恒压漏斗以2滴/s的速度滴加到装有0.0223 mol/L FeSO4•7H2O醇/水混合体系(醇/水比为 3:1)的三口烧瓶中,两种溶剂的体积相等.并加入适量 PEG-4000作为分散剂,在高纯氮气保护下以1500 r/min进行快速搅拌,溶液中立刻出现黑色沉淀,其反应为:
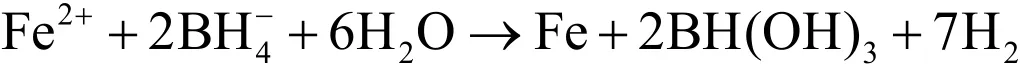
待KBH4溶液滴加完毕后,继续搅拌30min.弃去上清液,分别用脱氧去离子水和无水乙醇洗涤数次,最后保存在无水乙醇中备用.
1.3 透射电镜(TEM)表征所合成材料的性质
用吸管从反应器中取出少量溶液,密封保存在小试管中,利用超声使其分散均匀,再将溶液滴在铜网上,利用 TEM对所合成的零价铁的粒度和形貌进行分析.
1.4 降解动力学实验
反应在100mL顶空瓶中进行,瓶中加入一定量的nZVI和一定浓度的γ-HCH水溶液,并加入50mg/L的叠氮化钠抑制微生物生长,瓶口用带聚四氟乙烯的橡胶塞密封,置于恒温振荡器中振荡(25℃,225r/min),用注射器定时取样 2mL,过0.45µm滤膜后用 2mL正己烷萃取,用气相色谱测定反应产物.
1.5 样品编号
pH值3.5,7.0,9.5分别编号为P1,P2,P3;nZVI浓度为0.25,0.50,1.00g/L分别编号为F1,F2,F3;γ-HCH 浓度为 1.25,2.50,5.00mg/L分别编号为L1,L2,L3;考虑共存离子时的编号,加入CaSO4为P2F2L2CS,加入 MgSO4为 P2F2L2MS,加入Mg(NO3)2为P2F2L2MN.
1.6 分析方法
采用Agilent 6890N自动进样气相色谱-电子捕获检测器测定,柱子为 HP-5(30m×0.32mm× 0.25µm);γ-HCH 的工作条件:进样口温度为200
℃,检测器温度为 300℃,高纯氮气作为载气和尾吹气,流速分别为 20mL/min和 30mL/min,程序升温为初始温度 100℃,以 30℃/min升至180℃,保留 1min,以 5℃/min升至 200℃,以30℃/min,升至240℃.
采用 GC-MS (Thermo-Quest,Austin,TX, USA)测定γ-HCH降解产物.降解反应条件为:pH 7.0,nZVI用量0.5g/L,γ-HCH浓度2.5mg/L,反应45min.实验重复 3次.GC/MS所用柱子为DB-5(30m×0.25mm×0.25µm),采用电子轰击源(EI)和全扫描模式,质量范围(m/z)50~650amu,进样口温度为 250℃,离子源温度为 230℃,程序升温为初始温度35℃,保留1min,以15℃/min升至150℃,保留4min,以15℃/min升至250℃.
2 结果与讨论
用 TEM(JEM-2010FEF,200kV)观察所合成的nZVI的形貌特征,由图1可见,所合成的nZVI粒径<20nm,颗粒尺寸均匀、呈球状,有规则由球心向外呈辐射状生长堆积形成一个较大的纳米 铁团簇,团簇中的孔隙和通道清晰可见.

图1 透射电镜下的纳米零价铁Fig.1 TEM image of nZVI
2.1 nZVI与普通铁粉降解效果的比较
γ-HCH的初始浓度为 2.5mg/L,在相同实验条件下分别采用 2.5g/L普通铁粉(100目)和0.5g/L nZVI进行还原脱氯比较实验,结果见图2.
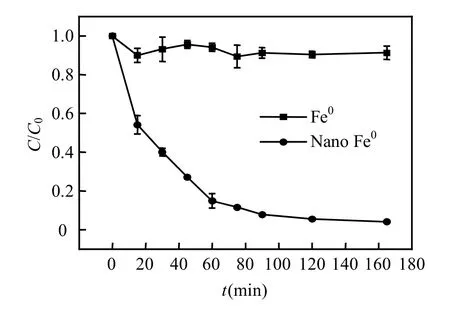
图2 普通铁粉与nZVI还原γ-HCH的比较Fig.2 Comparison of the reduction effect of γ-HCH with nZVI and normal Fe power
从图2可见,中性条件下2.5g/L的普通铁粉在 165min内对 γ-HCH的去除率不足 10%,而0.5g/L的nZVI,在90min之内即可获得大于90%的去除率.这主要是由于球形颗粒的比表面积和直径成反比,随着粒径变小,粒子比表面积显著增大,同时表面原子占总原子的百分数也显著提高,当尺寸达到纳米尺度时,表面原子所占比例由微米尺度时的 1%~2%急剧增加到超过 50%[13].表面原子所占比例的增加使得nZVI的表面反应活性大幅提高.
2.2 降解反应动力学
在nZVI过量的情况下,γ-HCH的还原脱氯反应可以看作准一级速率反应,其动力学方程可表示为:

积分变得:
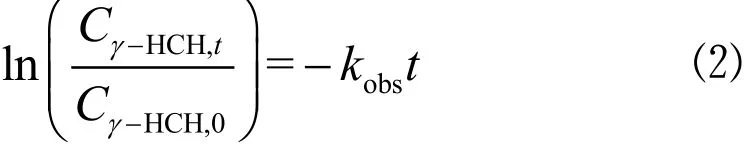

半衰期可表示为:式中:t为反应时间,min;t1/2为反应半衰期,min; Cγ-HCH,t为 t时刻溶液中 γ-HCH 的浓度,mg/L; Cγ-HCH,0为 γ-HCH的初始浓度,mg/L;kobs为该降解反应的准一级速率常数,min-1.以ln(C/C0)-t曲线作图,如图3所示.

图3 γ-HCH脱氯反应动力学Fig.3 Dechlorination kinetics for γ-HCH
由图3可知,ln(C/C0)与t具有很好的线性关系,说明在该反应条件下,nZVI对γ-HCH的还原脱氯反应基本符合准一级反应动力学方程.通过式(2)拟合可以得出 nZVI在不同反应条件下还原γ-HCH的反应速率常数和半衰期,见表1.

表1 nZVI还原γ-HCH的反应速率常数和半衰期Table 1 Reaction rate constant and half life for reduction of γ-HCH by nZVI
2.3 nZVI对γ-HCH降解反应的影响因素
2.3.1 溶液初始pH值的影响 在nZVI-H2O体系中,溶液的 pH值是降解反应的重要影响因素
[18].由图4和表1可以看出,随着溶液pH值的降低,nZVI降解γ-HCH的速率逐渐上升.在强酸性条件下,nZVI还原γ-HCH具有较快的反应速率,调节溶液初始pH值3.5,振荡反应60min其去除率可达 95%;在碱性条件下,反应 60min,只有77%被去除.这可能是由于pH值较低时,大量H+的存在导致 nZVI腐蚀速度加快,产生了更多的活性氢(H0)以还原γ-HCH[19];在高pH值条件下,容易产生铁的氢氧化物钝化层并沉积于nZVI表面,表现为反应速率低,且去除效果差.

图4 初始pH值对γ-HCH去除效果的影响Fig.4 Effects of initial pH on the dechlorination efficiency
2.3.2 nZVI添加量的影响 图5和表1表明,随着nZVI添加量的增加,γ-HCH的去除速率加快,相同反应时间的去除率提高.这是由于溶液中 nZVI量的增加增大了其总的比表面积以及新鲜表面和污染物接触的机会,因此加快了反应的进行.

图5 nZVI量对γ-HCH去除效果的影响Fig.5 Effects of amount of nZVI on the dechlorination efficiency
从图 5可见,即使对于 nZVI添加量为0.25g/L的反应体系,振荡反应165min其降解效率也可达到99%以上.表明在实验条件下,只要接触时间足够长,较少量的 nZVI也可以完全去除体系中的γ-HCH,在此基础上nZVI量的增加只是提高了反应速率.因此在实际应用中,应根据需要选择合适的剂量.
2.3.3 γ-HCH初始浓度的影响 不同 γ-HCH初始浓度对反应的影响如图6所示,过量的nZVI与不同初始浓度的γ-HCH溶液反应,表现出相似的反应趋势,对试验中不同初始浓度的溶液,均可达到迅速完全的脱氯效果.
从图6和表1可以看出,当其他实验条件相同时,γ-HCH的初始浓度越高,达到同样去除率所需的时间就越长.

图6 初始浓度对γ-HCH去除效果的影响Fig.6 Effects of initial concentration of γ-HCH on the dechlorination efficiency
2.3.4 共存离子的影响 在实际水样中往往存在大量其他离子,这些离子可能会对γ-HCH还原过程产生不同的影响,分别考察了几种常见共存离子对γ-HCH去除过程的干扰作用,干扰离子浓度为 200 mg/L.从图 7可知,Ca2+,Mg2+,SO42-对nZVI降解反应的影响较小,而NO3-对γ-HCH的降解反应有明显抑制作用.这可能是由于 NO3-与nZVI发生了脱硝反应[20],与γ-HCH的脱氯反应竞争反应位,在一定程度上阻碍了γ-HCH的去除.
2.4 降解反应机制的研究
在nZVI-γ-HCH反应体系中,运用GC-MS检测,根据质谱特征离子与标样质谱(NIST)进行比对,结果发现有降解产物四氯环己烯和氯苯的存在(图 8).同时,从理论上推测,二氯环己二烯(DCCD)和苯完全可能作为降解产物存在本体系中,但由于二氯环己二烯不稳定而易被进一步脱氯转化,因此,在 GC-MS上未扫描到.同时在GC-FID上检测到微弱的苯的信号峰.

图7 共存离子对γ-HCH去除效果的影响Fig.7 Effects of co-ions on the dechlorination efficiency

图8 γ-HCH被nZVI降解产物的质谱Fig.8 Mass spectrogram of degradation products of γ-HCH by nZVIpH 7.0, nZVI 0.5 g/L,γ-HCH 2.5mg/L,时间45min
根据检测到的降解产物以及上面的理论推测,归纳γ-HCH在nZVI体系中的降解途径如图9所示,与Elliott等[21]利用nZVI降解γ-HCH所得结论一致,另外Middeldorp等[22]与van Doesburg等[23]利用微生物降解 β-HCH也得到了类似转化途径.为了避免微生物降解带来的干扰,在本研究中加入50mg/L的叠氮化钠抑制微生物生长.
γ-HCH在纳米零价铁体系中主要有如下2种转化机制:一是脱氯化氢反应;另一机制为双氯脱除反应,产物可进一步发生脱氯化氢反应(图9).

图9 γ-HCH在纳米零价铁体系中可能的转化途径Fig.9 The possible pathways of γ-HCH transformation in nZVI system
3 结论
3.1 采用液相还原法合成的 Fe0均在纳米级范围内,由于其具有较高的比表面积,对 γ-HCH具有很高的去除效率,0.5g/L的nZVI在90min之内就可以达到90%以上去除效果.
3.2 nZVI对γ-HCH的降解符合准一级反应动力学方程,对 γ-HCH影响因素的研究结果表明,反应速率与pH值、nZVI添加量、γ-HCH初始浓度、共存离子等因素有关.随着pH值的减小反应速率增大,Ca2+,Mg2+和 SO42-对反应速率影响不大,其中SO42-对反应速率略有促进,而NO3-对反应速率有较强的抑制作用.
3.3 根据检出产物及理论推测确定降解途径可能为:γ-HCH→四氯环己烯(TeCCH)→二氯环己二烯(DCCD)→苯和氯苯,涉及 2种反应机制,即双氯脱除反应和脱氯化氢反应.
[1] Walker K, Vallero D A, Lewis R G. Factors influencing the distribution of lindane and other hexachlorocyclohexanes in the environment [J]. Environmental Science and Technology, 1999,33(24):4373-4378.
[2] Ngabe B, Bidleman T F, Falconer R L. Base hydrolysis of alphaand gamma-hexachlorocyclohexanes [J]. Environmental Science and Technology, 1993,27(9):1930-1933.
[3] Huang Hong, Ou Wen-hua, Wang Lian-Sheng. Semivolatile organic compounds, organochlorine pesticides and heavy metals in sediments and risk assessment in Huaihe River of China [J]. Journal of Environmental Science, 2006,18(2):236-241.
[4] 龚香宜,祁士华,吕春玲,等.洪湖表层沉积物中有机氯农药的含量及组成 [J]. 中国环境科学, 2009,29(3):269-273.
[5] Brajesh K, Singh R C K. Degradation of insecticide lindane (gamma-HCH) by white-rot fungi Cyathus bulleri and Phanerochaete sórdida [J]. Pest Management Science, 2000,56(2): 142-146.
[6] Datta J, Maiti A K, Modak D P, et al. Metabolism of gammahexachlorocyclohexane by Arthrobacter citreus strain Bl-100: identification of metabolites [J]. Journal of General and Applied Microbiology, 2000,46(2):59-67.
[7] Deo P G, Karanth N G. Biodegradation of hexachlorocyclohexane isomers in soil and food environment [J]. Critical Reviews Microbiology, 1994,20(1):57-78.
[8] Okeke B C, Siddique T, Arbestain M C, et al. Biodegradation of gamma-hexachlorocyclohexane and alpha-hexachlorocyclohexane in water and a soil slurry by a Pandoraea species [J]. Journal of Agricultural and Food Chemistry, 2002,50(9):2548-2555.
[9] Siddique T, Okeke B C, Arshad M, et al. Temperature and pH effects on biodegradation of hexachlorocyclohexane isomers in water and a soil slurry [J]. Journal of Agricultural and Food Chemistry, 2002,50(18):5070-5076.
[10] Masciangioli T, Zhang W X. Environmental technologies at the nanoscale [J]. Environmental Science and Technology, 2003, 37(5):102A-108A.
[11] Zhang W X. Nanoscale iron particles for environmental remediation: An overview [J]. J. Nanopart Res., 2003,5(3/4):323-332.
[12] Zhang W X, Wang C B, Lien H L. Treatment of chlorinated organic contaminants with nanoscale bimetallic particles [J]. Catal Today, 1998,40(4):387-395.
[13] Ball P, Garwin L. Science at the atomic scale [J]. Nature, 1992, 355(6363):761-766.
[14] Choe S, Chang Y Y, Hwang K Y, et al. Kinetics of reductive denitrification by nanoscale zero-valent iron [J]. Chemosphere, 2000,41(8):1307-1311.
[15] Song H, Carraway E R. Reduction of chlorinated ethanes by nanosized zero-valent iron: kinetics, pathways, and effects of reaction conditions [J]. Environmental Science and Technology, 2005,39(16):6237-6245.
[16] Quinn J, Geiger C, Clausen C, et al. Field demonstration of DNAPL dehalogenation using emulsified zero-valent iron [J]. Environmental Science and Technology, 2005,39(5):1309-1318.
[17] Lowry G V, Johnson K M. Congener-specific dechlorination of dissolved PCBs by microscale and nanoscale zerovalent iron in a water/methanol solution [J]. Environmental Science and Technology, 2004,38(19):5208-5216.
[18] Lu M-C, Anotai J, Liao C-H, et al. Dechlorination of hexachlorobenzene by zero-valent iron [J]. Practice Periodical of Hazardous, Toxic, and Radioactive Waste Management, 2004,8(2): 136-140.
[19] Matheson L J, Tratnyek P G. Reductive dehalogenation of chlorinated methanes by iron metal [J]. Environmental Science and Technology, 1994,28(12):2045-2053.
[20] 李铁龙,刘海水,金朝晖,等.纳米铁去除水中硝酸盐氮的批试验[J]. 吉林大学学报(工学版), 2006,36(2):264-268.
[21] Elliott D W, Lien H L, Zhang W X. Degradation of lindane by zero-valent iron nanoparticles [J]. Journal of Environmental Engineering, 2009,135(5):317-324.
[22] Middeldorp P J M, Jaspers M, Zehnder A J B, et al. Biotransformation of alpha-, beta-, gamma-, and deltahexachlorocyclohexane under methanogenic conditions [J]. Environmental Science and Technology, 1996,30(7):2345-2349.
[23] van Doesburg W, van Eekert M H A, Middeldrop P J M, et al. Reductive dechlorination of β-hexachlorocyclohexane (β-HCH) by a Dehalobacter species in coculture with a Sedimentibacter sp. [J]. FEMS Microbiology Ecology, 2005,54(1):87-95.
Degradation efficiency and mechanisms of γ-hexachlorocyclohexane by nanoscale zero valent iron particles.
CHANG Chun, ZHU Ling-yan*, ZHU Shu-Zhen (Key Laboratory of Pollution Process and Environmental Criteria, Ministry of Education, Tianjin Key Laboratory of Urban Ecology Environmental Remediation and Pollution Control, College of Environmental Science and Engineering, Nankai University, Tianjin 300071, China) . China Environmental Science, 2010,30(2):167~173
Nanoscale zero valent iron particles (nZVI) were synthesized using liquid phase reduction method. TEM analysis indicated that the size of nZVI was < 20 nm, and clustered in the medium. It displayed high reactivity to decompose γ-hexachlorocyclohexane (γ-HCH). More than 90% of γ-HCH was removed in 90 min with 0.5 g/L of nZVI in the solution. The degradation reaction followed a pseudo-first order kinetic. The reaction rate coefficient and removal efficiency were affected by many factors, such as the amount of nZVI, pH, the initial concentration of γ-HCH and coexisting ions. The reaction rate decreased with increasing initial pH. NO3-greatly inhibited the degradation reaction, but
Ca2+, Mg2+and SO42-had little effect on it. Degradation products such as tetrachlorocyclohexene (TeCCH) and chlorobenzene (CB), were identified by GC/MS. Based on this, the main reaction mechanism was suggested as dehydrochlorination and dichloroelmination.
nanoscale zero valent iron particles;γ-hexachlorocyclohexane;dechlorination;reaction kinetics;reaction mechanism
X131
A
1000-6923(2010)02-0167-07
2009-07-17
天津市科学技术委员会(06TXTJJC14000,07JCZDJC01900, 08ZCGHHZ01000);国家水体污染控制专项基金;“十一五”国家科技支撑计划(200603746006);教育部新世纪人才项目.
* 责任作者, 教授, zhuly@nankai.edu.cn
致谢:本实验在纳米零价铁制备过程中得到南开大学环境科学与工程学院博士生安毅的大力帮助,在此表示衷心的感谢.
常 春(1983-),男,辽宁锦州人,南开大学环境科学与工程学院硕士研究生,主要从事纳米材料修复环境污染技术.
