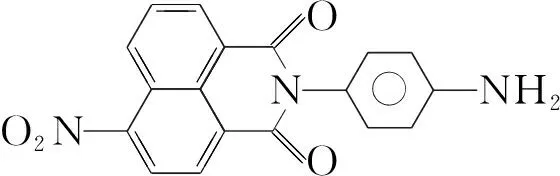
N-{4-[6-硝基-1,3-二酮-1H-苯并[de]异喹啉-2(3H)-基]苯基}-N′-苯基脲的合成及其对阴离子的识别性能
2010-11-26罗俊君
罗俊君, 刘 佳, 任 君
(湖北大学 化学与化工学院,湖北 武汉 430062)
随着超分子化学的发展,分子识别在合成化学﹑生命科学、信息科学及材料科学中起愈来愈重要的作用[1~4]。为了使分子识别所包含的信息简单而有效地向外界传递,可通过巧妙设计的分子器件所发出的光学信号来表达这种信息。荧光检测技术具有方便快捷、灵敏度高等优点,因此荧光化学传感器的研究日益受到人们的重视[5,6]。
由于阴离子在生命科学和化学过程中的重要作用,设计和合成选择性地键合阴离子物种的人工受体,越来越受到人们的广泛关注并成为当前超分子化学研究领域的重要课题[7~9]。对生物学上和环境中重要阴离子具有选择性识别的荧光受体在疾病诊治、环境改造等方面有着广泛的应用前景。

Scheme1
相对于阳离子而言,阴离子具有多样的几何构型(球形、平面型、四面体型等),半径较大,电荷密度小,易受溶剂效应影响。近年来,多种相互作用方式,如氢键作用、静电相互作用和路易斯酸中心阴离子配位作用等,都被应用于阴离子受体化合物的设计和合成。将适当的荧光团和对特定底物有键合作用的受体共价或非共价键合,可得到具有选择性识别性能的阴离子荧光受体。
鉴于目前对于阳离子荧光识别传感器的报道比较多,而阴离子处于刚发展阶段,本文设计并合成以萘酰亚胺为荧光发色团、脲为识别基团的新型荧光化学传感器分子——N-{4-[6-硝基-1,3-二酮-1H-苯并[de]异喹啉-2(3H)-基]苯基}-N′-苯基脲(1)。以苊为原料,经硝化、氧化、缩合和取代反应合成了1(Scheme 1),其结构经1H NMR和IR表征。运用荧光滴定法测试了1对阴离子(F-, Cl-, Br-和I-)的识别能力。
1 实验部分
1.1 仪器与试剂
WRS-1A型数字熔点仪;UV 2300型紫外-可见吸收光谱仪;RF-540型荧光光谱仪;INOVA(600 MHz)型核磁共振仪(以DMSO-d6为溶剂,TMS为内标);PE-Spectrum ONE型红外光谱仪(KBr压片)。
无水乙醇,用氧化钙回流2 h后蒸馏备用;无水四氢呋喃,以无水氯化钙干燥5 h后压入新鲜钠丝,加入指示剂二苯甲酮,于80 ℃回流直至四氢呋喃变蓝,蒸出备用;苯胺,加入无水碳酸钠干燥24 h后减压备用;其余所用溶剂均为市售分析纯。
1.2 中间体的合成
(1) 5-硝基苊(2)的合成
在反应瓶中加入苊20.0 g(130 mmol)和冰醋酸120 mL,加热搅拌使苊溶解。冷却至室温,滴加浓硝酸9 mL(约10 min),反应2 h。倒入约700 mL水中,立即析出大量黄色固体,过滤,滤饼用无水乙醇重结晶得黄色针状晶体2 14 g,产率54%。
(2) 4-硝基-1,8-萘酐(3)的合成
在反应瓶中加入2 14.0 g(70 mmol)和冰醋酸160 mL,搅拌使其溶解;于80 ℃分四次(每间隔30 min加40 g)加入重铬酸钠160 g(610 mmol),反应3 h。倒入约500 mL水中,过滤,滤饼用水洗涤后用5%碳酸钠溶液250 mL煮沸,趁热过滤,滤液冷却后用盐酸调至pH 2,静置,过滤,滤饼用水洗至中性,干燥后于120 ℃真空干燥2 h得黄色固体3 13 g,产率76%, m.p.225 ℃~227 ℃(228 ℃~229 ℃[10])。
(3) 对苯二胺取代4-硝基-1,8-萘酐(4)的合成
在反应瓶中加入3 1.0 g(4.1 mmol),对苯二胺1.95 g(18 mmol)及无水乙醇100 mL,氮气保护,搅拌下回流反应约3 h。过滤,滤渣烘干,用无水乙醇重结晶两次得红褐色固体4 1.23 g,产率90%;1H NMRδ: 8.74(d,J=8.4 Hz, 1H, ArH), 8.62(m, 3H, ArH), 8.12(d,J=7.8 Hz, 1H, ArH), 6.98(d,J=8.4 Hz, 2H, PhH), 6.65(d,J=8.4 Hz, 2H, PhH), 5.31(s, 2H, NH2)。
1.3 目标化合物1的合成
在单口烧瓶加入4 0.5 g(1.5 mmol),无水四氢呋喃150 mL及催化剂吡啶5滴,搅拌下缓慢滴加三光气(10 mL)的THF溶液(c0.26 mol·L-1),常温反应2 h;加入新蒸苯胺2 mL,继续反应2 h。过滤,滤饼用乙醇(10 mL)洗涤,干燥得黄色固体1 510 mg,产率75%, m.p.>300 ℃;1H NMRδ: 8.88(d,J=8.4 Hz, 1H, ArH), 8.77(m, 2H, ArH), 8.64(m, 2H, ArH), 8.13(m, 2H, NH2), 7.60(d,J=9.0 Hz, 2H, PhH), 7.49(d,J=9.0 Hz, 2H, PhH), 7.30(m, 4H, PhH), 6.98(m, 1H, PhH); IRν: 3 370(NHCO), 1 709(C=O), 1 622, 1 594(C=C), 1 532, 1 352(NO2) cm-1。
2 结果与讨论
2.1 UV-Vis光谱
1[THF溶液,c(1)=1.0×10-5mol·L-1]和1与阴离子四丁基季铵盐{记为[1+X-]}的UV-Vis谱图见图1。由图1可见,只有加入20倍量的F-的溶液的最大吸收波长发生了红移(λmax=485 nm,溶液的颜色由无色变为粉红色);而空白和加入20倍量的Cl-, Br-及I-溶液的颜色没有明显的变化。红移产生的原因在于F-较其它阴离子具有较小的离子半径,能够与脲形成稳定的氢键;脲基作为阴离子的识别结合部位与F-结合后,增强了电子给体的供电子能力,氮原子上电子云密度增加也将促进电荷向萘环转移,使其吸收带进一步向长波长方向移动。而Cl-, Br-和I-虽是吸电子基团,但其吸电子能力未能达到使分子内电荷分离的程度,故没有明显的红移。由此可见1对F-具有选择性识别作用,能够用于裸眼识别。

λmax/nm图1 1和[1+X-]的UV-Vis谱图Figure 1 UV-Vis spectra of 1 and [1+X-]
2.2 荧光滴定光谱
1和[1+X-]的荧光滴定光谱见图2。由图2可见,只有[1+F-]溶液的荧光发射光谱曲线产生较大的变化,说明1在选用的阴离子中,仅对F-有较强的响应,即对F-有选择性识别作用。

λmax/nm图2 1和[1+X-]的荧光光谱图Figure 2 Fluorescence pectra of 1 and [1+X-]

λmax/nm图3 不同浓度F-存在时1的荧光光谱图Figure 3 Fluorescence spectra of 1 in different concentration F-
F-浓度对1识别的影响见图3。由图3可见,荧光最大发射波长(550 nm)下的发射峰强度随F-浓度的增加,荧光强度有明显的增强趋势,说明F-对1的荧光性能具有增强的作用。产生荧光明显增强的原因在于1分子结构中存在萘环和苯环,萘环和苯环本身都是平面刚性的结构,但是脲基的存在下导致萘环和苯环不能共平面,F-与脲基络合后,增加了络合物的平面性,使其荧光增强[11]。其他的卤素离子与脲基的结合能力比较弱,不能改变其结构的平面性,荧光几乎没有变化。
3 结论
设计并合成了以荧光性能优良的萘酰亚胺作为分子荧光基团,以及对阴离子具有较好识别能力的脲作为识别基团的荧光化学传感器分子——N-{4-[6-硝基-1,3-二酮-1H-苯并[de]异喹啉-2(3H)-基]苯基}-N′-苯基脲(1)。测试了1对F-, Cl-, Br-及I-的识别能力,结果表明,加入F-后吸收波长发生了红移,并且裸视可见;荧光滴定光谱表明,随着F-浓度的增大,荧光强度明显增强,而加入Cl-, Br-, I-无明显变化,说明其对F-具有较好的选择性识别能力。
[1] Li Jun-fen, Li Du-xin, Han Yu-ying,etal. Synthesis of 1-phenyl-3-biphenyl-5-(N-ethylcarbazole-3-yl)-2-pyrazoline and its use as DNA probe[J].Spectrochimica Acta Part A,2009:221-225.
[2] Altava B, Barbosa D S, Burguete M I,etal. Synthesis of new chiral imidazolium salts derived from amino acids:Their evaluation in chiral molecular recognition[J].Tetra Asym,2009,20(9):999-1003.
[3] Katayev E A, Kolesnikov G V, Sessler J L. Molecular recognition of pertechnetate and perrhenate[J].Chem Soc Rev,2009,38(6):1572-1586.
[4] Biavardi E, Favazza M, Motta A,etal. Molecular recognition on a cavitand-functionalized silicon surface[J].J Am Chem Soc,2009,131(21):7447-7455.
[5] Fan L J, Zhang Y, Murphy C B,etal. Fluorescent conjugated polymer molecular wire chemosensors for transition metal ion recognition and signaling[J].Coord Chem Rev,2009,253(2~3):410-422.
[6] Liu Y, Shi J, Guo D S. Novel permethylated beta-cyclodextrin derivatives appended with chromophores as efficient fluorescent sensors for the molecular recognition of bile salts[J].J Org Chem,2007,72:8227-8234.
[7] Devaraj S, Saravanakumar D, Kandaswamy M. Dual responsive chemosensors for anion and cation:Synthesis and studies of selective chemosensor for F-and Cu(Ⅱ) ions[J].Sensors & Actu. B-Chem,2009,136(1):13-19.
[8] Cao D X, Liu Z Q, Li G Z. A trivalent organoboron compound as one and two-photon fluorescent chemosensor for fluoride anion[J].Sensors & Actu,B-Chem,2008,133(2):489-492.
[9] Moon K S, Singh N, Lee G W,etal. Colorimetric anion chemosensor based on 2-aminobenzimidazole:Naked-eye detection of biologically important anions[J].Tetra,2007,63(37):9106-9111.
[10] 夏盛钦,李承志,吴振国,等. 1,8-萘酰亚胺类荧光染料的合成及其荧光性质的研究[J].湖南师范大学自然科学学报,2000,23(4):51-54.
[11] Xu G, Tarr MA. A novel fluoride sensor based on fluorescence enhancement[J].Chem Commun,2004:1050-1051.
