左旋盐酸精氨酸腹腔注射建立轻、重两种急性胰腺炎模型
2010-11-23许永春李兆申龚燕芳金晶
许永春 李兆申 龚燕芳 金晶
左旋盐酸精氨酸腹腔注射建立轻、重两种急性胰腺炎模型
许永春 李兆申 龚燕芳 金晶
急性胰腺炎(acute pancreatitis,AP)是发生于胰腺的炎症性疾病,建立合适的动物模型有助于其研究。目前较多采用逆行胆胰管注射法制备急性坏死性胰腺炎(ANP)模型和腹腔注射雨蛙素制备急性水肿性胰腺炎(AEP)模型。本文采用不同浓度的左旋盐酸精氨酸腹腔注射建立两种AP模型,现报告如下。
一、材料和方法
1.动物模型制备:健康雄性SD大鼠60只,体重200~250 g,清洁级,上海西普尔-必凯实验动物有限公司提供。按数字表法随机分为对照组、5%左旋盐酸精氨酸(5%精氨酸)组和15%精氨酸组,每组20只。左旋盐酸精氨酸,分析纯级,由上海华美生物工程公司提供。实验前大鼠禁食12 h,自由饮水。精氨酸组大鼠分两次腹腔注射5%或15%左旋盐酸精氨酸2.0 mg/g体重,间隔1 h。对照组腹腔注射等容积无菌生理盐水。注射后6、12、24 h自大鼠股静脉取血1 ml,分离血清,置-80℃冰箱保存。注射后24 h处死大鼠,取胰腺组织予10%中性甲醛固定。
2.观察指标:(1)观察大鼠24 h死亡率。(2)采用酶法(麦芽6糖)检测血淀粉酶;葡萄糖氧化酶法检测血糖;化学比色法检测血钙;酶法检测肌酐;速率法检测GTP。均按HITACHI 7600型全自动生化分析仪(日本)标准规程操作。(3)固定的胰腺标本常规包埋、制片、HE染色,由专业的病理医师阅片,每张切片观察20个视野,参考Schmidt等[1]的标准评分。
二、结果
1.死亡率:24 h后,对照组及5%精氨酸组大鼠无死亡,15%精氨酸组死亡6只,死亡率30%。
2.实验室检测指标的变化:5%精氨酸组、15%精氨酸组血淀粉酶均较对照组明显升高(P<0.01),其中5%精氨酸组升高程度相对较低。5%精氨酸组血糖、血钙、肌酐及GTP含量与对照组无显著差异;15%精氨酸组的血糖、肌酐及GTP含量随时间延长呈上升趋势,均较对照组显著升高(P<0.05或P<0.01),而血钙含量较对照组显著降低(P<0.05或P<0.01,表1)。
3.胰腺组织病理学改变:对照组胰腺外观正常,镜下未见异常改变。5%精氨酸组胰腺轻度肿胀;镜下见腺泡和导管基本正常,未见出血坏死,间质水肿明显,有少至中等量炎细胞浸润,水肿及炎细胞浸润分值分别为(1.48±0.39)、(1.53±0.41)分。15%精氨酸组大鼠胰腺明显肿胀,质硬,见片状黄色坏死灶,大网膜、肠系膜上见皂化斑,腹腔有中至大量血性腹水;镜下见胰腺组织大片出血、凝固性坏死及脂肪坏死,坏死区内大量中性白细胞和单核细胞浸润,血管破裂出血(图1),水肿、炎细胞浸润、出血以及坏死分值分别为(3.35±1.21)、(3.15±1.28)、(2.60±0.83)和(2.75±1.04)分,与5%精氨酸组比较均有显著差异(P值均<0.01)。
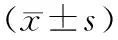
表1 各组大鼠血清淀粉酶、血糖、血钙、肌酐和GTP含量的变化
注:与对照组比较,aP<0.05,bP<0.01
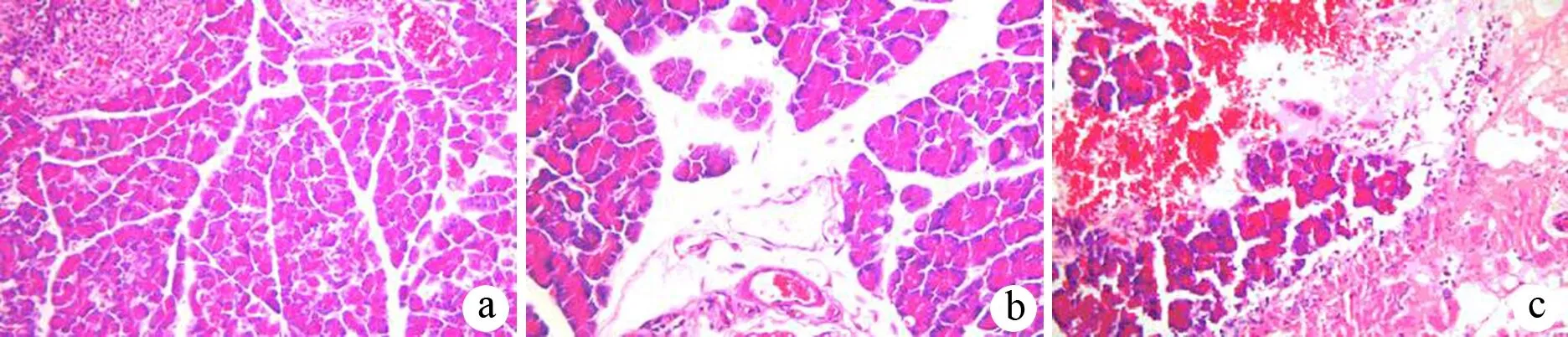
图1假手术组(a)、5%精氨酸组(b)、15%精氨酸组(c)胰腺组织病理改变(HE ×200)
讨论理想的AP动物模型应使其发病机制与人相似,重复性好,非侵入性,且简便、价廉,疾病进程、并发症、死亡率与人类AP相似,并具有同样的治疗反应[2]。现有的AP动物模型主要包括胰管结扎法、乙硫氨酸饮食法、逆行胰胆管注射法和促胰液分泌法(包括雨蛙素腹腔注射法),其中胆胰管注射法由Aho等[3]1980年首创,运用较为广泛,该模型较接近人类胰管梗阻、胆汁反流等病因形成的急性胰腺炎。这些动物模型尚无一种与人类AP发病过程完全一致,仅在某些方面有不同程度的相似性,因而根据不同的研究目的,选择相应的动物模型。
Tani等[4]首次报道腹腔内注射过量左旋盐酸精氨酸建立大鼠AP动物模型,其机制是大剂量左旋盐酸精氨酸抑制胰腺腺泡细胞核酸及蛋白质合成,诱导细胞凋亡和胰腺炎相关蛋白(pancreatitis-associated protein,PAP)基因的表达,从而抑制胰腺腺泡细胞增殖,损伤胰腺组织;此外,左旋盐酸精氨酸注射入动物体内后转化形成的NO以及氧自由基、细胞因子等也参与了胰腺的损伤[5-7]。本文结果显示,5%左旋精氨酸组仅能引起一过性血淀粉酶升高,无其他脏器功能改变,病理检查仅见胰腺组织水肿,炎细胞浸润,为AEP的病理表现。注射15%左旋精氨酸有一定的动物死亡率,血淀粉酶、血糖升高,血钙降低,肝、肾功能损害,病理检查见胰腺出血坏死,大量炎症细胞浸润,出现血性腹水,符合ANP的表现,与重症急性胰腺炎患者胰腺损伤及脏器功能障碍表现相似。
目前常用的十二指肠闭袢法和逆行性胆胰管注射法等AP建模方法需要对动物进行手术,操作复杂,损伤大;腹腔、静脉注射蛙皮素诱导的AP病变程度轻、费用高;胆碱乙硫胺酸(CDE)膳食诱导的AP死亡率过高,病理变化程度不一致;而本文采用不同浓度的左旋盐酸精氨酸大鼠腹腔内注射建立的轻、重两种AP模型,不用开腹操作,简单、省时,费用低廉,并且实验重复性好,结果可靠,适合AP发病机制和治疗学的研究。
[1] Schmidt J,Rattner DW,Lewandrowski K,et al.A better model of acute pancreatitis for evaluating therapy.Ann Surg,1992,215:44-56.
[2] Ulrich CD 2nd,Kopras E,Wu Y,et al.Hereditary pancreatitis:epidemiology,molecules,mutations,and models.J Lab Clin Med,2000,136:260-274.
[3] Aho HJ,Koskensalo SML,Nevalainen TJ.Experimental pancreatitis in the rat.Sodium taurocholate-induced acute hemorrhagic pancreatitis.Scane J Gastroenterol,1980,15:411-416.
[4] Tani S,Itoh H,Okabayashi Y,et al.New model of acute necrotizing pancreatitis induced by excessive dose of arginine in rats.Dig Dis Sci,1990,35:367-374.
[5] Rakonczay Z Jr,Hegyi P,Dósa S,et al.A new severe acute necrotizing pancreatitis model induced by L-ornithine in rats.Crit Care Med,2008,36:2117-2127.
[6] Paszt A,Eder K,Szabolcs A,et al.Effects of glucocorticoid agonist and antagonist on the pathogenesis of L-arginine-induced acute pancreatitis in rat.Pancreas,2008,36:369-376.
[7] Ishiwata T,Kudo M, Onda M,et al.Defined localization of nestin-expressing cells in L-arginine-induced acute pancreatitis.Pancreas,2006,32:360-368.
2010-03-12)
(本文编辑:吕芳萍)
10.3760/cma.j.issn.1674-1935.2010.06.025
全军医药卫生科研基金资助(08MA064)
200433 上海,第二军医大学附属长海医院消化科(许永春,现在江西省南昌市解放军第九四医院消化科)
李兆申,Email:zhsli@81890.net
