2008年美国FDA批准新药点评Δ
2010-11-22童荣生彭成叶松柏成都中医药大学药学院成都市60065四川省人民医院药剂科成都市60072四川大学华西基础医学与法医学院药理学教研室成都市6004
童荣生,彭成,叶松柏(.成都中医药大学药学院,成都市60065;2.四川省人民医院药剂科,成都市60072;.四川大学华西基础医学与法医学院药理学教研室,成都市 6004)
2008年美国FDA批准新药点评Δ
童荣生1,2*,彭成1,叶松柏3(1.成都中医药大学药学院,成都市610065;2.四川省人民医院药剂科,成都市610072;3.四川大学华西基础医学与法医学院药理学教研室,成都市 610041)
2008年美国食品与药品管理局(FDA)批准了21个新药物分子实体,而2005、2006、2007年则分别批准了20、17和15个,从批准的新药物分子实体数量上来看增加了,是2004年批准36个新药物分子实体以来新药物分子实体被批准的数量最多的一年[1]。本文主要根据2008年FDA批准新药报批资料及相关文献,对有创新意义、有重要作用机制、有重要临床意义的新药物分子实体摘要进行点评,以供读者参考。
1 2008年美国FDA批准的21个新药物分子实体和7个新生物制品[2]
2008年FDA批准的7个新生物制品和21个新药物分子实体,按照药物作用分类,精神系统药4个,镇痛药4个,诊断试剂3个,抗肿瘤药2个,抗病毒药2个,胃肠道药2个,血液系统药2个,泌尿系统药2个,其它药物7个,但是缺乏用于治疗冠状动脉病、心律失常、Alzheimer病(老年痴呆)、焦虑症、失眠、骨质疏松、哮喘和糖尿病的药物。7个新生物制品和21个新药物分子实体通用名、商品名及适应证详见表1、表2。
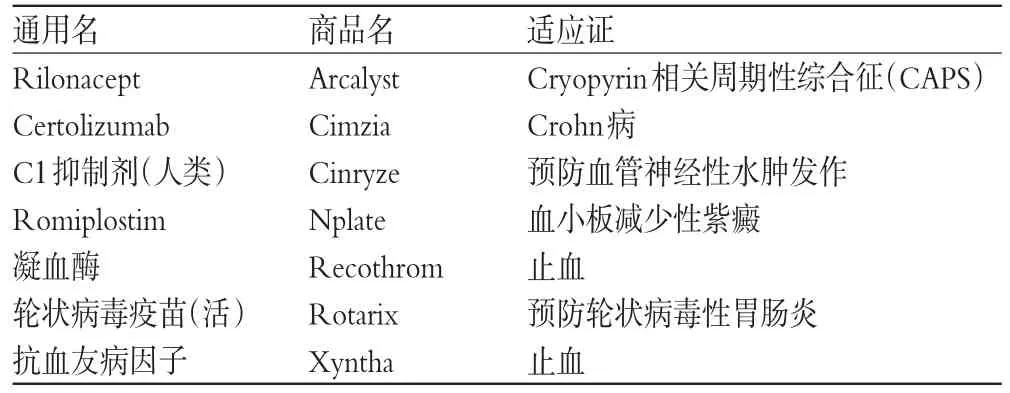
表1 2008年美国FDA批准的7个新生物制品及其适应证

表2 2008年美国FDA批准的21个新药分子实体及其适应证
2 主要新药的点评
以下介绍的所有新药的标注格式为:圆括号前为通用名(中文译名为暂用名,应以我国药品命名机构颁布的正式译名为准),圆括号内为商品名,方括号内为批准日期。
2.1 阿维莫泮Alvimopan(Entereg)[05/20/2008][3]
本品为阿片μ受体拮抗药(抑制常数Ki=0.4nmol·L-1),在多种标准药理测试中,未见其对受体的激动效应。在1~10μmol·L-1浓度下,对超过70种非阿片受体、酶和离子通道无影响。其在治疗剂量下不通过血脑屏障,因此能选择性和竞争性地与胃肠道μ受体结合,从而拮抗阿片类对胃肠道运动和分泌的外周作用而不影响阿片类的镇痛作用,也不会激发阿片类戒断症状。FDA批准其用于预防术后肠梗阻(Postoperative ileus,POI)。POI是造成腹部手术患者延迟出院的最常见原因。综合性因素如手术创伤、炎症、交感功能抑制、内源性物质释放(如内啡肽类)和阿片类镇痛药的应用等在POI发病中可能起着重要作用。从20世纪80年代开始,人们曾经试图用多种类型药物缓解或预防POI,但均未获成功,如促胃肠动力药甲氧氯普胺、胃动素(Motilin)受体激动药红霉素、β受体阻断药普萘洛尔、抗胆碱酯酶药新司的明等,甚至同样是外周阿片受体拮抗药甲基纳曲酮虽能缓解阿片类引起的便秘,但对POI仍无效。因此,可以认为,本品是目前唯一一个预防POI有效的药物。本品临床应用时应注意:(1)本品仅限在医院使用(住院患者);(2)用药不得超过7d(15个剂量,总量不得超过180mg);(3)本品禁用于连续应用阿片类药物超过7d的患者;(4)本品慎用于1周内应用超过3个治疗量的阿片类药物的患者,因其能增敏本品对胃肠道的作用,可致腹痛、腹泻、恶心、呕吐;(5)严重肝肾功能不良者不宜使用。但本品价格昂贵,据2008年美国市场价,1个疗程(7d,最大15个剂量)约需1125美元,故临床推广应用受到一定限制。
2.2 苯达莫司汀Bendamustine(Treanda)[03/20/2008][4]
本品早在20世纪60年代即由前东德研制成功,系由烷化剂与嘌呤类似物联结而成的合成杂交物,体现出一种合理的合成设计理念。它在欧洲已经应用30余年,美国FDA于2008年才批准其用于治疗慢性淋巴细胞白血病(CLL)与难治性B细胞非霍奇金淋巴瘤(NHL)。本品治疗CLL的总有效率(包括完全缓解率和部分缓解率)和无进展存活期分别为90%和18个月,而苯丁酸氮芥分别为38%和6个月,有非常显著的差别(P<0.0001)。但FDA认为,相对于一线治疗药,还不能确定本品效能不同于苯丁酸氮芥。不过,本品的批准上市至少为CLL患者提供了一种新的治疗选择。本品对利妥昔单抗治疗无效的NHL的总有效率为74%,有效持续时间为9.2个月,这是令人振奋的好消息,为这类患者带来了福音。因此,美国临床肿瘤学会(ASCO)将FDA对本品的批准认为“这是一项非同寻常的批准”,并且评为2008年癌症治疗12项重大进展之一。美国FDA还授予本品以孤儿药(Orphan drug)地位,这当然为开发厂商提供了多项优惠政策,但无疑也极大地促进对罕见病治疗药的开发。
2.3 地加瑞克Degarelix(Firmagon)[12/24/2008][5]
前列腺癌在欧美国家发病率高,仅次于或已超过肺癌,是男性癌症死亡的主要原因之一。据美国癌症协会估计,2008年美国约有186000例新发前列腺癌患者,约有200万人生活在前列腺癌威胁阴影之中。我国为前列腺癌低发地区,但近年来,其发生率明显增加,流行病学数据显示,我国前列腺癌发生率1993年为1.71/10万,2000年增加为4.55/10万,2005年更增加达到7.9/10万,而且以每年10%的速度攀升,因此,对前列腺癌的防治应予重视。多年来已知前列腺癌病因与睾丸酮产生过多有关,因此,去势治疗(手术去势和药物去势)是治疗前列腺癌的重要手段。自从黄体激素释放激素(LHRH)受体激动药亮比瑞林(Leuprolide)批准上市以来,药物去势已成为晚期前列腺癌首选治疗方法之一。但是,由于亮比瑞林是通过激动垂体LHRH受体,使之释放更多的LH,刺激睾丸产生更多的睾丸酮,最后才导致垂体反馈性停止释放促性腺激素而抑制睾丸酮产生。因此,亮比瑞林的一个明显缺点是用药第1日血中睾丸酮含量反而上升,至第3日最高,增加65%,第7日才降到用药前的基线水平(400ng·dL-1),然后血中睾丸酮含量才开始下降。亮比瑞林的这种一过性睾丸酮升高,可导致临床症状加剧,特别是有骨转移的前列腺癌患者,如骨痛、尿潴留、梗阻性肾功能衰竭、脊髓压迫以及高凝状态导致的致命性心血管事件等。因此,在用药前2周需同时加用抗雄激素药。而本品因通过拮抗垂体促性腺激素释放激素(GnRH)受体而抑制促性腺激素释放,从而直接抑制睾丸酮产生,所以,本品不会出现一过性睾丸酮升高,用药第1日,血中睾丸酮含量即可明显下降,并且迅速达到去势水平。因此,从这些方面比较,本品优于亮比瑞林,为晚期前列腺癌患者的治疗提供了新的选择,带来了福音。但是,目前本品用药频率为每月注射1次,应用较麻烦,而亮比瑞林新剂型不断被开发并获美国FDA批准,如1996年1月批准的肌肉注射1次22.5mg可维持3个月的混悬剂(Lupron Depot);1997年7月批准的肌肉注射1次30mg可维持4个月的混悬剂(Lupron Depot);2000年3月批准的可维持12个月的皮下植入剂型(Viadur),到期后还可置换。因此,本品新的长效剂型有望开发上市,以满足患者需要。
2.4 去甲文拉法辛Desvenlafaxine(Pristiq)[02/29/2008][6]
本品是文拉法辛(Venlafaxine)的活性代谢物,两者均能抑制5-羟色胺(5-HT)和去甲肾上腺素再摄取,为5-HT/去甲肾上腺素再摄取抑制剂(SNRIs),因而能提高突触间隙递质浓度,发挥抗抑郁作用。临床研究资料表明,加大剂量(>50mg·d-1)并不相应增加疗效,但不良反应增多。本品主要优点是用药简便,每日服药1次,且不需要进行剂量滴定,可以直接使用推荐剂量。由于本品是文拉法辛在体内经CYP2D6催化后产生的活性代谢产物,因此,本品治疗剂量与CYP2D6底物发生药物相互作用较少。但是,本品的抗抑郁疗效仅在门诊患者而且是短程治疗(8周)试验中得到验证,因此,长期用药的有效性和安全性还有待研究。本品临床应用时应注意:(1)对本品及文拉法辛过敏者禁用;(2)本品为控释片剂,因此,应完整吞服,禁止嚼碎或分割服用;(3)定时服药,如忘记服药,应及时当日补服,禁止次日服用2个剂量;(4)服药期间避免饮酒;(5)青光眼、高血压、高血脂、有惊厥发作史及易出血患者慎用;(6)突然停药可致停药症状(眩晕、恶心、头痛、失眠、焦虑、出汗等),应缓慢停药(延长给药间隔如每日1次改为隔日1次);(7)肾功能不良轻度及中度者(CrCl=30~80mL·min-1),剂量(50mg·d-1)不需调整,重度者(CrCl<30mL·min-1)或终末期肾病(ESRD)剂量需调整为每隔日50mg;(8)本品不宜用于儿童抑郁症;(9)由于本品抑制单胺递质摄取,如同时应用单胺氧化酶抑制剂(MAOIs),抑制单胺氧化,使递质作用增强,可导致严重反应(如血压剧烈升高等),因此,本品禁与MAOIs同时应用,可以在停用MAOIs 14d后应用本品,或者停用本品7d后应用MAOIs;(10)本品不宜与增强5-HT能神经活动的药物如5-HT摄取抑制剂(SSRIs、SNRIs)、5-HT受体激动药(如治疗偏头痛的曲坦类Triptans)、5-HT前体(色氨酸补充剂)等同时应用,因可致严重的5-HT综合征(幻觉、意识障碍、血压升高、心悸、体温升高、肌痉挛、反射亢进等)。如临床需要合用,则应严密观察,尤其在治疗开始和剂量增加时,但是,5-HT前体不推荐与本品合用。
2.5 艾曲波帕Eltrombopag(Promacta)[11/20/2008][7]
本品为血小板生成素(Thrombopoietin)受体非肽激动剂,通过结合并激动人类血小板生成素受体,激活细胞内信号转导途径,从而增加从骨髓祖细胞释放的巨核细胞的分裂与分化而增加血小板数目,但不会诱导血小板聚集和活化。临床口服仅用于有出血危险和对肾上腺皮质类固醇、免疫球蛋白或脾切除无明显疗效的慢性免疫性(特发性)血小板减少性紫癜(ITP)患者。本品的开发有两大特点,其一,本品是第1个口服治疗ITP药物;其二,治疗观念更新,由过去的减少和预防血小板破坏转变到增加血小板生成。因此,本品的开发成功被认为是ITP治疗的里程碑。FDA授予本品以孤儿药地位。但是,由于本品可致严重肝损害和其他如骨髓纤维化等风险,因此,本品目前只限于进入本品保健计划的患者使用。本品临床应用时应注意:(1)本品每日剂量不得超过75mg;(2)本品可致肝损害,因此,用药前及用药期间应密切监测肝功能,如丙氨酸氨基转移酶水平超过/等于其正常值上限3倍,并且是进行性的或持续≥4周,或有直接胆红素增加,或同时有肝损伤临床症状或肝代偿证据,应停药;(3)有报道,血小板生成素受体激动药可增加骨髓内网织纤维沉积,因此,本品应用期间应密切监测骨髓纤维化的外周血象变化,必要时骨髓涂片染色检查纤维化;(4)本品不得用于非ITP引起的血小板减少(如抗癌药等引起血小板减少)以企图恢复正常的血小板计数;(5)本品激动造血细胞表面血小板生成素受体,有可能增加发生白血病的危险,宜注意;(6)血小板大量增加可致血小板栓塞并发症,因此,如血小板计数≥200×109·L-1,应减量,如血小板计数>400×109·L-1,应停药。
2.6 依曲韦林Etravirine(Intelence)[01/18/2008][8]
本品为非核苷逆转录酶抑制剂(NNRTI),能与病毒逆转录酶结合,从而阻断RNA依赖的和DNA依赖的病毒DNA多聚酶活性,而不抑制人类DNA多聚酶活性。本品抗病毒活性并不需要在细胞内磷酸化。本品对野生型HIV-1实验室和临床分离株的抗病毒活性 EC50为0.9~5.5nmol·L-1(0.4~2.4ng·mL-1),在65株最常见的单氨基酸取代的HIV-1NNRTI耐药株中,有55株(85%)对本品仍然敏感。在2项随机双盲安慰剂对照的24周治疗试验中,全部病例均接受地瑞那韦/利托那韦(背景治疗)和2种其它抗逆转录病毒药加用或不加用恩夫韦地,在第24周治疗结束时,达到每毫升HIV-1RNA<400复制数者的百分率和平均增加的CD4+细胞计数,本品治疗组和安慰剂对照组分别为74%与81个·mm-3和51.5%与64个·mm-3。但是,本品最大特点是与其它NNRTIs较少产生交叉耐药性,被认为是本类药物的一个突破。因此,本品是目前唯一一个对NNRTIs产生耐药性的HIV-1感染成年患者治疗有效的NNRTI,为耐药性患者带来了福音。本品临床应用时应注意:(1)本品宜饭后即时服用,因空腹服用,明显影响吸收;(2)用药期间,如在6h内忘记服药,可补服,如已超过6h,不宜补服,更不宜将漏服药和下次药一并服用;(3)本品偶可致严重皮肤反应如多形性红斑和Stevens-Johnson综合征,因此,如出现进行性皮疹,应及时停药处理;(4)本品与其它NNRTIs如依法韦伦或奈韦拉平合用,会明显降低本品血浓度而影响疗效,因此,本品不宜与其它NNRTIs合用;(5)在未合用低剂量利托那韦作背景治疗时,本品不宜与蛋白酶抑制剂合用,因可致这些药物血液中的浓度改变。
2.7 磷丙泊酚钠Fospropofol(Lusedra)[12/12/2008][9]
本品为丙泊酚(Propofol)的前药,是一种新型镇静催眠药,作用类似丙泊酚,但时效有差别,决定于从前药释放的速率。本品在血中迅速和完全被碱性磷酸酶代谢为丙泊酚、甲醛和磷酸盐,1mmol·L-1磷丙泊酚钠二钠盐可产生1mmol·L-1丙泊酚,甲醛和磷酸盐血浓度可达内源性水平。健康成人静脉推注本品10mg·kg-1,平均在7min内进入明显镇静深睡状态(从大呼其名才有反应到疼痛刺激无反应)。它可能通过与γ-氨基丁酸A(GABAA)受体和甘氨酸受体相互作用,延缓通道关闭时间,从而产生镇静催眠麻醉作用,在对成年患者进行诊断或治疗操作过程时(如结肠镜检查、支气管镜检查等)作为麻醉监控性镇静,但仅限于麻醉专业人员使用。本品优点是其水溶性,克服了丙泊酚注射剂含脂质乳剂的缺点。本品为控制药品,尚有待美国联邦药品强制管理局(DEA)定级。
2.8 拉科酰胺Locasamide(Vimpat)[10/28/2008][10]
本品在作用机制上有新发现,除能选择性提高钠通道慢失活,还能与神经系统的表达产物脑衰蛋白反应介导体蛋白-2(Collapsin response mediator protein-2,CRMP-2)结合,对后者作用是其它抗癫痫药所没有的,可以认为,本品是一种新类型抗癫痫药。临床治疗试验表明,对于现有抗癫痫药难以控制的部分发作癫痫患者,在原有药物治疗基础上,加用本品,约40%病例发作频率减少50%以上,而安慰剂组仅约20%。因此,本品批准上市,为那些难治性部分发作癫痫患者带来了福音。本品还有其他优点:较少发生药物相互作用,短时不宜口服者可以静脉给药而不需调整剂量与给药间隔时间,对糖尿病性神经痛还有镇痛作用。但本品可延长P-R间期,故心脏传导障碍患者慎用。
2.9 甲基纳曲酮 Methylnaltrexone(Relistor)[04/24/2008][11]
本品早在20世纪80年代为寻找外周性阿片受体拮抗药而设计合成。它是第1个被加拿大、美国和欧盟批准的用于治疗阿片类引起便秘的药物。临床报道,由阿片类药物引起便秘的患者用本品后大部分在4h内出现轻泻反应,其中1/3在30min内见效。这对于不堪忍受阿片类镇痛药导致的便秘困扰的晚期癌症等患者无疑带来了福音。但是,本品并非对所有这类患者都有效,说明可能还有其他机制参与如阿片类的某些中枢作用。此外,与同样是外周性阿片受体拮抗药的阿维莫泮(Alvimopan)不同,本品对术后肠梗阻无效,说明可能不同肠段受体对药物敏感性有差异。最后,本品长期用药(>4个月)的安全性和疗效还有待临床评价。
2.10 普利沙福 Plerixafor(Mozobil)[12/15/2008][12,13]
本品是趋化因子受体-4(CXCR4)拮抗药,能阻断与其同源配体即基质细胞衍生因子-1α(SDF-1α)的结合。在导引人类造血干细胞(HSCs)进入并固定于骨髓成分中,CXCR4与SDF-1α发挥了重要作用,因此,阻断这种结合,就能有效驱动造血干细胞和祖细胞从骨髓进入外周血循环。本品最初是作为抗病毒药而研制的,极低浓度(1~10nmol·L-1)即可抑制HIV-1和HIV-2生长,而对宿主细胞即使浓度高达500μmol·L-1亦无毒,选择指数高达100000。但在进行Ⅰ期临床试验时,意外地发现,它能特异性增加外周血造血干细胞计数。从此,本品成为新分子实体中第1个干细胞驱动剂,为造血干细胞移植提供了重新构建造血系统可能,这对于某些血液系统肿瘤患者带来了福音。本品能有效驱动骨髓中造血干细胞进入外周血循环,为获取更多的干细胞用于自身移植提供了便利。在2项安慰剂对照临床试验中,其中一项298例非霍奇金淋巴瘤患者在≤ 4d的血细胞分离术(Apheresis)中,达到靶数量(≥5×106CD34+细胞数·kg-1)者的百分率,本品联用粒细胞集落刺激因子(G-CSF)组和安慰剂联用G-CSF组分别为59%和20%(P<0.001),达到靶数量的平均日数,本品为3d,对照组未评价;另一项302例多发性骨髓瘤患者在≤2d的血细胞分离术中,达到靶数量(≥6×106CD34+细胞数·kg-1)者的百分率与平均日数,本品联用G-CSF组和安慰剂联用G-CSF组分别为72%与1d和34%与4d,2组百分率有非常显著的差异(P<0.001)。FDA授予本品以孤儿药地位。本品临床应用时应注意:(1)白血病患者不宜应用,因可能出现驱动白血病细胞而污染血细胞分离产物;(2)因可致中性白细胞增多和血小板减少,因此,用药期间应监测血象;(3)有可能出现脾肿大(因骨髓外造血作用)和脾破裂可能,用药期间如出现左上腹痛或肩痛,应注意检查脾脏;(4)本品对大鼠有致畸作用(D类),孕妇忌用;(5)中度和重度肾功不良者(CrCl≤50mL·min-1)剂量需减少1/3,应为0.16mg·kg-1,最大剂量不得超过27mg·d-1;(6)剂量如超过推荐剂量0.24mg·kg-1,胃肠道反应、血管迷走神经反应、体位性低血压或晕厥发生率较高;(7)应按患者实际体质量计算剂量。
本品的开发公司Genzyme Corporation正在进行1项为期5年的追踪试验计划(包括患者死亡和现状如复发或无病存活),以评价本品的长期有效性和安全性,预计2014年提出第5个年度报告。
2.11 卢非酰胺 Rufinamide(Banzel)[11/14/2008][14]
Lennox-Gastaut综合征占小儿癫痫5%~10%,其临床表现主要特点为:多种发作形式并存(非典型失神发作、强直发作、强直-阵挛发作、强直-失张力发作、部分发作),常进行性加重,预后不良,药物难以控制。本品为三唑衍生物,化学结构完全不同于现有抗癫痫药,抗癫痫作用机制尚不明,皮质神经原培养试验证明,本品(≥1μmol·L-1)能显著延缓钠通道失活恢复时间,限制钠依赖性动作电位持久重复放电(EC50=3.8μmol·L-1)。本品对控制癫痫患者Lennox-Gastaut综合征发作有显著作用,在随机双盲对照治疗试验中,这些患者在背景治疗(1~3种抗癫痫药)下,加用本品治疗后,其总发作频率减少率、强直-失张力型发作减少率和发作严重程度显著改善率分别为32.7%、42.5%和53.4%,而安慰剂组分别为11.7%、1.4%(增加)和30.6%。FDA授予本品以孤儿药地位。本品临床应用时应注意:(1)本品可缩短QT间期,因此,家族性短QT综合征患者禁用。(2)有报道,本品治疗过程中出现多器官过敏反应(皮疹、荨麻疹、发热、面部水肿和严重肝炎等)病例,因此,过敏者禁用,治疗过程中如出现皮疹,应严密观察,必要时停药。(3)本品应在饭时服用,因食物能促进本品吸收。(4)与其它抗癫痫药相似,本品不宜突然停药,以免激发发作,如需停药,可每2日减量25%。(5)肾功能不良者无需调整剂量。(6)本品不推荐用于肝功能不良者。(7)羧酸酯酶参与本品代谢,因此,诱导或抑制此酶活性的药物,可能干扰本品代谢,从而影响血药浓度。(8)本品与卡马西平、苯妥英、扑痫酮或苯巴比妥合用,清除增加,血药浓度降低25%~46%(卡马西平使本品血药浓度降低19%~26%)。由于CYP酶不参与本品代谢,因此,此种相互作用显然不是由于CYP酶诱导的结果,而是另有其他尚不明了的因素参与。此外,本品可使卡马西平血药浓度降低7%~13%,苯巴比妥与苯妥英血药浓度分别增加8%~13%与7%~21%。(9)本品与丙戊酸钠合用,可使本品血药浓度增加达70%,因此,服用本品患者,加用丙戊酸钠时,应从小剂量开始,滴定出有效剂量;同样,服用丙戊酸钠患者,加用本品时,开始剂量应小于400mg。
2.12 丁苯那嗪 Tetrabenazine(Xenazine)[08/15/2008][15,16]
本品作用于基底神经节,通过抑制囊泡单胺转运体2(VMAT2)(Ki=100nmol·L-1),从而减少单胺类神经递质如多巴胺、5-HT和去甲肾上腺素摄取进入囊泡,导致囊泡内单胺递质储存耗竭,其作用类似利血平,但外周作用较少,作用维持时间亦较短。本品还抑制突触前多巴胺释放,也阻断中枢神经多巴胺受体,但对D2受体亲和力较弱(Ki=2100nmol·L-1)。本品对高动力性疾患包括亨廷顿(Huntington)病舞蹈症、偏侧抽颤症、老年性舞蹈症、痉挛、Gilles de la Tourette综合征和迟发性运动障碍等可获得症状改善。在对亨廷顿病舞蹈症的临床治疗试验中,本品治疗组与安慰剂对照组比较,其舞蹈分数改变分别为(-5.04±0.49)和(-1.52±0.67)(P<0.0001)。第12周时,治疗组有69%患者总舞蹈分数下降3分以上,达到临床显著疗效,而对照组只有23%达到类似效果。
亨廷顿病舞蹈症是一种遗传性大脑退行性变性疾病,由于患者大脑尾状核部分神经细胞变性死亡,导致患者智力、平衡能力、语言能力和情绪控制能力的衰退,表现为人格改变、心境不稳、言语不清和不自主的舞蹈样动作,通常于中年发病,在美国其发病率为1/10000,美国现有患者约30000余例,而在我国尚无有关流行病学资料报道,仅见散发性家族性发作病例。尽管本品在欧洲各国应用已有30余年,但在美国,这是由其FDA批准的第1个用于治疗亨廷顿病舞蹈症的药物,并授予其孤儿药地位。但是,本品的应用能增加患者发生抑郁症和自杀的风险;其引起的中枢不良反应有时难与疾病本身加重的表现区分;其个体反应又受到如代谢型等的影响;其还可使QT间期延长,因此,先天性长QT综合征患者、有心律失常病史或心动过缓患者以及低血钾、低血镁患者应避免应用,否则,可能导致出现致命性尖端扭转型室性心律失常;其与其它药物合用(如MAOIs、利血平、延长QT间期药物等)时更应注意避免发生药物相互作用。这些都是临床应用时需要关注的问题。
2.13 他喷多Tapentadol(Nucynta)[11/20/2008][17]
本品是25年来美国FDA批准的第1个口服的中枢性镇痛新药,其镇痛作用与曲马多(Tramadol)相似,但较后者更强。曲马多是含左旋与右旋异构体的消旋体,其激动μ受体与抑制去甲肾上腺素再摄取作用分别来自其不同异构体及其代谢物,而本品则是同一分子构型起作用,不经过中间代谢途径。2009年6月DEA审定本品为控制物资法规(1970)的Ⅱ类药(开发公司申请列为Ⅲ类药,未获同意)。本品临床应用时的注意事项除与其它阿片类镇痛药相似外,因其还有抑制单胺递质摄取作用,如同时应用MAOIs,抑制单胺氧化,使递质作用增强,可导致严重反应(如血压剧烈升高等),故本品禁与MAOIs同时应用,可以在停用MAOIs 14d后应用本品,或者停用本品7d后应用MAOIs;本品也不宜与增强5-HT能神经活动的药物如5-HT摄取抑制剂(SSRIs、SNRIs)、5-HT受体激动药(如治疗偏头痛的曲坦类药Triptans)、色氨酸补充剂等同时应用,因可致严重的5-HT综合征(幻觉、意识障碍、血压升高、心悸、体温升高、肌痉挛、反射亢进等)。本品对终末期关节退行性变进行关节置换术后的慢性疼痛的Ⅲ期临床治疗试验报告正在FDA评议中。
[1] Hughes B.2007FDA drug approvals:a year of flux[J].Nat Rev Drug Discov,2008,7(2):107.
[2] Wnn RL.FDA new drug approvals in 2008[J].Gen Dent,2009,57(4):300.
[3] Leslie JB.Alvimopan for the management of postoperative ileus[J].Ann Pharmacother,2005,39(9):1502.
[4] Aivado M,Schulte K,Henze L,et al.Bendamustine in the treatment of chronic lymphocytic leukemia:results and future perspectives[J].Semin Oncol,2002,29(4suppl 13):19.
[5] Van Poppel H,Tombal B,de la Rosette JJ,et al.Degarelix:a novel gonadotropin-releasing hormone(GnRH)receptor blocker-results from a 1-yr,multicentre,randomized,phase 2dosage-finding study in the treatment of prostate cancer[J].Eur Urol,2008,54(4):805.
[6] DeMartinis NA,Yeung PP,Entsuah R,et al.A doubleblind,placebo-controlled study of the efficacy and safety of desvenlafaxine succinate in the treatment of major depressive disorder[J].J Clin Psychiatry,2007,68(5):677.
[7] Bussel JB,Gregory C,Mansoor NS,et al.Eltrombopag for the treatment of chronic idiopathic thrombocytopenic purpura[J].N Engl J Med,2007,357(22):2237.
[8] Andries K,Azijn H,Thielemans T,et al.TMC125,a novel next-generation nonnucleoside reverse transcriptase inhibitor active against nonnucleoside reverse transcriptase inhibitor-resistant human immunodeficiency virus type 1[J].Antimicrob Agents Chemother,2004,48(12):4680.
[9] Fechner J.Pharmacokinetics and pharmacodynamics of GPI 15715or fospropofol(Aquavan injection)-a water-soluble propofol prodrug[J].Handbook Exp Pharmacol,2008,182:253.
[10] Ben-Menachem E,Biton V,Jatuzis D,et al.Efficacy and safety of oral lacosamide as adjunctive therapy in adults with partial-onset seizures[J].Epilepsia,2007,48(7):1308.
[11] Portenoy RK.Subcutaneous methylnaltrexone for the treatment of opioid-induced constipation in patients with advanced illness:a double-blind,randomized,parallel group,dose-rangeing study[J].J Pain Symptom Manage,2008,35(5):458.
[12] De Clercq E.The AMD3100story:the path to the discovery of a stem cell mobilizer(Mozobil)[J].Biochem Pharmacol,2009,77(11):1655.
[13] Liles WC,Broxmeyer HE,Rodger E,et al.Mobilization of hematopoietic progenitor cells in healthy volunteers by AMD3100,a CXCR4antagonist[J].Blood,2003,102(8):2728.
[14] Glauser T,Sachdeo R,Krauss G,et al.Rufinamide for generalized seizures associated with Lennox-Gastaut syndrome[J].Neurology,2008,70(21):1950.
[15] Morrow T.Gene therapy offers HD patients relief from some symptoms.Tetrabenazine inhibits the transport of a molecule called vesicular monoamine transporter type 2or VMAT2[J].Manag Care,2008,17(11):46.
[16] Paleacu D,Giladi N,Moore O,et al.Tetrabenazine treatment in movement disorders[J].Clin Neuropharmacol,2004,27(5):230.
[17] Thompson CA.Tapentadol approved as pain reliever[J].Am J Health Syst Pharm,2009,66(1):8.
R97
A
1001-0408(2010)17-1611-05
2009-11-25
2010-02-22)
