MCM-41 的化学修饰及其对Cu2+的吸附性能
2010-11-16柏珊珊岳秀丽戴志飞
柏珊珊,岳秀丽,马 放,戴志飞
(哈尔滨工业大学 城市水资源与水环境国家重点实验室,哈尔滨150090,bss12345@163.com)
目前,水体中重金属不断增加的趋势严重危害着人类健康.铅、镉、铜及其化合物因广泛应用于采矿、冶炼、电子、电镀、石油、肥料制造等行业,已成为污水中的重要污染源而备受关注[1].吸附法是去除废水中重金属的常用方法,其去除重金属离子的效果主要取决于吸附剂的性能.理想的吸附剂应具有适用范围广、吸附容量大、吸附时间短、再生性能好和价格低廉等特点.
有序介孔二氧化硅(孔径范围2 ~50 nm)具有比表面积高、孔道规整、孔径分布窄、易于引入功能化基团等特点,作为吸附剂引起了高度关注[2-3].然而,仅依靠介孔分子筛骨架,二氧化硅的性能还远不能满足实际应用的要求.因此,为了提高其吸附性能,介孔材料的功能化设计引起了人们的重视.
由于介孔分子筛孔道表面有大量具有化学反应活性的羟基,它可以与有机硅烷缩合.本文将通过两步化学反应依次用3-氨丙基三乙氧基硅烷和一溴代乙酸与全硅MCM-41 介孔分子筛反应,使其表面羧基化.由于分子筛表面的羧基可与Cu2+等过渡金属离子发生配位或螯合作用,从而大大提高选择性吸附效率.
1 实 验
1.1 全硅MCM-41 介孔分子筛的合成
合成步骤[4]为:将25 g 硅酸钠用30 ml 蒸馏水溶解.将6.4 g 十六烷基三甲基溴化铵(CTAB)加热溶解于20 mL 的蒸馏水中,冷却至室温后,将其与硅酸钠混合后搅拌10 min.用硫酸溶液(5 mol/L)调节混合物的pH 值至10,继续搅拌80 min,使溶液变为粘稠的白色凝胶状.然后装入100 mL 带有聚四氟乙烯内胆的不锈钢水热反应釜内,置于烘箱中,在130 ℃下晶化72 h,取出后冷却抽滤,洗涤至中性,然后在90℃下干燥过夜,将所得半成品置于马弗炉中,在550 ℃下焙烧5 h,即得到全硅MCM-41 介孔分子筛.
1.2 MCM-41 介孔分子筛的表面修饰
采用两步后嫁接法用3-氨丙基三甲氧基硅烷(APTES)和一溴代乙酸对介孔分子筛进行修饰:
(1)将1.0 g 煅烧过的MCM-41 分子筛在180 ℃下活化5 h 后,置于含50 mL 无水甲苯溶剂的烧瓶中,加入1 mL 氨丙基三乙氧基硅烷,在N2保护下,130 ℃回流搅拌反应48 h,冷却,过滤,同时分别用甲苯、乙醇、乙醚进行洗涤,得到氨基化的MCM-41,室温下干燥过夜.
(2)将1 g 一溴代乙酸溶于少量去离子水中,用1 mol/L Na2CO3将pH 值调至7.0 左右,加入0.5 g 氨基化的MCM-41 后,继续调节pH 值至7.4,再加入体积为此时液体2 ~3 倍的pH 为7.4的缓冲溶液,室温搅拌48 h,过滤,同时分别用去离子水、乙醇、乙醚进行洗涤,得到羧基化的MCM-41.
1.3 样品表征
扫描电镜采用FEI Quanta 200 型号仪器进行测定;红外光谱用傅里叶变换红外光谱仪(Varian 3100),采用KBr 压片法测定;接触角在光学接触角仪(CAM101)上测定.
1.4 羧基化的介孔分子筛对Cu2+的吸附
将羧基化介孔分子筛与Cu2+溶液混合振荡,达到吸附平衡后,用0.45 μm 滤膜过滤,吸取上清液,用ICP 测定吸附后溶液中Cu2+的质量分数,计算吸附量Q(mg/g).

式中:Q 为吸附量(mg/g);C0为溶液初始质量浓度(mg/L);Ce为溶液平衡质量浓度(mg/L);V 为溶液体积(L);m 为吸附剂投加量(g).
2 结果与讨论
2.1 扫描电镜
图1 为MCM-41 放大10000 倍下的SEM 图,由图1 可以看出所合成的MCM-41 呈现均匀的球状颗粒,粒径为200 ~300 nm.

图1 MCM-41 的SEM 图(10000 倍)
2.2 接触角
接触角是表征材料表面亲水性的一个重要指标.羧基修饰前后的介孔分子筛的接触角见表1.

表1 材料的接触角
由表1 可见,羧基化后的MCM-41 的接触角略大于羧基化前的MCM-41,但仍为亲水性物质.这是由于修饰前MCM-41 表面含有大量硅羟基,所以亲水性很强,当对其进行表面修饰后,有机官能团使其亲水性略为降低,因此接触角变大.这表明,有机基团已经成功修饰到MCM-41 的表面.
2.3 傅里叶红外光谱(FT-IR)
FT-IR 的检测结果如图2 所示.

图2 羧基化前后介孔分子筛的红外光谱
修饰前,798 cm-1和1 085 cm-1处的峰分别归属为Si-O-Si 的对称伸缩振动峰和非对称伸缩振动,1 639 cm-1和3 440 cm-1处为-OH 的振动吸收峰.羧基化后,在798 cm-1和1 639 cm-1附近的吸收峰强度明显增加.此外,还出现几个新的峰,2 929 cm-1处的峰可归属为-CH 的振动吸收,1 440 ~1 210 cm-1处为OC-OH 的伸缩振动吸收峰,955 cm-1处为OC-OH 的变形振动吸收峰[5],这说明羧基被成功嫁接到介孔分子筛MCM-41 的表面.
2.4 pH 值对吸附性能的影响
pH 值是重要的介质因素,不仅会影响吸附点解离,而且还会影响重金属离子的溶液化学水解,氧化还原反应和沉淀[1].本实验pH 值对吸附性能的影响见图3,由于pH 值为7 时,Cu2+开始沉淀,因此选择pH 值的范围为2 ~6.在同一温度下,介孔吸附剂对Cu2+的吸附能力随着pH 的上升明显增强,这表明pH 值对吸附Cu2+有很大的影响.在pH <4 时,吸附剂对Cu2+的吸附能力较弱;在pH >5 时,吸附剂对Cu2+的吸附能力较强;当pH 为6 时,吸附剂对Cu2+的吸附量最大.这是因为在pH 值很小的时候,溶液中存在大量的H+离子,使吸附剂表面的功能基团质子化,导致重金属离子并没有被充分吸附,所以吸附量相对较低.随着溶液的pH 值的升高,跟吸附剂表面官能团结合了的H+会发生离解,从而使重金属离子有效地被吸附,所以吸附量是随着pH 值的增大而增大的.因此,本实验选择最佳pH 值为6.
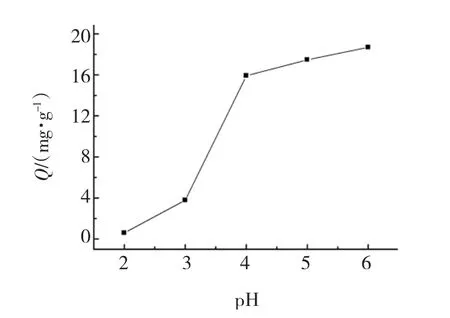
图3 吸附剂对Cu2+的吸附量随pH 值的变化
吸附过程中吸附剂表面的基团流失量可以通过检测吸附前后的溶液中的Si 的质量浓度来获得[6],见图4.当pH 值从2 变化到6 的过程中,吸附剂表面的基团流失量逐渐增加,通过对比NH2-MCM-41 和COOH-MCM-41 的基团流失量,可以看出投加NH2-MCM-41 的溶液中的Si 的释放量远远高于投加COOH-MCM-41 的溶液中的Si 的释放量,这是由于-NH2与Si-O-Si 键进行亲核攻击,从而使键断裂[6],可见,羧基比氨基更易保护吸附剂表面,减少表面基团流失.
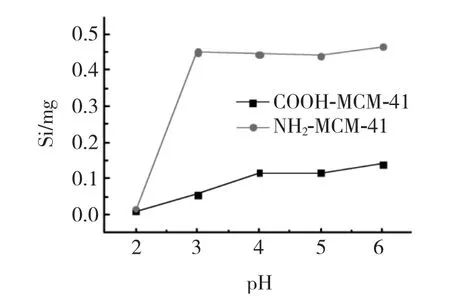
图4 释放到溶液中的Si 的量随pH 值的变化
2.5 吸附时间对吸附性能的影响
吸附时间是影响吸附效率的重要因素,溶液中的金属离子占据活性中心是一个渐进的过程,需要一定的时间来使吸附达到平衡,这段时间即所谓的吸附平衡时间.本实验吸附时间对吸附性能的影响见图5,可以看出,随着时间的推移,吸附剂对Cu2+的吸附量逐渐增加.振荡初始10 min内,吸附速度很快,吸附量大幅提高;40 min以后吸附逐渐趋于稳定并达到动态平衡.因此,本实验的平衡吸附时间为40 min.
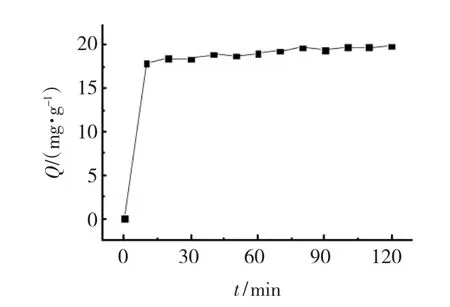
图5 吸附时间对吸附性能的影响
2.6 初始质量浓度对吸附效率的影响
初始质量浓度对吸附效率的影响见图6,介孔吸附剂对重金属离子的吸附效率随着重金属离子的初始质量浓度的增加而减少,当初始质量浓度<20 mg/L 时,吸附剂对Cu2+的去除率达到96%以上;当质量浓度为178.2 mg/L 时,去除率仅为41.67%.这主要是因为在重金属离子初始质量浓度较低时,同样投加量的吸附剂没有完全反应,吸附能力并没有充分发挥,因此其吸附量还没有达到吸附剂自身的饱和吸附值,随着重金属离子初始浓度的增大,吸附效率逐渐降低,重金属离子吸附量逐渐趋于饱和.
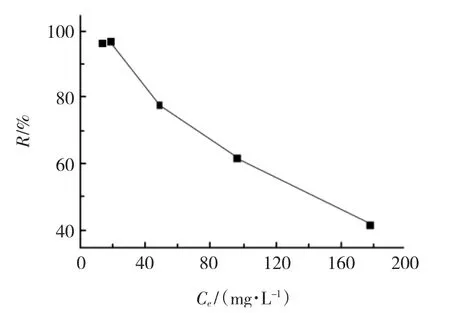
图6 初始质量浓度对吸附效率的影响
2.7 吸附等温线
吸附剂表面的吸附行为通常可以用Langmuir和Freundlich 吸附等温线来描述.Cu2+在25 ℃时的吸附等温线见图7.介孔吸附剂对重金属离子的吸附量随着重金属离子的平衡质量浓度的增加而递增,这个结果具有一定的普遍性[6-10].

图7 吸附等温线
将吸附等温线进行Langmuir 型和Freundlich型线性拟合.Langmuir 式为
(Ce/Qe)=1/(b*Qm)+Ce/Qm.
式中:Ce为平衡质量浓度(mg/L);b 为吸附平衡常数;Qe为平衡时吸附量(mg/g);Qm为饱和吸附量(mg/g).
Freundlich 式为
lnQe=lnK+(lnCe)/n.
式中:K 为表征吸附能力的常数;n 是表示吸附趋势大小的常数.
表2 为Langmuir 型和Freundlich 型拟合结果.Langmuir 型和Freundlich 型拟合的相关系数均达到0.95 以上,表明吸附剂对水中Cu2+的吸附既符合Langmuir 吸附等温方程又符合Freundlich 吸附等温方程.1/n 值为0.1 ~0.5 时,表明羧基功能化介孔分子筛对Cu2+的吸附比较容易进行,理论模型与实验结果相吻合.
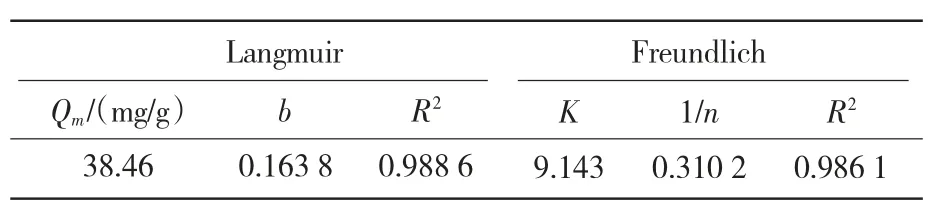
表2 Langmuir 和Freundlich 方程拟合羧基化MCM-41 对Cu2+的吸附参数
3 结 语
通过两步反应对介孔分子筛MCM-41 进行羧基化表面修饰.接触角和傅里叶红外光谱结果证明了羧基已经成功地修饰到介孔分子筛的表面上.羧基修饰后的介孔分子筛对水中的铜离子有很好的吸附效果,而且它比氨基修饰的分子筛更易保护吸附剂表面,减少表面基团流失,其吸附水中Cu2+的最佳pH 值为6,平衡吸附时间为40 min.它对铜离子的吸附符合Langmuir 和Freundlich 等温吸附方程.通过Langmuir 模型拟合得出吸附剂对Cu2+的最大吸附量为38.46 mg/g.
[1]张淑琴,童仕唐.活性炭对重金属离子铅镉铜的吸附研究[J].环境科学与管理,2009,33(4):91-94.
[2]LINSSEN T,CASSIERS K,COOL P,et al.Mesoporous templated silicates:an overview of their synthesis,catalytic activation and evaluation of the stability[J].Adv Colloid Interf Sci,2003,103(2):121-147.
[3]吴胜举,吴翠荣,李风亭.新型介孔吸附剂的制备及吸附性能[J].环境科学学报,2009,29 (9):189701904.
[4]陶涛.MCM-41 介孔分子筛的合成方法及催化性能研究[D].镇江:江苏大学,2006.
[5]PRETSCH E.波谱数据表:有机化合物的结构解析[M].荣国斌,译.上海:华东理工大学出版社,2002:290-291.
[6]EVELIINA R,TONNI A K,JOLANTA K W,et al.Removal of Co(II)and Ni(II)ions from contaminated water using silica gel functionalized with EDTA and/or DTPA as chelating agents[J].J Hazard Mater,2009,171(1-3):1071-1080.
[7]MIHAELA M,AURORA R,IOAN S,et al.Modified SBA-15 mesoporous silica for heavy metal ions remediation[J].Chemosphere,2008,73(9):1499-1504.
[8]BENHAMOU A,BAUDU M,DERRICHE Z,et al.Aqueous heavy metals removal on amine-functionalized Si-MCM-41 and Si-MCM-48[J].J Hazard Mater,2009,171(1-3):1001-1008.
[9]HEIDARI A,YOUNESI H,MEHRABAN Z.Removal of Ni(II),Cd(II),and Pb(II)from a ternary aqueous solution by amino functionalized mesoporous and nano mesoporous silica[J].Chem Eng J,2009,153(1-3):70-79.
[10]GORAN D,VUKOVIC′,ALEKSANDAR D,et al.Removal of cadmium from aqueous solutions by oxidized and ethylenediamine-functionalized multi-walled carbon nanotubes[J].Chem Eng J,2010,157(1):238-248.
