CuNaX催化乙苯选择氧化制苯乙酮
2010-11-09汤清虎赵培正赵培真
汤清虎,胡 钰,乔 冉,赵培正,赵培真
(河南师范大学 化学与环境科学学院,河南 新乡 453007)
CuNaX催化乙苯选择氧化制苯乙酮
汤清虎,胡 钰,乔 冉,赵培正,赵培真
(河南师范大学 化学与环境科学学院,河南 新乡 453007)
采用离子交换法制备了一系列不同铜含量的 CuNaX催化剂。该催化剂能有效催化以叔丁基过氧化氢 (TBHP)为氧化剂的液相乙苯选择氧化反应,产物以苯乙酮为主。在催化剂用量 200mg、乙苯用量 6mmol、TBHP用量 12mmol、乙腈用量 1mL、反应温度 80℃、反应时间 10h的优化反应条件下,乙苯转化率达到 78%,苯乙酮选择性为 98%,且催化剂能多次循环使用。XRD,DRS,H2-TPR表征结果表明,当铜质量分数小于 6.0%时,交换到NaX分子筛中的铜离子主要位于分子筛的超笼中;而当铜质量分数超过 6.0%时,交换到NaX分子筛中的铜离子主要位于分子筛的方钠石笼或六角柱笼中。位于NaX分子筛超笼中的六配位的铜离子是催化以 TBHP为氧化剂的乙苯选择氧化制苯乙酮反应的活性组分。
CuNaX催化剂;乙苯;苯乙酮;选择氧化;叔丁基过氧化氢
苯乙酮是有机合成的重要中间体[1~3],广泛应用于染料、香料、医药等工业。乙苯氧化制苯乙酮对石油化工下游产品的开发、精细化工的发展及饱和碳氢键选择氧化的理论研究都具有重要意义。目前,工业上主要采用乙苯空气直接氧化法制取苯乙酮[4],但该方法转化率低,选择性差,效益不好,有待改进。随着石油化工的发展,乙苯液相催化氧化制苯乙酮已成为十分活跃的课题。其中,以较清洁的过氧化物 (如叔丁基过氧化氢 (TBHP)和H2O2)、氧气或空气等为氧化剂的多相催化氧化是当前的研究热点[5~8]。
Chen等[9]报道了掺杂铬的磷酸铝催化剂能催化以 TBHP为氧化剂的乙苯选择氧化反应。负载型锰氧化物催化剂[10~12]对以 TBHP为氧化剂的乙苯选择氧化反应也具有一定的活性,但活性和选择性不够理想。最近,也有报道 Cu(Ⅱ)化合物催化剂[13~15]能用于催化以 TBHP为氧化剂的乙苯选择氧化制苯乙酮反应,且得到较高的苯乙酮收率。但该类催化剂大多是负载型 Cu(Ⅱ)配合物,反应过程中存在配体分解或活性组分脱落而使催化剂失活的问题[16,17]。
本工作通过一种简单有效的方法将铜导入N aX分子筛孔道中,制备了 CuN aX催化剂,考察了该催化剂对以 TBHP为氧化剂的乙苯选择氧化制苯乙酮反应的催化性能,并采用 XRD,DRS,TPR等方法对催化剂的结构和铜的存在状态进行了表征。
1 实验部分
1.1 催化剂的制备
称取一定量的氯化铜 (AR,天津市德恩化学试剂有限公司)溶解于 80mL去离子水中,再将 1.0g硅铝比为 1.3的 N aX分子筛 (A cro O rganics公司)加入到该溶液中,在室温下搅拌 4h,经过滤、洗涤后在 110℃下干燥,得到催化剂试样。在催化剂制备过程中,通过控制氯化铜溶液的浓度,可得到一系列不同铜含量的 CuN aX催化剂。含其他过渡金属的N aX分子筛催化剂均采用与 CuN aX催化剂类似的方法制备。
1.2 催化剂的表征
催化剂试样中铜含量的测定采用北京第二光学仪器厂W FX-1F2型原子吸收分光光度计,试样测定前用稀盐酸和少量的氢氟酸完全溶解。XRD表征在布鲁克 AXS公司 D8ADVANCE型 X射线衍射仪上进行,Cu Kα射线 (λ=0.150 64nm),管电压 40kV,管电流 40mA,扫描速率 1(°)/m in,扫描范围 2θ=5~70°。H2-TPR实验在装配有热导池检测器的流动系统中进行,称取 100m g试样置于石英反应管中,在 110℃的体积组成为 20%O2-80%N2的混合气流中处理 3h后切换成纯 N2,当反应管温度降至 50℃以下时,切换为体积组成为 5%H2-95%A r的混合气 (30mL/m in),待基线平稳后进行 H2-TPR测定,升温速率 8℃/m in。DRS表征在 V arian公司 Cary5000型近红外 -紫外 -可见分光光度计上进行,以BaSO4为参比,扫描范围λ=200~1 300nm。
1.3 催化剂的评价
乙苯选择氧化反应在带有回流冷凝管和磁力搅拌器的常压浴式反应器中进行。将 6mm ol乙苯(AR,国药集团上海化学试剂有限公司)、12mm ol TBHP(质量分数 70%,国药集团上海化学试剂有限公司)和 5mL乙腈 (AR,天津市化学试剂三厂)装入 25mL烧瓶中,再加入一定量的催化剂后在一定温度下反应。反应温度通过水浴控制,温度波动为±1℃。反应数小时后,将催化剂过滤,液体产物由装配有 DB-5毛细管色谱柱和 FID的 GC-920型气相色谱仪 (上海海欣色谱仪器有限公司)分析。
1.4 催化剂的循环使用
反应结束后,离心除去液体产物,回收催化剂,依次用丙酮 (AR,天津市德恩化学试剂有限公司)和去离子水洗涤,再于 110℃下干燥 12h后重复使用。
2 结果与讨论
2.1 催化剂的表征
2.1.1 铜含量的测定
CuN aX催化剂试样的铜含量见表 1。

表 1 CuNaX催化剂试样的铜含量Table1 Copper contents in CuNaX catalyst samples
当用于离子交换的 N aX分子筛的量和氯化铜溶液的体积一定时,试样的铜含量和离子交换度取决于氯化铜溶液的浓度。当用 2mm ol/L的氯化铜溶液 (80mL)与 1.0g的N aX分子筛进行离子交换时,所得试样的铜含量 (质量分数)为 0.9%,氯化铜溶液中的铜离子有 90%被交换到N aX分子筛中,离子交换度为 7%。随氯化铜溶液浓度的增加,试样中的铜含量和离子交换度随之增加,但氯化铜溶液中能交换到N aX分子筛中的铜离子的比例明显下降。当氯化铜溶液的浓度为 32mm ol/L时,试样中的铜含量为 10.4%,离子交换度达到 79%。进一步增加氯化铜溶液的浓度,试样的铜含量和离子交换度变化不大。可见,CuN aX催化剂试样的铜含量可通过改变氯化铜溶液的浓度加以控制。2.1.2 XRD表征
不同铜含量的CuN aX催化剂试样的 XRD谱图见图 1。由图 1可见,各试样的 XRD谱图中,除了N aX分子筛的衍射峰外,看不到任何归属于 CuOx晶相的衍射峰,说明通过离子交换法制备的催化剂试样中的铜处于离子状态。当试样中的铜含量超过 6.0%时,N aX分子筛衍射峰的强度逐渐降低。Sebastian等[18]报道,当钴离子的交换度大于 30%时,钴离子与N aX分子筛中的氧原子相互作用引起分子筛的结构变形,从而使 N aX分子筛的结晶度明显下降。因此,当交换到N aX分子筛中的铜离子较多时,衍射峰强度降低的原因可能是铜离子与 N aX分子筛骨架中的氧原子相互作用造成结构变形所致。

图 1 CuNaX催化剂试样的 XRD谱图Fig.1 XRD spectra of CuNaX catalyst samples.
2.1.3 H2-TPR表征
不同铜含量的 CuN aX催化剂试样的 H2-TPR曲线见图 2。由图 2可见,在所研究的温度范围(100~800℃)内,各试样均呈现两个较宽的还原峰,分别位于 290℃和 450℃附近 。Gentry等[19]研究表明,N aX分子筛中铜离子的还原与其在分子筛中的位置有关,位于 N aX分子筛超笼中的铜离子的还原温度明显低于方钠石笼和六角柱笼中的铜离子。因此,290℃附近的还原峰应归属于分子筛超笼中铜离子的还原,而 450℃附近的还原峰应归属于方钠石笼或六角柱笼中铜离子的还原。由图 2还可看出,当铜含量较低 (小于 6.0%)时,290℃附近的还原峰所占比例明显增大,说明交换到 N aX分子筛中的铜离子主要位于分子筛的超笼中。Kieger等[20,21]曾报道,当铜离子的交换度降低时,铜离子位于分子筛超笼中的比例远高于方钠石笼和六角柱笼。随铜含量的增加,450℃附近的还原峰所占的比例逐渐增大。当铜含量大于 6.0%时,在290℃附近的还原峰面积变化不大,而 450℃附近的还原峰面积却明显增加。为了更直观地说明铜离子在分子筛各笼中的分布情况,分别计算了各试样在290℃和 450℃附近还原峰面积的比值。当铜含量为 3.1%,6.0%,10.4%时,该比值分别为 2.05,1.43,1.17。这进一步说明,交换到 N aX分子筛中的铜离子优先占据 N aX分子筛超笼中的离子位,而后再占据方钠石笼或六角柱笼中的离子位。当铜含量较高时,位于 N aX分子筛超笼中可被交换的离子位已基本被全部占据,多余的铜离子只能被交换到方钠石笼或六角柱笼中的离子位上。

图 2 CuNaX催化剂试样的 H2-TPR曲线Fig.2 H2-TPR curves of CuNaX catalyst samples.
2.1.4 DRS表征
DRS表征能提供与铜离子配位相关的信息[15]。不同铜含量的 CuN aX催化剂试样的 DRS谱图见图 3。由图 3可见,各试样在 235nm处均呈现出一很强的吸收峰,该吸收峰归属于配位 O2-到中心 Cu2+的电荷迁移跃迁[22]。当铜含量较低 (小于 6.0%)时,在 800nm处可看到一很宽的吸收峰,该吸收峰归属于 N aX分子筛超笼中六配位的铜离子[Cu(H2O)6]2+的 d-d轨道跃迁[23]。该结果进一步证实,当铜含量或离子交换度较低时,交换到N aX分子筛中的铜离子主要存在于 N aX分子筛的超笼中。随铜含量或离子交换度的增加,该吸收峰逐渐向低波长方向移动。D elabie等[23]研究表明,位于方钠石笼或六角柱笼中的四配位铜离子在670nm附近呈现出特征吸收峰。因此,该位移应是交换到N aX分子筛中的铜离子进入方钠石笼或六角柱笼中,使铜离子的配位结构发生变化所引起的。
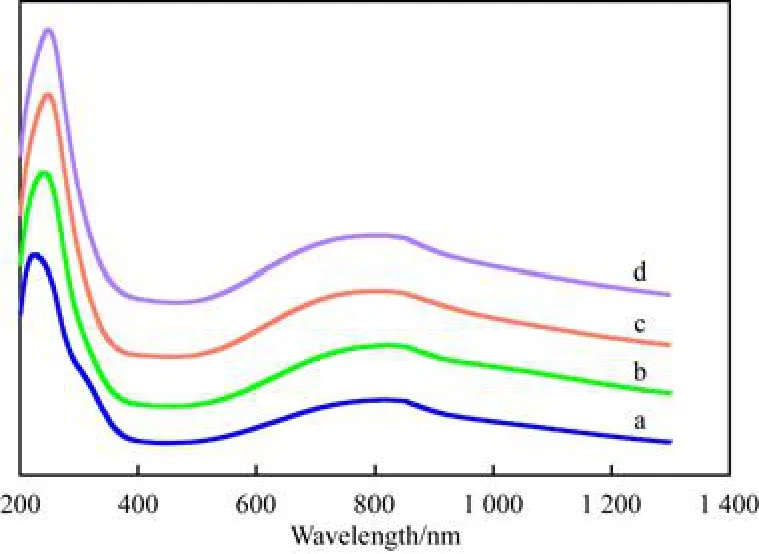
图 3 CuNaX催化剂试样的DRS谱图Fig.3 DRS patterns of CuNaX catalyst samples.
2.2 催化性能的评价
2.2.1 不同催化剂的催化性能
含不同过渡金属的 N aX分子筛催化剂对乙苯选择氧化反应的催化性能见表 2。

表 2 不同催化剂对乙苯选择氧化反应的催化性能Table2 Performances of different catalysts in selective oxidation of ethylbenzene
从表 2可看出,当过渡金属含量接近时,CuN aX催化剂具有最高的催化活性和较高的苯乙酮选择性,在 70℃下反应 10h,乙苯转化率达到 54.5%,苯乙酮选择性达到 91.8%。而含其他过渡金属的N aX分子筛催化剂上的乙苯转化率和苯乙酮选择性均较低 (CrN aX催化剂除外)。尽管 CrN aX催化剂具有最高的苯乙酮选择性 (98.8%),但其乙苯转化率远低于 CuN aX催化剂。以 CuC l2·2H2O和CuSO4·5H2O为铜源加入到反应液中的 Cu2+以及CuO也能催化乙苯选择氧化生成苯乙酮,但乙苯转化率均低于 CuN aX催化剂。由此可见,N aX分子筛中的铜物种对催化以 TBHP为氧化剂的乙苯选择氧化反应具有独特的催化性能。
2.2.2 铜含量对催化性能的影响
图 4是不同铜含量的 CuN aX催化剂对乙苯选择氧化反应的催化性能。由图 4可见,以不含铜的N aX分子筛为催化剂时,乙苯转化率仅为 5.5%;随铜含量的增加乙苯转化率提高,说明铜是催化乙苯选择氧化反应的活性组分。当铜含量较低 (小于1.6%)时,乙苯转化率随铜含量的增加提高幅度很大;当铜含量稍高时,乙苯转化率随铜含量的增加增幅趋缓;当铜含量大于 6.0%时,乙苯转化率随铜含量的增加变化不大。因此,适宜的铜含量为6.0%左右。
由 H2-TPR和 DRS表征结果可知,当铜含量较低 (小于 6.0%)时,交换到 N aX分子筛中的铜离子主要是位于分子筛超笼中的六配位的铜离子;而当铜离子含量超过 6.0%时,增加的铜离子主要以四面体配位的形式存在于分子筛的方钠石笼或六角柱笼中。考虑到方钠石笼和六角柱笼的窗口较小(0.22~0.26nm)[24],TBHP和乙苯由于窗口效应难以在方钠石笼和六角柱笼中的铜离子上发生反应。因此,认为位于 N aX分子筛超笼中的六配位的铜离子是催化 TBHP氧化乙苯反应的有效活性位。

2.2.3 反应条件的优化
为优化反应条件,在保持其他条件不变的情况下,考察了溶剂乙腈、反应物乙苯、催化剂用量和反应温度对 CuN aX催化剂催化乙苯选择氧化反应的 影响,实验结果见图 5。
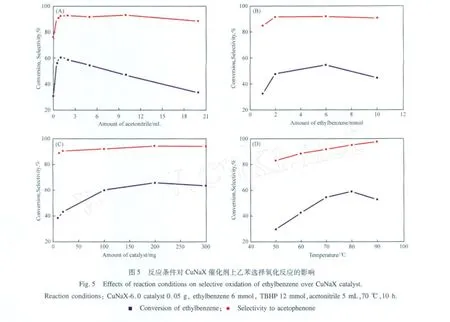
图 5(A)为溶剂乙腈用量对乙苯选择氧化反应的影响。由图 5(A)可看出,当乙腈用量由 0增至1mL时,乙苯转化率从 30%提高到 62%,苯乙酮选择性从 76%提高到 92%;继续增加乙腈用量,苯乙酮选择性变化不大,但乙苯转化率却明显降低,当乙腈用量为 20mL时,乙苯转化率仅为 33%。
图 5(B)为反应物乙苯用量对乙苯选择氧化反应的影响。由图 5(B)可看出,随乙苯用量的增加,乙苯转化率呈先增加后降低的趋势,当乙苯用量为6mm ol时,乙苯转化率达到最大值。乙苯用量对苯乙酮选择性的影响不大。
图 5(C)为催化剂用量对乙苯选择氧化反应的影响。由图 5(C)可看出,当催化剂用量从 25m g增至 200m g时,乙苯转化率从 45%提高到 66%,苯乙酮选择性从 88%提高到 94%;当催化剂用量从200m g增至 300m g时,苯乙酮选择性基本保持不变,但乙苯转化率降低。
图 5(D)为反应温度对乙苯选择氧化反应的影响。由图 5(D)可看出,当反应温度从 50℃升至80℃时,乙苯转化率从 29%提高到 59%,苯乙酮选择性从 83%提高到 95%。当反应温度升至 90℃时,苯乙酮选择性略有增加,但乙苯转化率却明显降低。这可能是由于 TBHP在较高温度下分解所致。
综上实验结果,优化的反应条件为:催化剂用量 200m g,乙苯用量 6mm ol,TBHP用量 12mm ol,乙腈用量 1mL,反应温度 80℃,反应时间 10h。
2.3 催化剂的循环使用性能
为考察 CuN aX催化剂的稳定性,对反应后除去固体催化剂的滤液进行了分析,未发现有铜离子存在,说明在反应过程中没有铜离子从催化剂上脱落。对经过多次循环使用的 CuN aX催化剂进行分析,也未发现其中的铜含量减少。
CuN aX催化剂的循环使用结果见图 6。由图 6可见,在优化的反应条件下,第一次使用时,乙苯转化率为 78%,苯乙酮选择性为 98%;第二次使用时,乙苯转化率 (74%)和苯乙铜选择性 (97%)均略有下降,这可能是由于 CuN aX催化剂在第一次使用过程中,有一小部分铜离子从分子筛的超笼迁移到方钠石笼和六角柱笼所致。在第二次使用后再次循环使用,乙苯转化率和苯乙酮选择性基本保持不变,表明 CuN aX催化剂在乙苯选择氧化反应中有较好的稳定性。

3 结论
(1)采用离子交换法制备的 CuN aX催化剂能够有效催化以 TBHP为氧化剂的乙苯选择氧化反应,产物以苯乙酮为主,且催化剂的性能稳定,可多次循环使用。
(2)H2-TPR和 DRS表征结果表明,当铜含量较低时,N aX分子筛中的铜离子主要以位于超笼中的六配位铜离子为主;而当铜离子含量超过 6.0%时,增加的铜离子主要以四面体配位形式存在于方钠石笼或六角柱笼中。位于 N aX分子筛超笼中的六配位铜离子是催化乙苯选择氧化反应的有效活性位。
(3)CuN aX-6.0催化剂上乙苯选择氧化反应的优化条件为:催化剂用量 200m g,乙苯用量6mm ol,TBHP用量 12mm ol,乙腈用量 1mL,反应温度 80℃,反应时间 10h。在此条件下,乙苯转化率为 78%,苯乙酮选择性为 98%。
(4)由于 N aX分子筛孔道的限制作用,采用TBHP为氧化剂时会存在一定的扩散阻力,但采用介孔分子筛催化剂有望解决该问题,进一步的研究还在进行中。使用 TBHP为氧化剂比 H2O2安全,且可以回收副产物叔丁醇,若能有效提高 TBHP的转化率和利用率,则该工艺有望实现工业化。
1 Tembe G L,Ganeshpure P A,Satish S.Oxidation of A lkanes by tert-Butyl Hydroperoxide Catalyzed by Polynuclear M anganese Schiff Base Complexes.J Mol Catal A:Chem,1997,121(1):17~23
2 A lcantara R,Canoira L,Joao P G,et al.Ethylbenzene Oxidation w ith A irCatalysed by B is(Acetylacetonate)N ickel(Ⅱ)and tetra-n-Butylammonium Tetrafluoroborate.Appl Catal,A,2000,203(2):259~268
3 M al N K,Ramaswamy V,Ganapathy S,et al.Synthesis of Tin-Silicalite M olecular Sieves w ith M EL Structure and Their Catalytic Activity in Oxidation Reactions.Appl Catal,A,1995,125(2):233~245
4 章思规.实用精细化学品手册 (有机卷·上册).北京:化学工业出版社,1996.34~35
5 李加其,郭军,尹笃林.乙苯催化氧化合成苯乙酮研究进展.精细化工中间体,2005,35(4):1~3
6 Choudhary V R,Indurkar J R,N arkhede V S,et al.M nO4-1Exchanged M g-A l Hydrotalcite:A Stable and Reusable/Environmental-Friendly Catalyst for Selective Oxidation by Oxygen of Ethylbenzene to Acetophenone and D ipheriylmethane to Benzophenone.J Catal,2004,227(1):257~261
7 许胜,闫修维,姚晔等.无溶剂法 Cu(Ⅱ)或 Fe(Ⅲ)盐催化氧化苯甲醇制备苯甲酸.石油化工,2009,38(2):193~196
8 李静霞,戴维林,曹勇等.选择氧化中新型 Keggin结构硅钨酸盐催化剂的研究进展.石油化工,2007,36(4):412~417
9 Chen Jidong,Haanepen M J,van Hooff J H C,et al.Redox M olecular-Sieves.8.Carpo-Catalyzed Oxidations of A lkylaromatics and A lcohols w ith TBHP in the L iquid-Phase.Stud Surf Sci Catal,1994,84:973~980
10 Kumar G S,Palanichamy M,Hartmann M,et al.Hydrothermal Incorporation of M anganese in the Framework of SBA-15.Catal Commun,2007,8(3):493~497
11 章艳,高保娇,王蕊欣等.固载 M nP-PGMA/SiO2催化剂的制备及其对乙苯氧化反应的催化性能.催化学报,2008,29(3):247~252
12 陈勇,李永生,李亮等.高分散的M nxOy/SBA-15的制备及其催化性能.催化学报,2009,30(3):230~234
13 Salavati-N iasari M. Host(N anocavity of Zeolite-Y)/Guest([Cu([R]2-N2X2)]2+(R=H,CH3;X=NH,O,S)Nanocomposite M aterials:Synthesis, Characterization and Catalytic Oxidation of Ethylbenzene.J Mol CatalA:Chem,2008,284(1~2):97~107
14 Zhu M ingxia,W ei Xin,L i Bodong,et al.Copper-Triethanolam ine Complex as Efficient and Active Catalyst for Selective Oxidation of A lkylarenes to Phenyl Ketones by tert-Butylhydroperoxide.Tetrahedron Lett,2007,48(52):9 108~9 111
15 Punniyamurthy T,Rout L.Recent Advances in Copper-Catalyzed Oxidation of O rganic Compounds.Coord Chem Rev,2008,252(1~2):134~154
16 孔德轮,高保娇,章艳等.硅胶固载聚 4-乙烯吡啶 -Cu(Ⅱ)配合物催化分子氧氧化乙苯的性能研究.分子催化,2007,21(6):579~584
17 Lahtinen P,Lankinen E,Leskela M,et al.Insight into Copper Oxidation Catalysts:Kinetics,Catalytic Active Species and Their Deactivation.Appl Catal,A,2005,295(2):177~184
18 Sebastian J,Jinka K M,Jasra R V,et al.Effect of A lkali and A lkaline Earth M etal Ions on the Catalytic Epoxidation of Styrene w ithM olecularOxygen Using Cobalt(Ⅱ)-Exchanged Zeolite X.J Catal,2006,224(2):208~218
19 Gentry S J,HurstN W,Jones A,et al.Temperature Programmed Reduction of Copper Ions in Zeolites.J Chem Soc,Faraday Trans 1,1979,75:1 688~1 699
20 Kieger S,Delahay G,Coq B,et al.Selective Catalytic Reduction of N itric Oxide by Ammonia over Cu-FAU Catalysts in Oxygen-Rich A tmosphere.J Catal,1999,183(2):267~280
21 Kieger S,Delahay G,Coq B,et al.Influence of Co-Cations in the Selective CatalyticReduction of NO by NH3over Copper Exchanged Faujasite Zeolites.Appl Catal,B,2000,25(1):1~9
22 Velu S,Suzuki K,OkazakiM,et al.Oxidative Steam Reform ing of M ethanol over CuZnA l(Zr)-Oxide Catalysts for the Selective Production of Hydrogen for Fuel Cells:Catalyst Characterization and Performance Evaluation.J Catal,2000,94(2):373~384
23 Delabie A,Pierloot K,GroothaertM H,et al.Study of the Coordination of Cu2+in Zeolite Y:Interaction w ith W ater and Ammonia.M icroporousMesoporouseMater,2000,37(1~2):209~222
24 Sherry H S.Ion-Exchange Properties of Zeolites I.Univalent Ion Exchange in Synthetic Faujasite.J Phys Chem,1966,70(4):1 158~1 168
Selective Oxidation of Ethylbenzene to Acetophenone over CuNaX Catalysts
Tang Q inghu,Hu Yu,Q iao Ran,Zhao Peizheng,Zhao Peizhen
(College of Chem istry and Environmental Science,Henan Normal University,Xinxiang Henan453007,China)
A series of CuN aX catalysts w ith different copper contents w ere prepared through ionexchange m ethod and used in selective oxidation of ethylbenzene w ith tert-butyl hydroperoxide(TBHP)to acetophenone in liquid phase.U nder the optim ized conditions:CuN aX-6.0catalyst dosage 200m g,ethylbenzene dosage6mm ol,TBHP dosage12mm ol,acetonitrile volum e1mL,reaction temperature80℃and reaction tim e10h,conversion of ethylbenzene and selectivity to acetophenone could reach78% and98%,respectively. The catalyst could be recycled for several tim es w ithout evident loss of the activity.The results of XRD,DRS and H2-TPR suggested that Cu ions w ere m ainly located in the N aX supercages w hen Cu m ass fraction w as low er than6.0%(w).But Cu ions w ould be exchanged into sodalite cages and/or hexagonal prism cages w hen the Cu m ass fraction w as higher than6.0%(w). The key active component for the selective oxidation w as the Cu ions in the supercages of N aX,w hich m ainly existed as six coordination Cu(Ⅱ).
CuNaX catalyst;ethylbenzene;acetophenone;selective oxidation;tert-butyl hydroperoxide
1000-8144(2010)07-0782-07
TQ426.8
A
2010-01-04;[修改稿日期 ]2010-05-04。
汤清虎(1970—),男,河南省新野县人,博士,副教授,电话 0373-3326544,电邮 qinghutang@sina.com.cn。
河南省高校科技创新人才支持计划项目(2010HASTIT028)。
(编辑 安 静 )
