新型含苯硼酸和喹啉的囊泡荧光多糖传感器的制备
2010-10-23李广全邵月君巨娟侠慕雪梅
李广全,谢 昕,邵月君,巨娟侠,慕雪梅
(中国石油兰州化工研究中心,甘肃兰州730060)
新型含苯硼酸和喹啉的囊泡荧光多糖传感器的制备
李广全*,谢 昕,邵月君,巨娟侠,慕雪梅
(中国石油兰州化工研究中心,甘肃兰州730060)
利用合成的含有识别基团苯硼酸和荧光读出基团喹啉的新型双亲化合物对硼酸苯甲基-8-十六烷氧基溴化喹啉(BHQB)在水中自组织成囊泡,囊泡的相变温度为52.4℃;当向囊泡体系加糖时,BHQB囊泡中的喹啉生色基在508 nm的荧光峰强度急剧减弱,425 nm处荧光逐渐增强.荧光强度变化可能归于所形成的硼酸酯改变了双亲化合物中硼原子的杂化轨道形式,进一步引起了整个分子内部的电子云排布所致.BHQB囊泡与糖的相互作用而导致体系荧光强度变化,并且这种变化的幅度与加入糖的种类和量均有关.因此体系有可能应用于检测生物物质如糖的化学传感器.
双亲化合物;传感器;囊泡;糖识别;荧光光谱
近年来,设计、合成用于检测生物物质的有效的荧光化学传感器已成为超分子化学领域极为活跃的研究课题[1].糖是维持生命活动的重要物质,是生物体内能量的传递物[2],因此,探讨新型选择性检测糖浓度的方法,受到人们的广泛关注[3-5].到目前为止,大量检测糖的方法已有报道,其中包括近红外光谱,电化学,比色,光旋转和荧光检测等[6-8].传统的血糖检测技术是生物酶法[9],但该方法存在很多弊端,人们的最大兴趣是发展连续跟踪葡萄糖浓度的体系及方法[10].由于化学传感器具有相对容易制备和稳定性较高的特点,目前有些公司已经进行相关的尝试[11].
根据Czarnik[12]和后来Shinkai[13]等人的工作,硼酸衍生物已被广泛用于识别含邻二醇结构的碳水化合物和邻苯二酚,并涌现了许多成功的范例[14].已知苯硼酸(PBA)基团与1,2-和1,3-二羟基化合物形成可逆硼酸酯,如葡萄糖等[15],James and Geddes等研究小组研发了多种含有苯硼酸和各种生色基组成的有机化合物作为糖的传感器[16-17].通过荧光强度的变化高效的检测了糖的浓度.为了发展基于连续检测的化学传感器器件,人们需要进行进一步的探索.如果将识别基团苯硼酸和荧光生色基同时引入双亲分子中,通过自组织作用,制备囊泡传感器,有可能实现可进入体内的连续检测血糖浓度的传感器.因此我们对具有较高的糖选择性和适度的亲合性荧光囊泡传感器非常感兴趣[18].
1 实验部分
1.1 试剂与仪器
所有的药品和溶剂均为分析纯:8-羟基喹啉,2,2-二偶氮异丁腈,N-溴代丁二酰亚胺购于Fluka公司.对甲基苯硼酸,1-溴代十六烷,1,3-丙二醇,无水乙醇,四氯化碳,1,4-二氧六环,二氯甲烷,氯仿,甲醇,乙腈,无水碳酸钾购于天泰化学试剂公司.水为二次去离子水.
核磁氢谱用Bruker Advance 500(500 MHz)型核磁共振仪测定,囊泡形态用JSM-6700F型场扫描电镜观测,荧光光谱用日本岛津RF-5301PC荧光光谱仪测定,囊泡的相变用Netzsch DSC 204差示扫描量热仪测定.元素分析由吉林大学分析测试中心测定.
1.2 实验过程
化合物对硼酸苯甲基-8-十六烷氧基溴化喹啉(简称BHQB)的制备过程如下:

1.3 BHQB囊泡的制备[19]
在10 mL容量瓶内,将0.058 4 g的双亲化合物BHQB溶于色谱级的氯仿,用高纯氮气吹干溶剂后用真空泵抽真空0.5 h.使其在容器壁上形成薄膜.向容量瓶中加入含有混合磷酸盐缓冲剂的去离子水,p H=7.4.用超声波超声震荡4 h,此时溶液的温度可达到50℃,将装有BHQB的容量瓶放入冰水之中冷却0.5 h后,室温放置.样品滴加在硅片上,真空干燥,待测扫描电镜.
2 结果与讨论
BHQB囊泡的形态由扫描电镜观测,典型的SEM([BHQB]=10μmol·L-1)如图1所示.由图1得出囊泡的直径约30~100 nm.差示扫描量热(DSC)测得凝胶态到液晶态的相变温度为52.4℃(见图2).实验结果表明,BHQB双亲化合物在水溶液中形成了囊泡[19-20].
荧光光谱的测定:把葡萄糖的磷酸缓冲溶液(p H=7.4)用可调微量进样器滴加到BHQB的磷酸缓冲溶液(p H=7.4)中,用干净的注射器将溶液混匀后静置10 s.用372 nm激发,囊泡溶液与各种不同浓度的葡萄糖体系的荧光光谱如图3所示.从图3可以看出,BHQB囊泡溶液在508 nm的荧光峰的强度随葡萄糖浓度从0到150 mmol·L-1的增大而急剧减弱,而425nm处荧光逐渐增强.产生这一变化的原因如图4所示,当体系中未加入葡萄糖时,囊泡中BHQB双亲化合物上的硼原子以sp2杂化形式为主,此时体现在荧光光谱中的508nm发射峰为主导,当向体系中逐渐加入葡萄糖形成硼酸酯后,硼原子变为sp3杂化形式,硼原子的电负性增加导致整个分子的电子云分布发生变化,此时体系中425 nm处的荧光发射峰出现并增强[21].

图1 BHQB囊泡的电镜照片Fig.1 SEM images of BHQB

图2 BHQB的DSC扫描曲线Fig.2 DSC thermogram of the BHQB vesicular solution
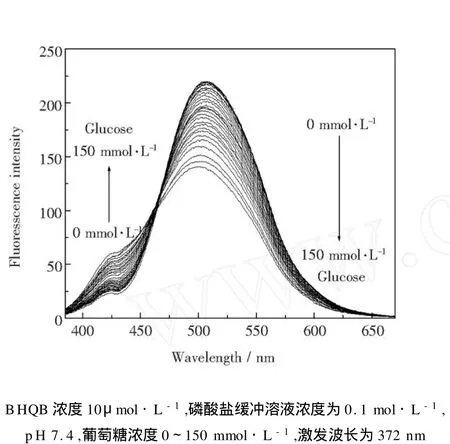
图3 BHQB囊泡溶液的荧光光谱Fig.3 Fluorescence spectra of BHQB vesicular solution

图4 BHQB囊泡与糖作用的示意图Fig.4 Illustration for molecular recognition process of the BHQB and surgar
为了研究BHQB囊泡传感器的选择性,用果糖代替葡萄糖进行相同的荧光测定得到图5,将图3和图5进行了比较.令I0为糖浓度为0时囊泡溶液的荧光光谱中425 nm处的荧光强度与508 nm处的荧光强度的比值,Ix为糖浓度为x时囊泡溶液的荧光光谱之中425 nm处的荧光强度与508 nm处的荧光强度的比值.以IX/I0为纵坐标,糖的浓度为横坐标,得到了随着糖浓度改变BHQB囊泡溶液荧光强度变化的曲线,详见图6.
通过图6可以直观的看出在糖的浓度相同时葡萄糖的变化大于果糖的变化,这在以往的文献中报道的单硼酸糖类检测器是不常见的.当体系之中的糖浓度为150 mmol·L-1时BHQB囊泡溶液体系下的IX/I0值与不加糖时比较葡萄糖变化了4.12倍,果糖变化了2.35倍.作为血糖检测器要求的葡萄糖变化范围一般小于1×10-2mol·L-1.在BHQB囊泡溶液中,当糖的浓度从0增加到1×10-2mol·L-1时,IX/I0值与不加葡萄糖时比较变化了1.58倍,果糖变化了1.38倍.同时血液之中的果糖的含量远远小于葡萄糖的含量,因此由于果糖的存在而引起的变化往往可以忽略不计.
3 结论
含有苯硼酸和喹啉生色基分别作为识别基团和荧光读出基团的新型双亲化合物,对硼酸苯甲基-8-十六烷氧基溴化喹啉在水中自组装成囊泡,囊泡的相变温度为52.4℃.当向囊泡体系加糖时,BHQB囊泡中的喹啉生色基在508 nm的荧光峰的强度急剧减弱,425nm处荧光峰逐渐增强.荧光强度变化可能是由于所形成的硼酸酯改变了BHQB双亲化合物电子云的分布所致.BHQB囊泡与糖相互作用而导致体系荧光强度变化还体现了一定的选择性,在相同操作条件下BHQB囊泡对葡萄糖作用的变化幅度大于果糖.使该体系有可能应用于检测生物物质如糖的化学传感器.

图5 BHQB囊泡溶液的荧光光谱Fig.5 Fluorescence spectra of BHQB vesicular solution
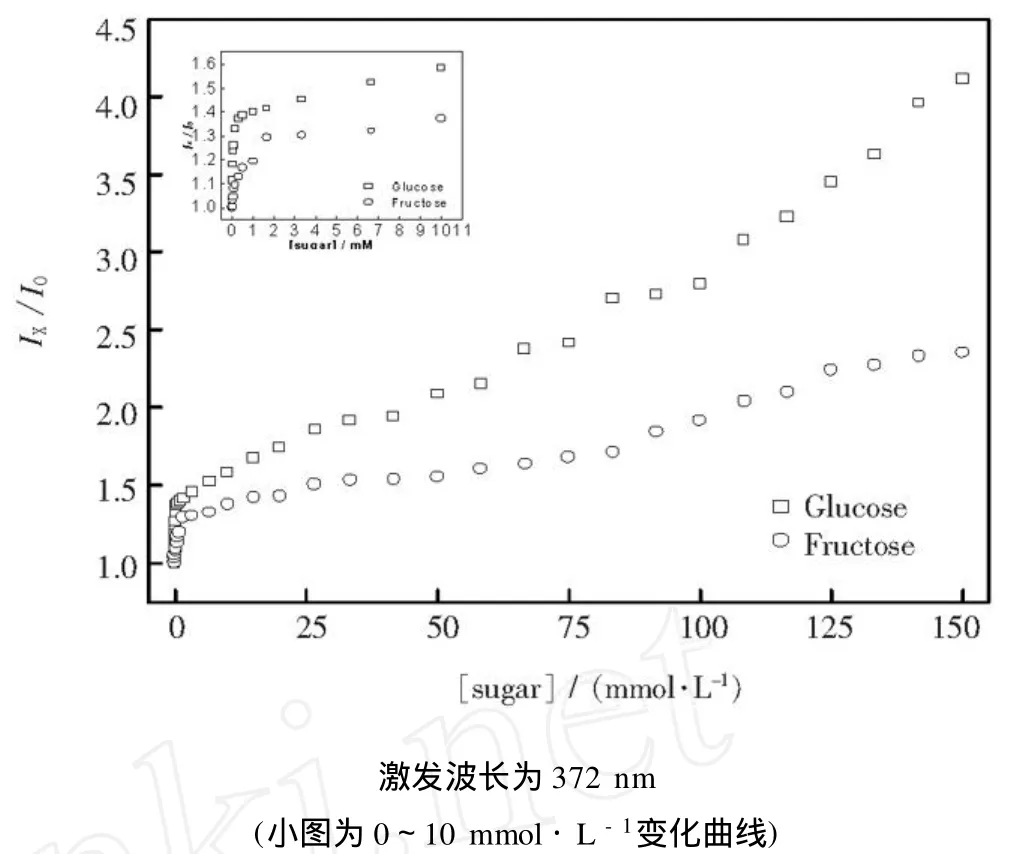
图6 BHQB囊泡溶液中加入不同浓度的糖时荧光光谱中IX/I0随糖浓度变化曲线Fig.6 Fluorescence intensity changes(IX/I0)as a function of surger concentration
[1]SesslerJ L,Camiolo S,Gale P A.Pyrrolic and polypyrrolic anion binding agents[J].Coord Chem Rev,2003,240:17-55.
[2]Hurtley S,Service R,Szuromi P.Cinderella’s coach is ready[J].Science,2001,291:2337-2337.
[3]James T D,Shinkai S.Artificial receptors as chemosensors for carbohydrates[J].Top Curr Chem,2002,218:159-200.
[4]Striegler S.Selective carbohydrate recognition by synthetic receptors in aqueous solution[J].Curr Org Chem,2003,7:81-102.
[5]Ni W,Fang H,Springsteen G,et al.The design of boronic acid spectroscopic reporter compounds by taking advantage of the pKa-lowering effect of diol-binding:Nitrophenol-based color reporters for diols[J].J Org Chem,2004,69:1999-2007.
[6]Robinson M R,Eaton R P,Haaland D M,et al.Non-invasive glucose monitoring in diabetic patients:a preliminary evaluation[J].Clin Chem,1992,38:1618-1622.
[7]Rabinovitch B,March W F,Adams R L.Measurement of very small optical rotations[J].Diabetes Care,1982,5:254-258.
[8]Schier G M,Moses R G,Gan I E T,et al.An evaluation and comparison of reflolux liand glucometer II,two new portable reflectance meters for capillary blood glucose determination[J].Diabetes Res Clin Pract,1988,4:177-181.
[9]Auria S D,Dicesare N,Gryczynski Z,et al.A thermophilic apo-glucose dehydrogenase as nonconsuming glucose sensor[J].Biochem Biophys Res Commun,2000,274:727-731.
[10]Gerritsen M,Jansen J A,Lutterman J A.Performance of subcutaneously implanted glucose sensors for continuous monitoring[J].Neth J Med,1999,54:167-179.
[11]Daniliff G Y.Continuous glucose monitoring:long-term implantable sensor approach[J].Diabetes Technol Ther,1999,(1):261-266.
[12]Yoon J,Czarnik A W.Fluorescent chemosensors of carbohydrates.A means of chemically communicating the binding of polyols in water based on chelation-enhanced quenching[J].J A m Chem Soc,1992,114:5874-5875.
[13]James T D,Shinkai S,Sadanayake K.Chiral discrination of monosaccharides using a fluorescent molecular sensor[J].N ature,1995,374:345-347.
[14]Robertson A,Shinkai S.Cooperative binding in selective sensors,catalysts and actuators[J].Coord Chem Rev,2000,205:157-199.
[15]Lorand J P,Edwards J O.Poltol complexes and structure of the benzeneboronate ion[J].J Org Chem,1959,24:769-774.
[16]Zhao J,Fyles T M,James T D.Chiral binol-bisboronic acid as fluorescence sensor for sugar acids[J].A ngew Chem Int Ed,2004,43:3461-3464.
[17]Ramachandram B,Joseph R L,Chris D G.Enhanced luminescence of phenyl-phenanthridine dye on aggregated small silver nanoparticles[J].Talanta,2005,66:569-574
[18]Wang Q S,Li G Q,Li G W,et al.Glucose-responsive vesicular sensor based on boronic acid glucose recognition in the ARS/PBA/DBBTAB covesicles[J].Sensors and Actuators B,2006,119:695-700.
[19]Moss R A,Okumura Y.Glucose responsive vesicular sensor based on boronic acid-glucose recognition in the ARS/PBA/DBBTAB covesicles[J].J A m Chem Soc,1992,114:1750-1756.
[20]Kunnitake T,Okahata Y.Formation of stable bilayer assemblies in dilute aqueous solution from ammonium amphiphiles with the diphenylazomethine segment[J].J A m Chem Soc,1980,102:549-553.
[21]Ramachandram B,Joseph R L,Chris D G.Wavelength-ratiometric and colorimetric probes for glucose determination[J].Dyes and Pigments,2006,68:159-163.
Preparation of the Fluorescent Vesicular Sensor Containing both Phenylboronic Acid and Quinolinium for Saccharide
A novel amphiphile containing two functional groups of both quinolinium and phenylboronic acid,N-(boronobenzyl)-8-hexadecyloxyquinolinium bromide(BHQB)was prepared.The amphiphile has self-organized into vesicles in the selective solution of water.TheTcof the vesicles from crystal to liquid crystal is 52.4℃.Addition of saccharide to the vesicular solution,the fluorescent intensities of quinolinium in BHQB vesicles centred at 425 nm increased and that at 508 nm decreased dramatically.The change of fluorescence intensity is ascribed to boronic ester formation which might change the boron atom hybrid orbital forms further causing the entire molecular electron cloud arrangement.The vesicular sensor through the interactions between boronic acid and saccharide displayed at a biomimetic membrane interface can be detected by means of fluorescence intensities.The results suggest that the fluorescent vesicles might be used as biosensors to determine saccharide.
amphiphile;sensor;vesicles;saccharide;fluorescence spectrum
O 657.3
A
1008-1011(2010)05-0058-05
2010-06-30.
李广全(1981-),男,工程师,博士,研究方向:生物检测器及树脂加工研究.E-mail:liguangquan@petrochina.com.cn.
