碧绿米仔兰叶的化学成分
2010-10-16张建辉杨淑敏谭昌恒
张 玲, 张建辉, 杨淑敏, 谭昌恒
(1.上海大学环境与化学工程学院,上海 200444;2.中国科学院上海药物研究所,上海 201203;3.首都医科大学化学生物学与药学院,北京 100069)
碧绿米仔兰叶的化学成分
张 玲1, 张建辉1, 杨淑敏2, 谭昌恒3
(1.上海大学环境与化学工程学院,上海 200444;2.中国科学院上海药物研究所,上海 201203;3.首都医科大学化学生物学与药学院,北京 100069)
采用硅胶、Sephadex LH-20柱层析等方法,对碧绿米仔兰 (Aglaia perviridis)的化学成分进行研究.从碧绿米仔兰叶的 95%乙醇提取物中分离得到 11个化合物,并通过1H-NMR,13C-NMR,MS等波谱技术鉴定了化合物的结构.
楝科;碧绿米仔兰;化学成分
Abstract:Column chromatographiesof silica gel and Sephadex LH-20 were used to isolate the chemical constituents of Aglaia perviridis.Eleven compoundswere isolated from the leavesof Aglaia perviridis,and their structures are identified on the basisof1H-NMR,13C-NMR and MS techniques.
Key words:meliaceae;Aglaia perviridis;chemical constituents
碧绿米仔兰 (Aglaia perviridis)系楝科(Meliaceae)米仔兰属 (Aglaia)植物,常绿乔木.米仔兰属植物主要分布于中国南部、印度和马来群岛以及太平洋岛地区,是印度和马来群岛热带雨林中的主要物种[1].米仔兰属的许多物种是传统的民间药物,如米仔兰 (Aglaia odorata),其叶味辛,微温,有活血散瘀、消肿止痛的功效,用于跌打、骨折、痈疮;其花味甘,性辛,有行气解郁的功能,用于气郁胸闷、食滞腹胀[2].东南亚部分地区 (如印度尼西亚)有将米仔兰属植物(如米仔兰)的花用做驱虫剂的传统.
国外对米仔兰属植物化学成分的研究较为广泛.结果表明,从该属植物中所分离得到的有机化合物主要涉及环戊四氢苯并呋喃、双酰胺、木质素、三萜、甾体、四降三萜等,其中环戊四氢苯并呋喃类化合物具有显著的杀虫作用和抗肿瘤作用[3-7].
虽然米仔兰为传统植物药,且米仔兰属植物中特有的 rocaglamide衍生物表现出显著的驱虫活性、抗肿瘤和抗炎活性,但在中药制备中却应用不足,国内也缺乏相关的基础研究.因而,对国内米仔兰属植物的化学成分及其生理活性成分进行研究是一项非常有意义的工作,可藉此发现具有药理活性的前体化合物用于药物研制,开发具有自主知识产权的新药或仿制药.
本研究对碧绿米仔兰 (采集于云南西双版纳)的化学成分进行分离,从其干燥叶子 95%乙醇提取物的氯仿部位和醋酸乙酯部位共分离获得 11个化学成分.运用波谱技术鉴定了该化学成分的结构,分别为 5,7,4′-三甲氧基双氢黄酮 (Ⅰ)、5,7,4′-三甲氧基黄芪苷 (Ⅱ)、5,7-二甲氧基 -4′-羟基双氢黄酮(Ⅲ)、胡椒碱 (Ⅳ)、尿嘧啶 (Ⅴ)、尿嘧啶核苷 (Ⅵ)、对甲氧基苯甲酸 (Ⅶ)、邻羟基对甲氧基苯甲酸(Ⅷ)、3,5-二甲氧基 -4-羟基苯甲酸 (Ⅸ)、对羟基苯甲酸 (Ⅹ)、β-胡萝卜苷 (Ⅺ).
化合物Ⅰ~Ⅺ的化学结构如图1所示.
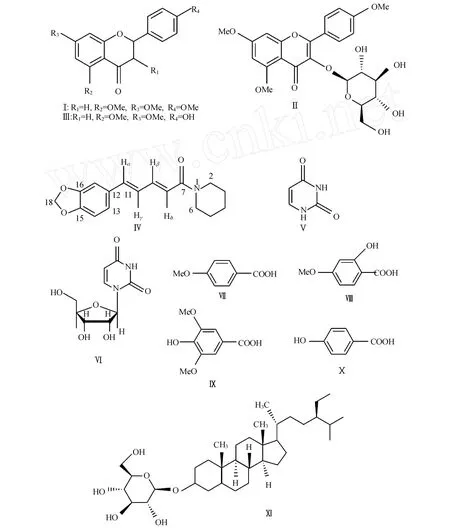
图1 化合物Ⅰ~Ⅺ的化学结构Fig.1 Chem ical structure of the compoundⅠ~Ⅺ
1 实验部分
1.1 仪器与试剂
Bruck AM-400核磁共振仪;MAT-95型质谱仪,LCQ-Deca型质谱仪,Q-Tof型质谱仪;200~300目硅胶;Sephadex LH-20葡聚糖凝胶.
实验用碧绿米仔兰干叶采集于云南西双版纳,由中科院西双版纳热带植物园崔景云老师鉴定.
1.2 提取与分离
自然风干的碧绿米仔兰叶 5 kg粉碎,用 95%乙醇溶液 20 L室温浸泡,提取 3次,时间分别为 4,4和3 h.合并提取液,减压浓缩后得粗浸膏.所得浸膏用水分散后,依次用石油醚、氯仿、乙酸乙酯、正丁醇各萃取 4次,浓缩,分别得石油醚部位、氯仿部位、乙酸乙酯部位和正丁醇部位.氯仿部位和乙酸乙酯部位经反复硅胶和 Sephadex LH-20柱层析得化合物Ⅰ~Ⅺ.
2 结果与讨论
分离所得化合物Ⅰ~Ⅺ的波谱数据结果如下.
化合物Ⅰ为无色晶体,MP为 124~126℃,分子式为 C18H20O5.1H-NMR(CDCl3,400 MHz)δ:7.39(2H,d,J=9.0 Hz,H-2′&6′),6.95(2H,d,J=9.0 Hz,H-3′&5′),6.14(1H,d,J=2.4 Hz,H-8),6.09(1H,d,J=2.4 Hz,H-6),5.36(1H,dd,J=12.9,2.1 Hz,H-2β),3.90,3.83,3.82(each 3H,s,3 OCH3),3.05(1H,dd,J=16.4,13.2 Hz,H-3α),2.77(1H,dd,J=16.4,3.0 Hz,H-3β).ESI-MS(positive)m/z:337[M+Na]+,651[2M+Na]+.以上数据与文献[8]数据基本一致,鉴定为 5,7,4′-三甲氧基双氢黄酮.
化合物Ⅱ为淡黄色晶体,MP为 212~214℃,分子式为 C24H26O11.1H-NMR (Me2CO-d6,400 MHz)δ:6.53(1H,d,J=2.3 Hz,H-8),6.80(1H,d,J=2.3 Hz,H-6),7.08(2H,dd,J=7.8,2.4 Hz,H-3′&5′),8.26(2H,dd,J=7.8,2.4 Hz,H-2′&6′),3.97,3.93,3.90(each 3H,s,3 OMe),5.0(1H,d,J=7.4 Hz,H-1″),3.2~3.7(6H,m,H-2″,3″,4″,5″,6″).ESI-MS(postive)m/z:491[M+H]+,513[M+Na]+,1003[2M+Na]+.以上数据与文献 [9]数据基本一致,鉴定为5,7,4′-三甲氧基黄芪苷.
化合物Ⅲ为淡黄色粉末,分子式为 C17H16O5.1H-NMR(CDCl3,400 MHz)δ:7.33(2H,d,J=8.4 Hz,H-2′&6′),7.12(2H,d,J=8.4 Hz,H-3′&5′),6.14(1H,d,J=2.2 Hz,H-6),6.09(1H,d,J=2.2 Hz,H-8),5.36(1H,dd,J=13.0,2.8,H-2),3.05(1H,dd,J=16.5,13.0,H-3α),2.77(1H,dd,J=16.5,2.8,H-3β),3.92,3.98(each 3H,s,2 OMe).ESI-MS:323[M+Na]+,623[2M+Na]+,299[M-H]-.以上数据与文献[10]数据基本一致,鉴定为 5,7-二甲氧基 -4′-羟基双氢黄酮.
化合物Ⅳ为无色晶体,分子式为 C17H19NO3,MP为 127~129℃.1H-NMR(CDCl3,400MHz)δ:7.40(1H,ddd,J=14.6,8.0,2.4 Hz,β-H),6.89(1H,dd,J =8.0,1.6 Hz,H-13),6.98(1H,d,J=1.6 Hz,H-17),6.78(1H,d,J=15.0 Hz,δ-H),6.78(1H,d,J=8.0 Hz,H-14),6.76(1H,dd,J=8.0,15.0 Hz,γ-H),6.44(1H,d,J=14.6 Hz,α-H),5.98(2H,s,CH2-18),3.64(2H,br.s,CH2-6),3.53(2H,br.s,CH2-2),1.70~1.55(6H,m,CH2-3,4,5).13C-NMR(CDCl3,100 MHz)δ:165.4(C-7),148.1(C-15&C-16),142.4(C-9),138.2(C-11),131.0(C-12),125.3(C-10),122.5(C-13),120.0(C-8),108.4(C-14),105.6(C-17),101.2(C-18),46.8(C-6),43.2(C-2),26.7(C-5),25.6(C-3),24.6(C-4).ESI-MS:m/z 286[M+H]+;308[M+Na]+;593[2M+Na]+.以上数据与文献[11]数据基本一致,鉴定为胡椒碱.
化合物Ⅴ为白色粉末,分子式为 C4H4N2O2.1H-NMR(DMSO-d6,400 MHz)δ:11.05(1H,br.s,H-NH),10.85(1H,br.s H-NH),7.40(1H,dd,J=7.5,5.8 Hz,H-6),5.46(1H,d,J=7.5 Hz,H-5).13C-NMR(DEPT)(DMSO,100MHz):δ 164.3(C-2),151.5(C-4),142.1(C-6),100.2(C-5).ESI-MS m/z:112(M+,100),69(50).以上数据与文献[12]数据基本一致,且与标准品混合后熔点不下降,TLC实验 Rf值一致,鉴定为尿嘧啶.
化合物Ⅵ为白色粉末,分子式为 C9H12N2O6.1H-NMR(CD3OD,400 MHz)δ:7.99(1H,d,J=7.8 Hz,H-5),5.81(1H,d,J=4.3 Hz,H-1′),5.68(1H,d,J=7.8 Hz,H-4),4.10(1H,dd,J=5.1,5.7 Hz,H-3′),4.06(1H,dd,J=4.2,5.4 Hz,H-2′),3.91(1H,m,H-4′),3.76(2H,m,CH2-5′).13C-NMR(CD3OD,100 MHz)δ:166.7(C-6),152.9(C-2),143.2(C-4),103.2(C-5),91.2(C-1′),86.8(C-4′),74.3(C-3′),71.7(C-2′),62.7(C-5′).ESI-MS m/z:267.0[M+Na]+,242.9[M-H]-,487.1[2M-H]-.以上数据与文献[13]数据基本一致,鉴定为尿嘧啶核苷.
化合物Ⅶ为白色针晶,MP为 165.7~168.7℃,分子式为 C8H8O3.1H-NMR(CDCl3,400 MHz)δ:7.92(2H,d,J=8.8 Hz,H-2&6),6.86(2H,d,J=8.8 Hz,H-3&5),3.89(3H,s,OCH3);ESIMS m/z:150.8[M-H]-.以上数据与文献 [14]数据基本一致,鉴定为对甲氧基苯甲酸.
化合物Ⅷ为无色晶体,MP为 211~213℃,分子式为 C8H8O4,1H-NMR(Me2CO-d6,400 MHz)δ:7.59(1H,dd,J=8.2,2.0 Hz,H-6),7.56(1H,d,J=2.0 Hz,H-2),6.92(1H,d,J=8.2 Hz,H-5),3.90(3H,s,H-OMe).ESI-MS m/z:180.9[M+H]+,526.8[3M+Na]+.以上数据与文献[15]中的数据基本一致,鉴定为邻羟基对甲氧基苯甲酸.
化合物Ⅸ为白色粉末,分子式为 C9H10O5.1HNMR(CDCl3,400 MHz)δ:3.95(6H,s,2 OMe),7.39(2H,s,H-2&6).13C-NMR (CDCl3,100 MHz)δ:56.4(2 OMe),107.2(C-2&6),146.7(C-3&5),171.6(COOH),140.0(C-4),120.1(C-1).ESI-MS m/z:196.9[M-H]-,417[2(MH+Na)-Na]-,637.9[3(M-H+Na)-Na]-.以上数据与文献[16]数据基本一致,鉴定为 3,5-二甲氧基-4-羟基苯甲酸.
化合物Ⅹ为白色粉末,分子式为 C7H6O3.1HNMR(CDCl3,400 MHz)δ:7.91(2H,d,J=8.6 Hz,H-2&3),6.92(2H,d,J=8.6 Hz,H-5&6).ESI-MS m/z:136.9[M-H]-1,297[2(M-H+Na)-Na]-1.以上数据与文献 [17]数据基本一致,鉴定为对羟基苯甲酸.
化合物Ⅺ为白色粉末,10%的硫酸乙醇溶液显紫红色斑点.与β-胡萝卜苷标准品 TLC实验 Rf值一致,且混合后熔点不下降,鉴定为β-胡萝卜苷.
[1] YANG SM,FU W W,WANG D X,et al.Two new p regnanes from Aglaia perviridis Hiern[J].JAsian Nat Prod Res,2008,10(5):459-462.
[2] ZHANG L,ZHANG J H,YANG SM,et al.Chemical constituents from the leaves of Aglaia perviridis[J].J A sian Nat Prod Res,2010,12(3):215-219.
[3] PROKSCH P,EDRADA R A,EBEL R,et al.Chemistry and biological activity of rocaglamide derivatives and related compounds in Aglaia species(Meliaceae)[J].Curr Org Chem,2001,5(9):923-938.
[4] NUGROHO B W,EDRADA R A,WRAY V,et al.An insecticidal rocaglamide derivatives and related compounds from Aglaia odorata (Meliaceae) [J].Phytochemistry,1999,51(3):367-376.
[5] OHSE T, OHBA S, YAMAMOTO T, et al.Cyclopentabenzofuran lignan protein synthesis inhibitors from Aglaia odorata[J].J Nat Prod,1996,59(7):650-652.
[6] JANPRASERT J,SATASOOK C,SUKUMALANAND P,et al.Rocaglamide,a natural benzofuran insecticide from Aglaia odorata[J].Phytochemistry,1993,32(1):67-69.
[7] ISHIBASHI F,SATASOOK C,ISMAN M B,et al.Insecticidal 1H-cyclopentatetrahydro[b]benzofurans from Aglaia odorata[J]. Phytochemistry,1993,32(2):307-310.
[8] 于德全,杨俊山.分析化学手册 (第七分册)[M].2版.北京:化学工业出版社,1999:822-825.
[9] UKUYAMA T,HOSOYAMA K,HIRAGA Y,et al.The constituentsof Osmunda(Ⅱ)a new flavonol glycoside of Osmunda asiatica[J].Chem Pharm Bull,1978,26(10):3071-3074.
[10] STEVENS J F,TAYLOR A W,NICKERSON GB,et al.Prenylflavonoid variation in Humulus lupulus:distribution and taxonomic significance of xanthogalenol and 4′-O-methylxanthohumol[J]. Phytochemistry,2000,53(7):759-775.
[11] DE ARAUJO-JUNIOR J X,DA-CUNHA EL,DE OM C,et al. Piperdardine,a p iperidine alkaloid from Piper tuberculatum[J].Phytochemistry,1997,44(3):559-561.
[12] 邹忠杰,杨俊山,鞠建华.泥胡菜的化学成分研究[J].中国中药杂志,2006,31(10):812-813.
[13] 宋妍,陈广通,孙博航,等.留兰香水溶性部分化学成分的分离鉴定[J].沈阳药科大学学报,2008,25(9):705-707.
[14] 康飞,吕华冲.广西白背叶植物叶的化学成分[J].广东药学院学报,2007,23(2):121-123.
[15] 任冬梅,娄红祥,季梅.岩青兰化学成分的研究 [J].中国药学杂志,2005,40(22):1695-1696.
[16] 郑万金,仲英,孙敬勇,等.瓦松的化学成分研究 [J].中草药,2009,40(6):859-862.
[17] 旷丽莎,江炜,侯爱君.水线草的化学成分研究 [J].中草药,2009,20(7):1020-1024.
(编辑:丁嘉羽)
Chem ical Constituents from the L eaves of Aglaia perviridis
ZHANGLing1, ZHANGJian-hui1, YANG Shu-min2, TAN Chang-heng3
(1.School of Environmental and Chemical Engineering,Shanghai University,Shanghai200444,China;2.Shanghai Institute of Materia Medica,Chinese Academy of Sciences,Shanghai201203,China;3.School of Chemical Biology and Pharmaceutical Sciences,Cap ital Medical University,Beijing 100069,China)
O 629
A
1007-2861(2010)05-0488-04
10.3969/j.issn.1007-2861.2010.05.008
2010-04-14
国家自然科学基金资助项目(20602037);上海市重点学科建设资助项目(S30109)
张 玲 (1974~),女,副教授,博士,研究方向为应用化学.E-mail:zhanglinglzu@staff.shu.edu.cn
