反相高效液相色谱法测定独活中蛇床子素与异欧前胡素的含量
2010-10-16邹继红娜日苏杨慧明刘青妍
邹继红,娜日苏,杨慧明,刘青妍
(赤峰学院 医学院,内蒙古 赤峰 024000)
反相高效液相色谱法测定独活中蛇床子素与异欧前胡素的含量
邹继红,娜日苏,杨慧明,刘青妍
(赤峰学院 医学院,内蒙古 赤峰 024000)
目的:建立测定独活中蛇床子素和异欧前胡素的高效液相色谱法.方法:采用Zorbax C18柱,乙腈-0.1%三乙胺水溶液(75:25)为流动相,流速为1mL·min-1,检测波长308 nm.结果:蛇床子素的线性范围为25.6~186.8mg·L-1,回归方程为Y=4.352×104X+1.062×102,r=0.9998,平均加样回收率为 98.2%,RSD=1.02%;异欧前胡素的线性范围为1.66~20.4mg·mL-1,回归方程为Y=5.736×102X+1.122,r=0.9999,平均加样回收率为98.8%,RSD=1.04%.结论:该方法简便、快速、准确,适用于独活中蛇床子素和异欧前胡素的质量控制.
反相高效液相色谱法;独活;蛇床子素;异欧前胡素;含量测定
独活为伞形科植物重齿当归的干燥根.性味辛、苦,微温.归肾、膀胱经.具有祛风,除湿,散寒,止痛之功效,是治疗风寒湿痹,腰膝酸痛,风湿性关节炎,风寒头痛等症的传统用药.独活中含有大量的蛇床子素和少量的异欧前胡素,本实验采用反相高效液相色谱法同时测定不同产地独活中的蛇床子素和异欧前胡素含量,通过比较不同产地独活的质量,为合理利用该药用植物资源及评价不同产地独活的质量提供依据.
1 仪器与试剂
Agilent 1200高效液相色谱仪(配置安捷伦色谱工作站),KQ-250E型超声波清洗器(昆山市超声仪器有限公司),METTLER AE240电子天平(瑞士梅特勒公司),TG332A型微量分析天平(上海仪器有限公司),PE-52AA型旋转蒸发仪(上海亚荣生化仪器厂),HH-2型恒温水浴锅(金坛市新航仪器厂),SHB-III型循环水式多用真空泵(河南太康教材仪器厂).
蛇床子素对照品和异欧前胡素对照品均购自中国药品生物制品检定所;甲醇为色谱纯(天津市康科德科技有限公司),实验用水为娃哈哈纯净水,冰醋酸、乙醚、乙酸乙酯和乙醇均为分析纯.
独活药材分别购自各地药材公司.
2 方法与结果
2.1 色谱条件
色谱柱:Zorbax C18色谱柱(4.6mm×250mm,5μm),柱温室温.流动相:乙腈-0.1%三乙胺水溶液(75:25),流速 1.0mL·min-1;检测波长 308nm,进样量20μL.
2.2 试验溶液的制备
2.2.1 蛇床子素对照品溶液
精密称取蛇床子素对照品10mg,置25ml容量瓶中,用甲醇溶解,并稀释至刻度,即得400mg·L-1的标准溶液.
2.2.2 异欧前胡素对照品溶液
精密称取异欧前胡素对照品3mg,置50ml容量瓶中,用甲醇溶解,并稀释至刻度,即得60mg·L-1的标准溶液.
2.2.3 混合对照品溶液
分别精密吸取5.0ml蛇床子素对照品溶液和异欧前胡素对照品溶液,置25ml容量瓶中,用甲醇稀释至刻度,即得混合对照品溶液.
2.2.4 样品溶液的制备
称取独活药材粉末约1.0g,精密称定,加6倍量体积的甲醇40℃水浴下提取2次,每次2h,合并提取液,减压回收溶剂,残渣用甲醇超声溶解转移至50mL的量瓶中,并定容至刻度,摇匀,经0.45μm微孔滤膜过滤,即得.
2.2.5 系统适用性试验
理论塔板数以蛇床子素和异欧前胡素计算均不低于24000,两物质的色谱峰之间及与相邻峰之间分离度均大于1.5,对称因子均在0.95~1.05之间.将对照品溶液和供试品溶液分别进样20μL,记录色谱图,对照品及样品色谱图见图1.
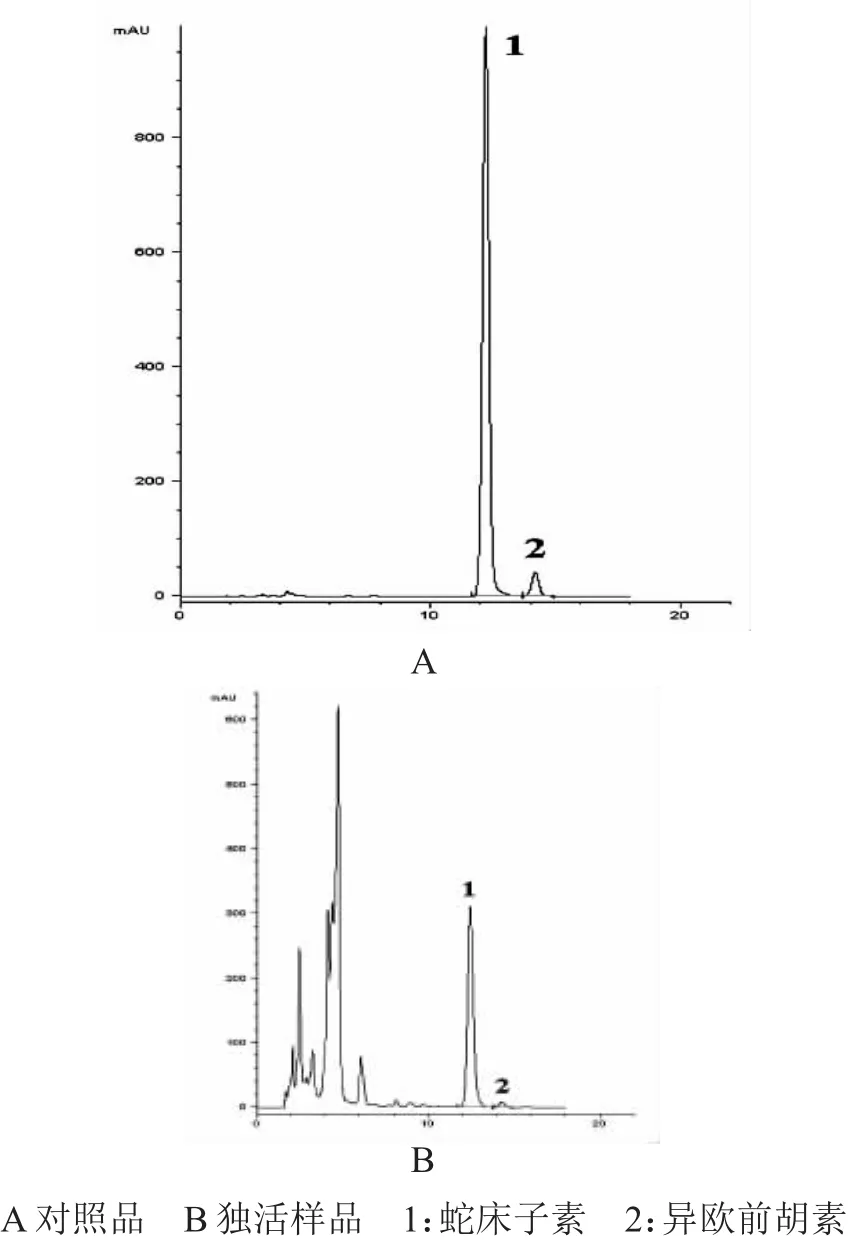
图1 高效液相色谱图
2.3 标准曲线的制备
分别精密吸取蛇床子素对照品溶液0.75,1.0,1.5,3.0,4.5mL置于 10mL量瓶中,以甲醇稀至刻度,各取20μL进样,以蛇床子素峰面积为纵坐标(Y),以蛇床子素浓度为横坐标(X)进行线性回归,回归方程为 Y=4.352×104X+1.062×102,r=0.9998.结果表明,蛇床子素的浓度在25.6~186.8mg·L-1范围内线性关系良好.
分别精密吸取异欧前胡素对照品溶液0.25,0.5,1.0,2.0,3.0mL置于 10mL量瓶中,以甲醇稀至刻度,各取20μL进样,以异欧前胡素峰面积为纵坐标(Y),以异欧前胡素浓度为横坐标(X)进行线性回归,回归方程为Y=5.736×102X+1.122,r=0.9999.结果表明,异欧前胡素的浓度在1.66~20.4mg·L-1范围内线性关系良好.
2.4 精密度试验
取1号药材样品粉末1.0g,精密称定,按样品溶液的制备方法制备成供试品溶液,按上述色谱条件重复进样6次,计算蛇床子素和异欧前胡素峰面积的相对标准偏差分别为0.92%和1.14%.
2.5 稳定性试验
取12号药材样品粉末1.0g,精密称定,按样品溶液的制备方法制备成供试品溶液,放置0,2,4,8,12,24h后,按上述色谱条件分别进样测定.结果表明,供试品溶液在24h内稳定性良好,蛇床子素和异欧前胡素峰面积的相对标准偏差分别为0.88%和0.97%.
2.6 重复性试验
取9号药材样品粉末6份,每份1.0g,精密称定,按样品溶液的制备方法制备成供试品溶液,按上述色谱条件分别进样,测得蛇床子素和异欧前胡素含量的相对标准偏差分别为1.28%和1.87%.
2.7 回收率试验
精密吸取已知含量独活药材(9号药材样品)粉末0.5g,分别加入一定量的蛇床子素和异欧前胡素对照品溶液,按供试品溶液制备方法制备成供试品溶液,按上述色谱条件分别测定.蛇床子素和异欧前胡素的回收率分别为98.2%和98.8%,RSD值分别为1.02%和1.04%.测定结果见表1~2.
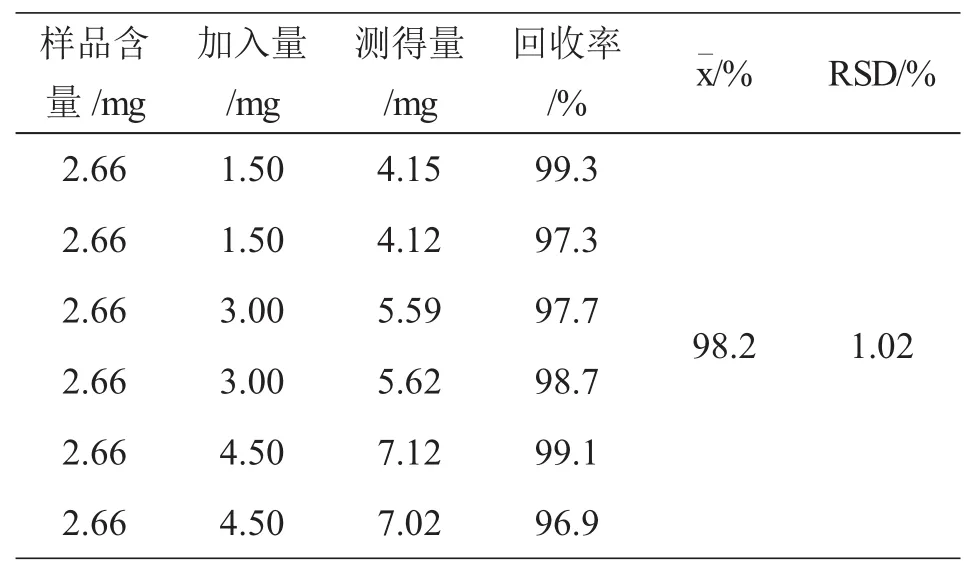
表1 蛇床子素回收率测定结果

表2 异欧前胡素回收率测定结果
2.8 样品的测定
称取各编号下独活药材粉末约1.0g,精密称定,按供试品溶液制备方法制备成供试品溶液,按上述色谱条件分别进样测定.测定结果见表3.
3 讨论
3.1 以分光光度计扫描蛇床子素和异欧前胡素对照品溶液,结果蛇床子素的的最大吸收波长为321nm,异欧前胡素的最大吸收波长为308nm,但独活中蛇床子素的含量较异欧前胡素大得多,为使异欧前胡素的测定灵敏度合乎要求,所以选择在308nm处测定.

表3 样品测定结果
3.2 在流动相选择的过程中,曾经尝试用乙腈-水和甲醇-水作为流动相,但蛇床子素和异欧前胡素的峰形不佳,故加入三乙胺进行调节,因此采用流动相为乙腈-0.1%三乙胺的水溶液=75:25,在此条件下,蛇床子素和异欧前胡素峰形对称,且能与其他组分得到良好分离.
3.3 曾经使用Kromasil C18柱测定,但组分保留时间太短,与前面的组分分不开,后改用Zorbax C18柱,保留时间适中,且能与其他组分得到良好分离.
3.4 样品的预处理,曾经采用甲醇、乙醇、乙酸乙酯和乙醚等溶剂分别进行提取,结果发现,甲醇回流提取所得异欧前胡素的含量最高,乙醇回流提取时所得蛇床子素含量最高,但独活药材中蛇床子素含量远远高于异欧前胡素,故本文选择以甲醇提取.
3.5 实验结果显示,不同产地的独活药材中蛇床子素和异欧前胡素含量差异显著.蛇床子素含量最高的为山西太原产独活,与其含量最低的湖北武昌产独活中蛇床子素的量相差四倍多;河南产独活中异欧前胡素含量却为这13个产地中最低的,与其含量最高的甘肃兰州产独活中的异欧前胡素含量相差更为悬殊,接近9倍.说明不同地域的气候、土壤等条件,可能极大的影响独活中各种化学成分的含量.
〔1〕贾敏如,王梦月,金曲嫫,等.HPLC 测定 13种白芷中欧前胡素和异欧前胡素的含量[J].华西药学杂志,2003,18(5):361-362.
〔2〕吴承云,郭力,董晓萍.HPLC测定寄生追风液中独活的有效成分蛇床子素 [J].华西药学杂志,2000,15(2):129-130.
〔3〕徐以亮,徐海波,李松.HPLC测定独活药材及配方颗粒中蛇床子素的含量 [J].中成药,2005,27(1):105-106.
〔4〕王洪志,李惠芬,周静,等.HPLC法测定元胡止痛片中欧前胡素和异欧前胡素 [J].中草药,2007,38(7):1018-1019.
〔5〕刘晓华,孙文基,李涛.HPLC法测定独活中蛇床子素的含量[J].药物分析杂志,2004,24(2):212-213.
〔6〕张娜,李云霞,孟宪生,等.高效液相色谱法测定羌活药材中异欧前胡素含量[J].辽宁中医杂志,2006,33(7):870-871.
〔7〕王书妍,谷学新,侯士果,等.HPLC 测定头风痛胶囊中欧前胡素和异欧前胡素的含量[J].药物分析杂志,2006,26(7):1011-1013.
〔8〕石钺,王卫华,杜力军.高效液相色谱法测定感冒一小时胶囊中异欧前胡素和蛇床子素的含量[J].中国中药杂志,2004,29(10):950-952.
R927.2
A
1673-260X(2010)02-0063-03
