氮杂氟硼荧(Aza-BODIPY)染料的研究进展
2010-09-21陈小利李翠红宋庆宝
陈小利 李翠红 宋庆宝
(浙江工业大学化学工程与材料学院,浙江 杭州310014)
氮杂氟硼荧(Aza-BODIPY)染料的研究进展
陈小利 李翠红 宋庆宝
(浙江工业大学化学工程与材料学院,浙江 杭州310014)
Aza-BODIPY荧光染料是一种新型荧光化合物,因其突出的优点而得到广泛地应用。从其应用的三方面(光动力学疗法的光敏剂、可控制的荧光传感器、近红外区域的荧光探针)详细描述了Aza-BODIPY荧光染料的研究进展,展望了该领域的研究发展方向。
氮杂氟硼荧(Aza-BODIPY);荧光染料;光敏剂;荧光传感器;荧光探针
Aza-BODIPY荧光染料是近十年才发展起来,并受到广泛重视的一种较新的荧光化合物。它有以下优点[1-5]:(1)Aza-BODIPY荧光染料的荧光光谱波长较长,一般在650~750 nm区间,接近于近红外区域,极大地促进了近红外荧光染料的发展。(2)Aza-BODIPY荧光染料具有相对较好的光稳定性。(3)Aza-BODIPY荧光染料的荧光光谱半峰宽较窄,作为荧光标识时有很好的灵敏度。(4)Aza-BODIPY荧光染料的荧光量子产率较高,通常在0.23~0.36区间。(5)Aza-BODIPY荧光染料的摩尔消光系数ε较大,一般在70,000~80,000 L·cm-1·mol-1。本文按其用途从三方面(光动力学疗法的光敏剂、可控制的荧光传感器、近红外区域的荧光探针)综述了Aza-BODIPY荧光染料的研究进展。
1 光动力学疗法的光敏剂
光动力学疗法(PDT)是一种非入侵的治疗癌症的方法,它基于光敏剂和与这种光敏剂吸收光谱相匹配的相应波长的光这两个因数[6-8]。当光敏剂注入人体并代谢一段时间后,在肿瘤组织中的浓度要比在正常组织中高,此时若用相应波长的激光照射患处 ,可对肿瘤组织进行靶破坏。目前,卟啉衍生物是临床上应用最普遍的PDT试剂,但是他们不是最理想的PDT试剂[9],因为其感光性和选择性还不够强。
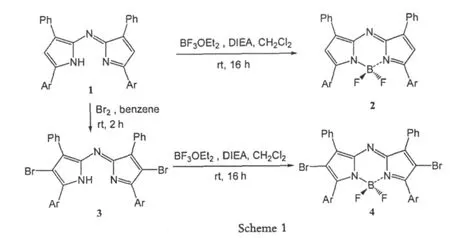
2002年,O'shea D F等人[1]报道了一种的新的PDT试剂,它是基于BF2与四芳基氮杂二吡咯甲川类化合物络合的产物,俗称Aza-BODIPY荧光染料(Scheme1)。四芳基氮杂二吡咯甲川类化合物1的合成首次报道于1943年[10],但是这一结构在其后50年来一直没被引起关注,直到O'shea D F等人报道了其与BF2络合的产物2,即Aza-BODIPY荧光染料,从此Aza-BODIPY荧光染料才开始被广泛研究。
Aza-BODIPY荧光染料作为PDT试剂,对于癌症的治疗具有极高的选择性,在没有光照射的区域,光敏剂是没有毒性的,只对受照射区域产生影响。在Aza-BODIPY荧光染料发色团中心β位置引入溴原子 4,是为了增加三重激发态的产生。三重态光敏剂与氧相互作用产生单态氧,这种单态氧被认为是PDT中的主要细胞毒素,它可造成细胞膜的不可逆损伤,使组织的脉管系统被破坏,细胞最后因得不到营养供给而死亡,最终靶组织被根除。
2004年,他们继续进行研究,首先对合成Aza-BODIPY荧光染料的条件进行优化,得出最佳反应条件。接着他们通过在Aza-BODIPY荧光染料发色团中心β位置引入溴原子研究其光物理性能,得出引入溴原子后,最大吸收波长变化不大,只产生轻微蓝移,而荧光量子产率却大幅度减少,其原因可能是当引入溴原子到荧光染料中心上,产生较强的重原子效应,导致荧光量子产率降低。同时他们研究了溶剂对Aza-BODIPY荧光染料的影响,得出不同溶剂(甲苯、氯仿、乙醇)对aza-BODIPY荧光染料的荧光光谱波长基本没影响[2]。
2005年,O'shea D F等人[3]报道了一类新的Aza-BODIPY荧光染料(Scheme 2)。当这类染料用作PDT试剂时,可通过调节pH值实现控制其选择性。通过光诱导电子转移机理,未被质子化的氨基受体使光敏剂的激发态快速达到平衡,没有发生能量的转移从而抑制了细胞毒素试剂(单态氧)的产生,最终不能杀死细胞。相反地,当氨基受体被质子化时,光诱导电子转移停止,发生能量的转移,产生细胞毒素试剂(单态氧),从而杀死细胞。

2 可控制的荧光传感器
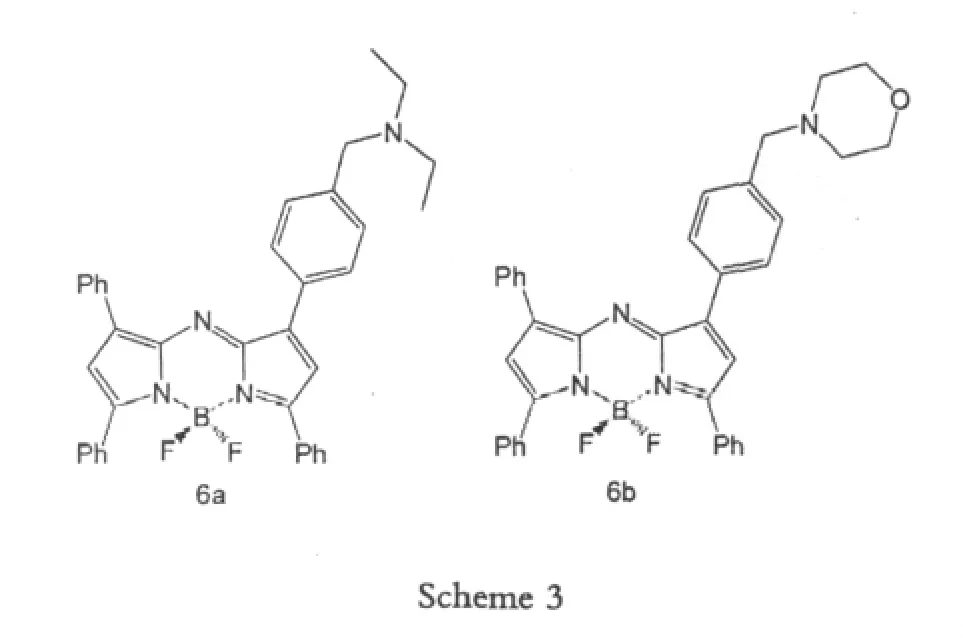
荧光传感器是一类能将分子识别事件通过荧光信号有效表达的分子[11]。典型的荧光传感器一般是由荧光团通过连接基与接受体相连而成。2006年,O'shea D F等人[12]报道了一类新的荧光传感器,它是基于BF2与四芳基氮杂二吡咯甲川类化合物络合的荧光物质,如图Scheme 3所示,它拥有受体(氨基)-连接基(亚甲基)-荧光团(Aza-BODIPY)这一体系。这类荧光传感器可用于分析检测质子、阳离子、阴离子、糖类和缩氨酸等[13],它的原理是当氨基受体接受客体时,导致光诱导电子转移机理失效,从而体现出荧光性,荧光传感器打开。他们通过研究pH值和溶剂极性对这类荧光传感器的影响,得出如下结论:随着pH值(10降至4)的减少,荧光性增强,荧光传感器打开;随着溶剂极性(DMF、THF、二恶烷、环已烷)的减少,荧光性增强,荧光传感器打开。
最近,O'shea D F等人[14-16]对Aza-BODIPY荧光染料进行基团修饰,开发出一系列新的荧光传感器(Scheme 4)。

这类传感器都是基于内在的电子转移机理来响应酸性变化的,随着酸性的变化,荧光传感器产生灵敏的响应,控制荧光性的关/开,其中荧光染料7和9都是内在的双重性质的荧光传感器。当pH从5~6 mol/L HCl变化时,荧光染料7上的一个氨基与H+结合形成氨基正离子,随着酸性的增强,另一个氨基也与H+结合形成氨基正离子,在这一过程中,最大吸收波长发生蓝移从800 nm到750 nm再到650 nm,最大荧光发射波长也发生蓝移从830 nm到760 nm再到680 nm,相应的比色度变化为从红色到紫色再到蓝色,因此荧光染料 7也可作为高灵敏性的多重响应的酸性指示剂。比较荧光染料8 a和8 b是为了研究其受限制的构象对其氨基受体的影响,他们研究发现通过细微的构象的改变,能够控制分析物引起光物理性能响应。
2007年,Gawley R E等人[17]报道了一类基于Aza-BODIPY荧光团-亚甲基连接基-冠醚受体这一体系的荧光传感器(Scheme 5)。这类荧光传感器主要是用于检测贝类毒素,其工作原理为:当贝类毒素不存在时,相当于氨基未被质子化,光诱导电子转移机理生效,荧光性关闭;当贝类毒素与冠醚络合时,相当于氨基被质子化,光诱导电子转移机理失效,荧光性打开,从而可检测出是否存在贝类毒素。

3 近红外区域的荧光探针
荧光探针是指用荧光试剂对待测物进行标记或衍生,生成具有高荧光强度的共价或非共价结合的物质 ,使检出限大大降低,可方便快速地检测金属离子、有机分子和生物大分子 (多肽、蛋白、核苷酸 )等。2008年,O'shea D F等人[18]报道了一类新的近红外区域的荧光探针(Scheme 6)。这类荧光探针的特点是具有较高的荧光量子产率和荧光发射波长超过750 nm,发射波长在750~900 nm区间的荧光探针可有效避免细胞内自身短波长荧光体的干扰,因此这类荧光探针在生物检测领域中具有极大的潜在应用价值。
2009年,O'shea D F等人[19]报道了一类基于Aza-BODIPY荧光染料固载化的荧光探针,通过固载化增强了Aza-BODIPY荧光染料的荧光亮度和光稳定性(Scheme 7)。同年,他们报道了一类pH值响应的近红外区域的荧光探针[20](Scheme 8)。随着pH值(5增至8)的增大,这类荧光染料的荧光性逐渐降低,直至荧光性关闭。引入糖基的目的是为了增强Aza-BODIPY荧光染料的水溶性,达到轻微水溶性的要求,利于生物领域的应用。
4 展望
最近十年来,Aza-BODIPY荧光染料的研究正以令人鼓舞的速度发展,但仍有不完善的方面,未来设计合成新的Aza-BODIPY荧光染料应满足如下要求:(1)较高的荧光量子效率。荧光量子效率越高,荧光性越强,灵敏度越高,荧光染料用量越少,对生物体毒害越小。(2)较长的最大吸收和发射波长。波长越长不但可避免生物体内有机共轭小分子自身荧光的干扰而且可使激发荧光染料所需能量最少,从而不会损害生物细胞。(3)较好的水溶性。水溶性好,有助于在细胞内很好的分散,从而有利于应用生物领域。

[1]Killoran J,Allen L,Gallagher J F,et al.Synthesis of BF2chelates of tetraarylazadipyrrometh-enes and evidence for their photodynamic therapeutic behaviour[J].Chem.Commun, 2002:1862-1863.
[2]Gorman A,Killoran J,O'Shea C,et al.In vitro demonstration of the heavy-atom effect for photodynamic therapy[J].J.Am.Chem.Soc,2004,126:10619-10631.
[3]McDonnell S O,Hall M J,Allen L T,et al. Supramolecular photonic therapeutic agents[J].J.Am.Chem. Soc,2005,127:16360-16361.
[4]Gallagher W M,Allen L T,O'Shea C,et al.A potent nonporphyrin class of photodynamic therapeutic agent:cellular localisation,cytotoxic potential and influence of hypoxia[J].Br. J.Cancer,2005,92:1702-1710.
[5]O'Shea D F,Killoran J,Gallagher W M.Compounds u seful as photodynamic therapeutic agents:US,7220732[P].2007.
[6]Bonnett R.Photosensitizers of the porphyrin and phthalocyanine series for photodynamic therapy[J].Chem.Soc. Rev,1995,24:19-33.
[7]Dougherty T J,Gomer C J,Henderson B W,et al. Review:photodynamic therapy[J].J.Natl.Cancer Inst,1998,90: 889.
[8]MacDonald I J,Dougherty T J.Basic principles of photodynamic therapy[J].J.Porphyrins Phthalocyanines,2001,5: 105-129.
[9]Ali H,Lier J E.Metal complexes as photo-and radiosensitizers[J].Chem.Rev,1999,99:2379-2450.
[10]Rogers M A T.2,4-Diarylpyrroles.Part I.Synthesis of 2,4-diarylpyrroles and 2,2',4',4-tetra-arylazadipyrrome thines[J].J.Chem.Soc,1943,590-596.
[11]De Silva A P,Gunaratne H Q N,Gunnlaugsson T, et al.Chem.Rev.,1997,97:1515-1566
[12]Hall M J,Allen L T,O'Shea D F.PET modulated fluorescent sensing from the BF2chelated azadipyrromethene platform[J].Org.Biomol.Chem,2006,4:776-780.
[13]Hartley J H,James T D,Ward C J.Synthetic receptors[J].J.Chem.Soc.Perkin Trans.1,2000,3155-3184.
[14]McDonnell S O,O'Shea D F.Near-infrared sensing properties ofdimethlyamino-substituted BF2-azadipyrrome thenes[J].Org.Lett,2006,8:3493-3496.
[15]Killoran J,O'Shea D F.Impact of a conformationally restricted receptor on the BF2chelated azadipyrromethene fluorosensing platform[J].Chem.Commun,2006,1503-1505.
[16]Killoran J,McDonnell S O,Gallagher J F,et al.A substituted BF2-chelated tetraarylazadi-pyrromethene as an intrinsic dual chemosensor in the 650~850 nm spectral range[J]. New J.Chem.2008,32:483-489
[17]Gawley R E,Mao H,Haque M M,et al.Visible fluorescence chemosensor for saxitoxin[J].J.Org.Chem,2007, 72:2187-2191.
[18]Loudet A,Bandichhor R,Burgess K,et al.B,O-chelated azadipyrromethenes as Near-IR Probes[J].Org.Lett, 2008,10:4771-4774.
[19]Palma A,Tasior M,Frimannsson D O,et al.New onbead near-infrared fluorophores and fluorescentsensorconstructs[J].Org.Lett,2009,11:3638-3641
[20]Murtagh J,Frimannsson D O,O'Shea D F.Azide conjugatable and pH responsive near-infrared fluorescent imaging probes[J].Org.Lett,2009,11:5386-5389.
Development of Boron Azadipyrromethene(Aza-BODIPY)Fluorophores
CHEN Xiao-li,LI Cui-hong,SONG Qing-bao
(College of Chemical Engineering and Materials,Zhejiang University of Technology,Hangzhou 310014,China)
Aza-BODIPY fluorescent dyes,which are a new fluorescent compounds,are widely used due to their outstanding advantages.The research progress of Aza-BODIPY fluorescent dyes are described from three aspects(photosensitizer,chemosensor,fluorescent probe)of their application.The last,the direction of research and development in this area are prospected.
Aza-BODIPY;fluorescent dyes;photosensitizer;chemosensor;fluorescent probe
1006-4184(2010)07-0018-05
2010-03-12
陈小利(1984-),男,浙江台州人,硕士研究生。主要从事Aza-BODIPY荧光染料的研究。
