含氟液晶材料的发展趋势
2010-09-21李文博姜祎陈新兵安忠维
李文博 姜祎 陈新兵 安忠维
(陕西师范大学化学与材料科学学院,陕西西安710062)
氟化工
含氟液晶材料的发展趋势
李文博 姜祎 陈新兵 安忠维
(陕西师范大学化学与材料科学学院,陕西西安710062)
综述了近年来含氟液晶材料的开发与应用进展,重点介绍了氟原子引入液晶母体分子中不同位置对液晶性能的影响。文中结合液晶材料的相变温度、介电各向异性、双折射和粘度等数据,说明氟取代液晶分子中的恰当位置,对上述性能具有明显的提高,从而满足其在高性能液晶显示器中的应用要求。
含氟液晶;液晶显示;结构与性能
液晶显示器的快速发展已经取代了传统的阴极射线管显示,成了当今信息显示领域的主流产品,这也直接牵动液晶材料的快速发展,据统计,2009年全球液晶材料的消费量超过300 t,而且随着液晶显示器挺进家用电器,特别是家用大屏幕电视的成功应用,对液晶材料从品质到响应速度都提出了更高的要求,而含氟液晶材料的成功开发和应用,不仅满足了高端液晶显示器对液晶材料的基本要求,而且引领了液晶材料的发展趋势。所以,对近年来开发成功的含氟液晶材料从结构到性能进行总结和类比,从中寻出氟原子的引入位置对性能的影响规律,不仅对从事液晶材料的研发人员,而且对从事液晶材料的应用和生产人员以及含氟精细化学品的科技人员都具有十分重要的意义。本文通过搜集文献报道的含氟液晶材料的物理参数,结合液晶显示器发展对材料性能的要求,分析和总结了这些规律,以期能对从事液晶材料及含氟精细化学品的科技人员有所帮助。
1 彩色液晶显示器对液晶材料的基本要求
彩色液晶显示器的主流显示模式分为TN型、VA型和IPS型,各模式对所需液晶材料均有特定要求,但是各种模式显示对液晶材料都具有基本的要求,只有满足这些基本要求,才能在实际中得到应用。一般显示器件要求液晶相变温度范围为-20℃~ 80℃,而特殊器件,比如摄像机、照相机、车载显示器、飞机机舱等要求液晶相变温度范围更宽,要达到-40℃~100℃[1],这样就要求组成混合液晶的各种单体具有更宽的液晶相变温度范围。所以寻找低熔点、高清亮点的液晶单体化合物永远是液晶研发要考虑的主要问题之一。其二是尽可能降低液晶材料的粘度[2]。由于液晶分子在显示器中的作用是在电场信号刺激下做往复运动,粘度越高,分子沿径向运动和恢复所用的时间就越长,就是所谓的响应速度越慢。随着高端显示器的发展需要,液晶的响应速度要求越来越快,所以降低单体液晶化合物的粘度也是高端液晶材料发展追求的目标。其三是增大介电各向异性(△ε)[2-6]。液晶分子介电各向异性值的大小,表明分子的极性差异。表现在液晶显示器中即为△ε值越大,器件的操作电压越低,这不仅意味着节省电力,而且也会提高器件的响应速度。尤其对于移动式显示器,用大绝对值的△ε液晶材料是唯一的选择。其四是适中的双折射。双折射是反映液晶分子沿长轴的折射率和垂直长轴折射率之差的统计值,它直接影响显示器的对比度、视角和清晰度,双折射一般要与所用显示器上下两块玻璃的间隙相匹配。间隙小的器件要选用大双折射的液晶材料,反之亦然。所以通过改变分子结构或引入一些取代基来改变双折射通常也是液晶设计与合成要考虑的基本问题[1]。
2 液晶化合物引入氟原子后的优势和劣势
以上述液晶显示器对液晶材料的基本要求为标准,当氟原子引入液晶分子中引起的性能变化有利于增加介电各向异性值,降低粘度和拓宽向列相温度时即为利用了氟原子的优势。这里我们先给出有机分子氟与其它元素取代后引起的性能参数变化,见表1。
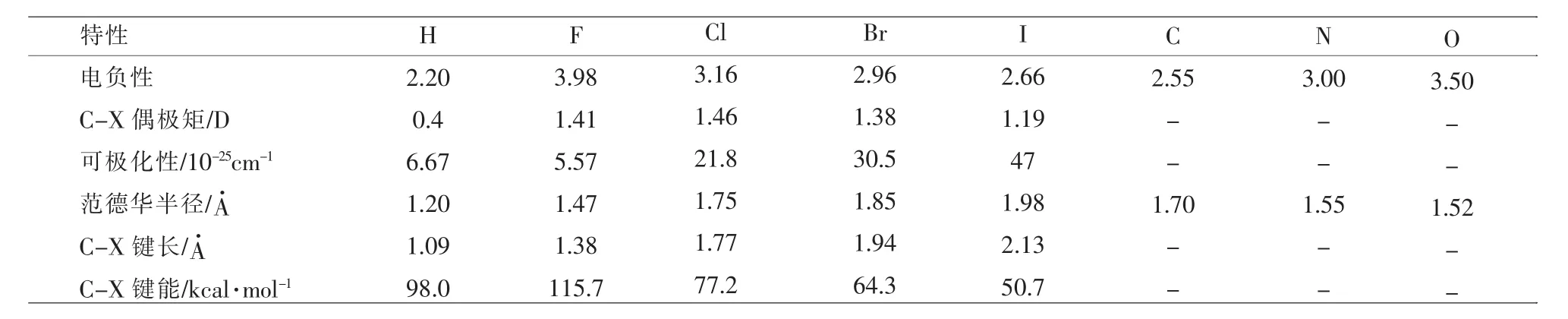
表1 有机分子中氟与其它元素取代的参数[7-9]
从表1可以看出,由于氟在元素周期表中电负性最大,所以C-F键的偶极矩比较大,对改善介电各向异性有很大帮助;而氟原子的范德华半径与氢原子最为接近,所以氟取代氢后在分子中引起的立体效应最小,也就是说用氟取代液晶分子径向伸展的氢之后,对整个分子的长径比影响较小,从而尽量减小了分子产生液晶相的几何构型变化,有利于保持其原有的液晶相稳定性[10];C-F键的键能最大,所以对液晶分子的光和热稳定性有一定改善。对表1中数据的分析认为氟引入液晶分子后具有很大的优势,那么是否可以认为全氟有机化合物就应该是最好的液晶材料?我们在表2中列出了正己烷与全氟正己烷的性能进行比较。
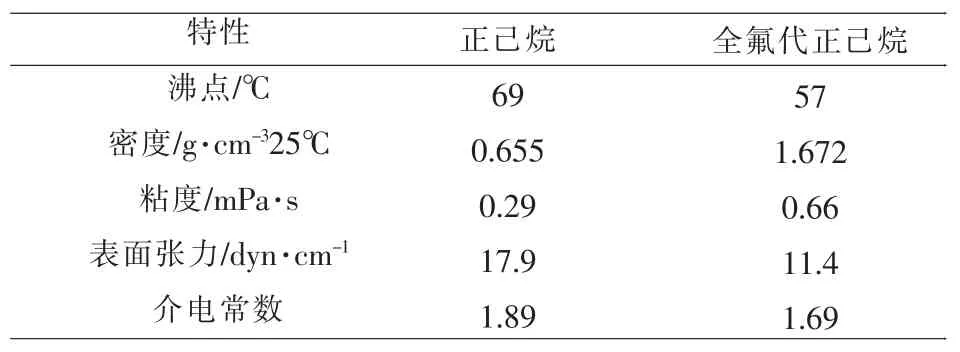
表2 正己烷与全氟正己烷的性能参数[11-13]
表2中从正己烷到全氟代正己烷的沸点降低,密度增加和表面张力降低对液晶的光电性能影响很小,但是粘度从0.29增加到0.66,说明全氟烷基的引入会增加液晶分子的粘度,对提高材料响应速度不利,同时介电常数下降,至少可以说明全氟化合物与碳氢化合物比较可极化度变小,从而降低分子的介电各向异性值。所以对于现有模式的高端彩色液晶显示材料来说,很少考虑引入长链全氟烷基作为取代基团。
3 分子中不同位置氟代对液晶材料性能的影响
为了更为简便的讨论在液晶分子中不同位置氟代后的性能变化情况,我将液晶分子用以下通式来表示:

图1 液晶分子的通式
图1中B代表液晶分子骨架中的各种刚性环结构,比如1,4-取代苯环,1,4-取代环己烷等。
A代表液晶分子骨架中环与环之间连接基 (亦称桥键)比如1,2-取代乙烷,1,2-取代乙烯,1,2-取代乙炔等,有时环与环也可以直接相连,即A代表单键。
X、Y代表液晶分子中的端基和末端基,比如正烷基,-F,-Cl,-CN等。
Z代表液晶分子中连接在环骨架上的基团,称作侧向基,比如侧向F,Cl等。
3.1 端基取代
氟或者含氟基团作为液晶分子的端基取代时,通常主要是为了增加分子的极性,从而提高介电各向异性。下面以烷基双环己基取代苯为例,观测不同基团取代后的介电各向异性差别。
表3中氰基取代的液晶分子△ε值最大,这也是为什么含氰基液晶材料被广泛用于TN和STN液晶混合物中的原因。但是由于TFT彩色液晶材料要求有更高的电阻率(1014Ωcm)和电压保持率(大于98%),而含氰基液晶材料因其易于和微量金属杂质络合而无法满足上述要求,所以液晶化学家们才将注意力集中在含氟液晶上来。△ε值其次的是-SF5作为端基的液晶分子,该化合物不但由于其液晶相温度范围变窄,而且因粘度过大无法在实际中使用[13,14]。表从由-CF3、-OCF3和-OCHF2作为端基的液晶分子均有适中的△ε值(5.2~9.5)。尽管随着△ε值的增加,液晶向列相稳定性下降,但是上述液晶化合物在某些显示器件中仍有使用。单氟取代的化合物△ε值最低,但因其具有比较合适的液晶向列相温度,通常器件中都会用到该类化合物。为了进一步提高氟作为端基的液晶化合物△ε值,可以在分子苯环末端引入多个氟原子,以进一步增加分子的极性,引入后的结果见表4。

表3中氰基取代的液晶分子△ε值最大,这也是为什么含氰基液晶材料被广泛用于TN和STN液晶混合物中的原因。但是由于TFT彩色液晶材料要求有更高的电阻率(1014Ωcm)和电压保持率(大于98%),而含氰基液晶材料因其易于和微量金属杂质络合而无法满足上述要求,所以液晶化学家们才将注意力集中在含氟液晶上来。△ε值其次的是-SF5作为端基的液晶分子,该化合物不但由于其液晶相温度范围变窄,而且因粘度过大无法在实际中使用[13,14]。表从由-CF3、-OCF3和-OCHF2作为端基的液晶分子均有适中的△ε值(5.2~9.5)。尽管随着△ε值的增加,液晶向列相稳定性下降,但是上述液晶化合物在某些显示器件中仍有使用。单氟取代的化合物△ε值最低,但因其具有比较合适的液晶向列相温度,通常器件中都会用到该类化合物。为了进一步提高氟作为端基的液晶化合物△ε值,可以在分子苯环末端引入多个氟原子,以进一步增加分子的极性,引入后的结果见表4。

从表4数据可以看出,从单氟代、双氟代到三氟代液晶化合物中,△ε值也相应从4.2增加到6.3再到11.7,取得了明显的效果。但是其相应向列相温度范围也从51.9℃降低到49.6℃,再进一步到29.8℃,所以在提高△ε值的同时,减小了液晶向列相的温度范围[13,19,15,20-22]。为了寻找既有较大的△ε值,又能尽量保持液晶向列相温度范围的液晶分子,其中最简便的方法之一就是增加分子的长度,所以在分子中增加两个碳原子的液晶化合物被设计和合成出来,它们的性能见表5。

从表5可知,丙基双环己基三氟代苯的熔点是66℃,向列相温度范围为28℃,当增加的-CH2CH2-处于苯环和环己基之间时(化合物11),熔点下降到35℃,向列相温度范围增加到58.8℃,出现了近晶相;当增加的-CH2CH2-处于两个环己烷之间时(化合物12),熔点下降到45℃,向列相温度范围增加到37.8℃,它们的介电各向异性值略有下降。特别有意义的是将母体分子中的一个末端氟被偏二氟乙烯氧基取代后 (化合物13),其相变温度范围增加到87℃,同时△ε值还略有上升[13,24]。这可能是由于一方面F2C=CHO-的长度大于-CH2CH2-,同时由于共轭作用,F2C=CHO-的吸电作用比单个氟原子更强。上述液晶化合物由于其优异的性能在各种显示器中均得到了广泛使用。
3.2 侧基取代
氟作为侧向取代基在液晶合成中已经做了比较广泛的研究。其主要作用是:1)利用氟原子的高电负性,增加侧向的分子极性,从而得到更大的-Δε值。这类液晶广泛应用于VA和IPS显示模式;2)借助氟原子半径(1.47)比氢原子半径(1.20)大,在两个共轭环之间取代从而破坏其共轭程度,以期减少Δn、降低熔点、降低粘度和破坏近晶相的形成而增加有利于显示的向列相温度范围[22]。表6给出了在分子侧向取代基依范德华半径不同而相行为变化的情况:
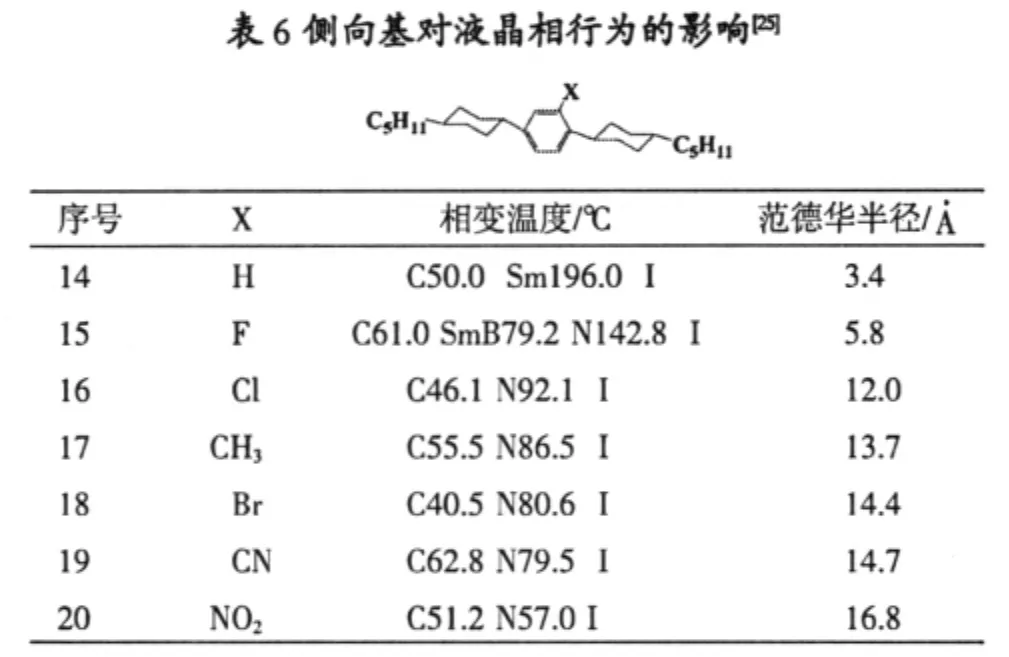
化合物14在50℃熔化后只有近晶相产生。当向苯环侧向引入的基团范德华半径逐渐增加时,从向列相产生(化合物15),到纯向列相(化合物16~20)。而向列相的温度范围也随着取代基体积的增加呈收窄趋势(化合物15~20)。
三联苯液晶因其稳定的液晶相和大的双折射而在液晶材料中占据了十分重要的地位,但是由于三联苯液晶中存在着较宽的近晶相,大的粘度和较小的溶解度(在液晶混合物中溶解度小于5%)而在应用中受到了很大的限制。表7给出了三联苯液晶单氟代后的相行为变化情况。
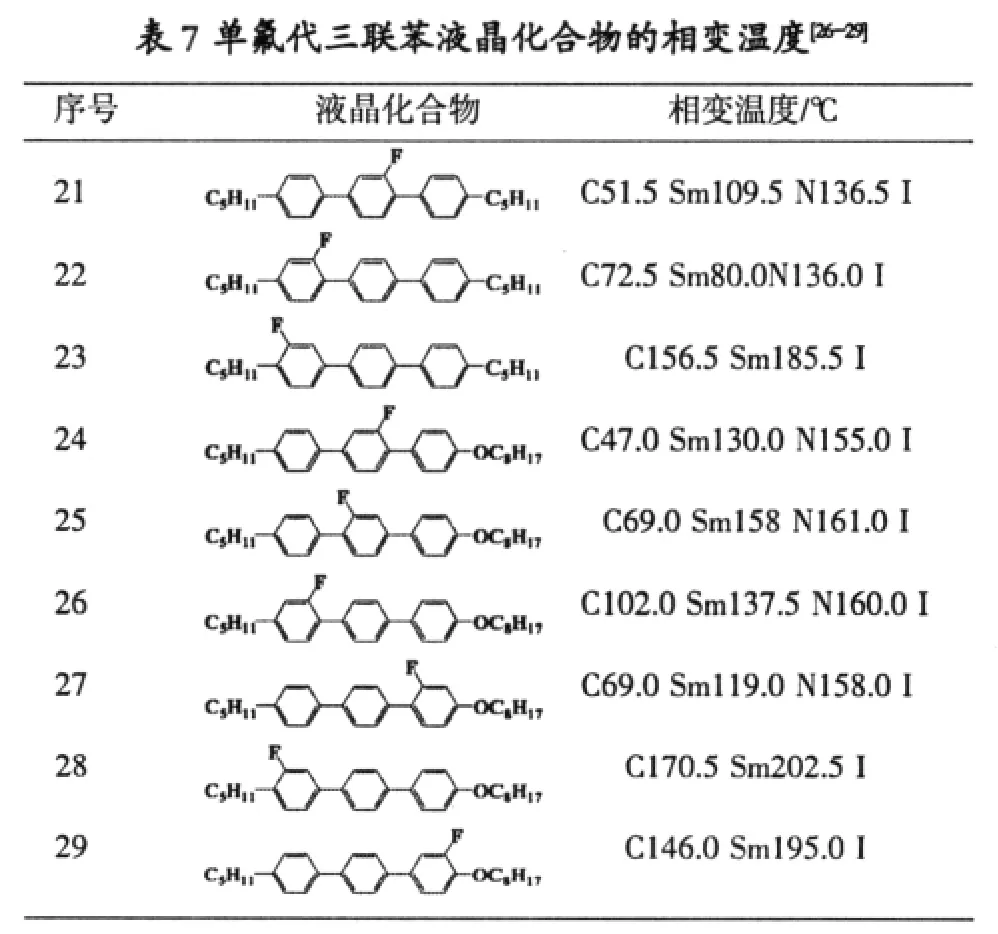
从表7可以看出,单氟代三联苯分为中心环取代(化合物21、24、25)、边环取代(化合物 22、23、 26~29),在边环取代中又有氟取代内侧方向(化合物22、26、27)和外侧向取代(化合物23、28、29)[26-28]。在三联苯两个端基相同的情况下,内环取代(化合物21)与边环取代中内侧方向(化合物22)清亮点变化不大,但内环取代的熔点低于边环取代。而边环外向取代(化合物23)的熔点最高,而且没有向列相[30,31],所以对于用作显示材料不利。其主要原因是氟取代在边环侧外方向时,对三联苯中苯环的共轭抑制作用降低所致。当三联苯两个端基不同时,氟在中心环取代时偶极矩方向与三联苯分子一致时,(化合物25)熔点、清亮点和近晶相温度都偏高,反之(化合物24),熔点、清亮点和近晶相温度都会下降。当氟原子在边环向内取代时,偶极矩方向与原分子极性一致(化合物27)会导致熔点、清亮点和近晶相温度下降,反之(化合物26),上述温度会上升。与上述相同端基三联苯一样,不对称端基三联苯化合物的边环侧外单氟代化合物(28、29)只存在近晶相,比较化合物28和29可知,氟代的偶极矩方向与原骨架偶极方向相反时,熔点和清亮点均会明显下降。
对于二氟代三联苯液晶的相变情况就更为复杂,数据见表8。

从表8中数据可以看出,如果比较化合物30和31相变温度,当两个氟相邻处于同一苯环上时,中心环取代只有向列相要明显优于边环取代(化合物31)。在三联苯两个端基不同时,比较化合物32、33和34可以看出,中心环双氟代化合物(32)要优于两个边环双氟邻取代化合物(33和34),而边环双氟邻取代处在烷基环上的化合物34由于熔点低、清亮点高要优于处在烷氧基环上的化合物33。
比较化合物37和40可以看出,在同一苯环上双氟对取代时,双氟对取代中心环上的化合物37由于熔点低,只有向列相而明显好于双氟对取代边环的化合物40,后者不仅熔点高,而且向列相温度范围仅为6℃。化合物35、36、38和39是两个氟取代在不同环上的双氟代三联苯液晶。而35和36中两个氟原子的偶极矩方向均指向分子中心,所以它们都具有较低的熔点和唯一的向列相,非常适合在显示用液晶材料中应用,而化合物38和39,由于有一个氟原子的偶极矩方向指向三联苯的侧外方向,所以有近晶相或较高近晶相温度存在,从而无法在实际中应用。
对含三个氟原子取代的三联苯液晶性能见表9,其相行为变化规律与单氟、双氟代相似,当其中一个氟原子的处于边环,且偶极矩指向侧外向时(化合物43、44),均有形成近晶相的倾向。而氟取代处于中心环和边环,偶极矩指向侧内时(化合物41、42),都具有较好的向列相温度。

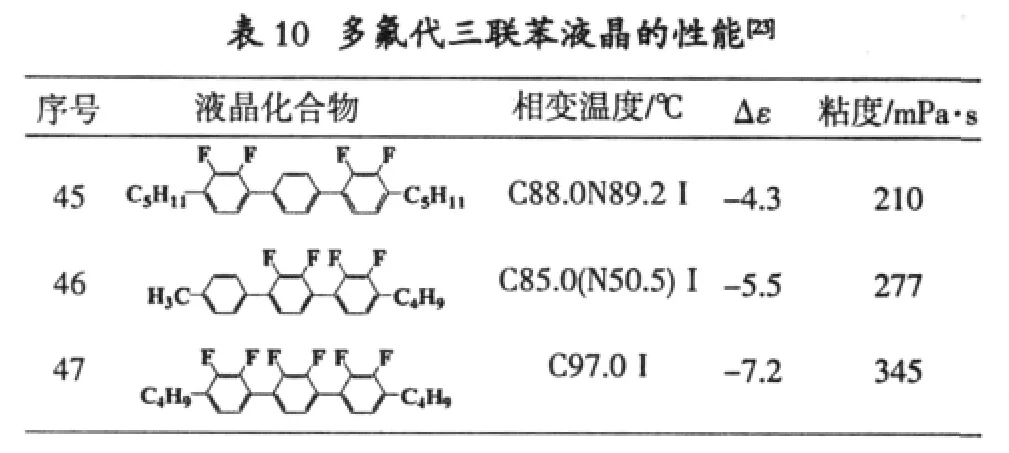
多于三个氟原子取代的三联苯液晶 (见表10)性能一般都表现为向列相,但是向列相温度范围很窄(化合物45、46),当三联苯中有六个氟原子取代后(化合物47),液晶相全部消失,但是化合物的△ε负值随着氟取代数增多而增加。特别值得注意的是,当四个氟原子处在两个边环时(化合物45)其粘度要小于四个氟原子处在两个相邻苯环上的化合物(化合物46)。而随着氟取代数的增多,粘度也相应增加。
随着高性能显示器件发展的需求,三联苯液晶暴露出了粘度高、溶解度小和双折射偏大等缺点。为了克服上述缺点,许多环己基苯和双环己基苯液晶被合成。氟代环己基苯类液晶的性能见表11。

通过比较化合物48和49可以看出,当苯环末端被乙氧基取代后的Δε值为-5.9,而甲基取代的Δε值仅为-2.7,这一变化可能是由于烷氧基除了有比烷基更大的供电子能力外,氧原子的p电子通过苯环π电子而影响氟原子的p电子轨道,从而使氟原子的电子云密度偏向分子中心方向,也就是氟的偶极矩方向垂直于分子长轴方向偏移,从而增加了Δε的负值。但是由于氧原子的存在,化合物49具有更高的粘度。比较化合物49和50可知,在分子结构中,中心环由于苯环取代环己烷(化合物50)后,相变温度和Δε值变化不大,但是化合物50有比化合物49更小的粘度,这就是由于氟取代而引起的反常现象。比较化合物51和化合物50、49可以看出,当分子中减小一个环骨架后,尽管液晶相消失,但是△ε负值略有增加,更主要的是粘度大大减小。所以化合物51通常被大量应用在实用配方中起到"溶剂"作用。
为了进一步提高液晶材料的响应速度,也就是进一步增加△ε负值和降低粘度,各种结构的含氟液晶化合物被化学家们设计和合成出来。下面举两组例子来说明所合成的化合物的性能变化情况。表12给出了含五元稠环的液晶化合物。从表中可以看出,此类化合物随着氟取代个数的增加,△ε值有明显的改善。

但是由于其熔点偏高,而且液晶相温度范围也不尽人意,所以未能实现其在显示器件中的应用。而表13中所列出的含双环己烷类氟代液晶,尽管同所预测的一样,此类液晶表现出较低的熔点和粘度,但是由于饱和环上氟取代后增加了分子中的侧向之间的吸引力,从而导致了形成近晶相的趋势,所以实用配方中一般避免使用该类液晶化合物。

4 连接基(桥键)
连接基处于液晶分子中心的环骨架之间,所以在连接基上进行氟取代后对液晶性能的影响非常显著,可以认为可以起到"四两拨千斤"的作用。主要作用除改变液晶的相行为外,对介电各向异性和粘度都有很显著的改善,表14给出了在含亚乙基连接基和乙氧基连接基中氢被氟取代后的性能变化情况。
表14中化合物59和60的数据比较可以看出,对于分子骨架中含饱和环的液晶化合物,中心连接乙基氟代后液晶相温度明显提高,粘度变化不大。而比较含有端基二氟代的化合物61和62也有同样的结果,只是化合物61的向列相温度范围65.3℃比化合物62的向列相温度范围57℃略宽一些。所以对于含端氟代液晶中连接基氟代后效果并不理想。比较化合物63和64可以看出增加氟代乙氧连接基后,其向列相温度范围从化合物63的28℃加宽到化合物64的61.3℃,而且△ε值从化合物63的9.7提高到化合物64的10.5,同时粘度也从171 mPa·s下降到145 mPa·s。如果将化合物64中的边环己烷用二噁烷取代成化合物65,△ε还可继续从10.5提高到20.6。但是二噁烷的引入会增加液晶化合物的粘度(从化合物64的145 mPa·s提高到化合物65的207 mPa·s)比较化合物66和67也同样可以看出,二噁烷的引入相同氟代苯骨架中,△ε值总会有一定程度的提高。如果在分子中继续增加氟代苯的数量,△ε值也会继续增加 (比较化合物66和68)。这里需要指出的是化合物66和68,尽管它们均不存在液晶相,但是在许多用于移动设备(如手机、笔记本电脑、照相机等)的显示器中均选用该类化合物来提高液晶材料的△ε值,以降低工作时所需的电压。

从表14可以看出,在液晶化合物中引入氟代乙氧基是液晶材料发展中的一大创造,它对于很多低阈值液晶配方是不可缺少的组分,同时该类化合物的低粘度也为其在高响应速度液晶显示器中应用奠定了基础。
5 总结与展望
本文通过列举氟作为端基、侧向基及连接基氟代对液晶性能的影响数据,在比较中归纳出氟取代液晶中不同位置所引起性能变化的规律。从上述数据可以看出,适当引入氟取代后对提升液晶材料的综合性能,特别是提高介电各向异性值,降低粘度和拓展显示用向列相温度范围都具有至关重要的作用,可以说没有氟代液晶材料的发现与发展,也就不会有当今火热的液晶显示器发展。
从液晶显示发展的总体趋势来看,提高响应速度和改善显示清晰度将是今后追逐的目标。从目前情况来看,要实现微秒级响应速度的液晶显示,可能需要更新的液晶材料和显示模式。其中铁电液晶和蓝相液晶有可能成为新的突破口[47,48]。而铁电液晶材料和蓝相液晶材料相对于向列相而言实际上是分子排列高度有序的液晶相。这种双轴二维有序排列往往需要分子间的作用力来驱动。而多氟化合物与碳氢化合物存在分子间氢键已经很早被人们所认识,比如全氟苯与苯的络合物其熔点由苯的5.5℃和全氟苯的3.9℃升高至23.7℃。所以巧妙地利用这一分子间的作用力构筑全新的液晶相是完全可能的,也是今后含氟液晶主要发展的趋势之一。
[1]陈新兵,安忠维.化学进展[J],2006,18:246-251.
[2]张晓军.乙烷类四环体系液晶的合成及性质研究[D]:硕士学位论文.北京:清华大学化学系,2002.
[3]李维堤,郭强.液晶显示器件应用技术(第三章实验部分)[M].北京:北京邮电学院出版社,1993.
[4]Takahashi T,Saito S,Akahane T.Jpn.J.Appl.Phys[J]. 1997,Part 1,36:3531-3536.
[5]Lee S H,Kim H Y,Park I C,et al.Appl.Phys.Lett [J].1997,71:2851-2853.
[6]Lee S H,Kim H Y,Park I C,et al.IEICE Trans. Electron[J].1998,E81C:1681-1684.
[7]Nagel J K,J.Am.Chem.Soc[J].1990,112,4740.
[8]Sen K D,Jorgensen C K。Electronegativity[M]. Springer,New York,1987.
[9]Bondi A.J.Phys.Chem[J].1964,68,441.
[10]Hird M.Chem.Soc.Rev[J].2007,36,2070-2095.
[11]Banks R E.Fluorine Chemistry at the Millennium[M]. Elsevier,Oxford,2000.
[12]Banks R E,Smart B E,Tatlow J.C.Organofluorine Chemistry: Principles and Commercial Applications [M]. PlenumPress,New York,1994.
[13]Kirsch P.,Modern Fluoroorganic Chemistry[M].Wiley-VCH,Weinheim,2004.
[14]Kirsch P,Bremer M,Heckmeier M,et al.Angew. Chem.,Int.Ed[J].1999,38,1989.
[15]Demus D,Goto Y,Sawada S,et al.Mol.Cryst.Liq. Cryst[J].1995,260:1.
[16]Takatsu H,Ohnishi H,Kobayashi K,et al.Mol.Cryst. Liq.Cryst[J].2001,364:171.
[17]Pavluchenko A I,Smirnova N I,Petrov V F,et al.Mol. Cryst.Liq.Cryst[J].1991,209:225.
[18]Bartman E.Ber.Bunsen-Ges.Phys.Chem [J].1993, 97:1349.
[19]Goto Y,Ogawa T,Sawada S,et al.Mol.Cryst.Liq. Cryst[J].1991,209:1.
[20]Mueller H J,Haase W.Mol.Cryst.Liq.Cryst[J].1983, 92:63.
[21]Shibata K S,Miyazawa K,Goto Y.Chem.Commun.[J], 1997:1309.
[22]Hird M.Chem.Soc.Rev.[J],2007,36:2070-2095.
[23]Pauluth D,Tarumi K.J.Mater.Chem.[J],2004,14: 1219.
[24]Raviol A,Stille W,Strobl G.J.Chem.Phys[J].1995, 103:3788.
[25]Osman M A.Mol.Cryst.Liq.Cryst[J].1985,128:45.
[26]Gray G W,Hird M,Toyne K J,Mol.Cryst.Liq.Cryst[J]. 1991,195:221.
[27]Chan L K M,Gray G W,Lacey D,et al.Mol.Cryst. Liq.Cryst[J].1988,158B:209.
[28]Chan L K M,Gray G W,Lacey D.Mol.Cryst.Liq. Cryst[J].1985,123:185.
[29]Chan L K M,Gray G W,Lacey D,et al.Mol.Cryst. Liq.Cryst[J].1987,150B:335.
[30]Chambers M,Clemitson R,Coates D,et al.Liq.Cryst [J].1989,5:153.
[31]Jones J C,Towler M J,Hughes J R.Displays[J].1993, 14:86.
[32]Slaney A J,Minter V,Jones J C.,Ferroelectrics[J]. 1996,178:65.
[33]Gray G W,Hird M,Lacey D,et al.J.Chem.Soc., Perkin Trans[J].1989,2:2041.
[34]Gray G W,Hird M,Toyne K J.Mol.Cryst.Liq.Cryst [J].1991,204:43.
[35]Hird M,Toyne K J,Gray G W,et al.Liq.Cryst[J]. 1995,18:1.
[36]Glendenning M E,Goodby J W,Hird M,et al.J.Chem. Soc.,Perkin Trans[J].1999,2:481.
[37]Glendenning M E,Goodby J W,Hird M,et al.J.Chem. Soc.,Perkin Trans[J].2000,2:27.
[38]Klasen M,Bremer M,Tarumi K.Jpn.J.Appl.Phys[J]. 2000,39:1180.
[39]Reiffenrath V,Bremer M.Angew.Chem.,Int.Ed.Engl [J].1994,33:1386.
[40]Kirsch P,Tarumi K.Angew.Chem.,Int.Ed[J].1998,37: 484.
[41]Bremer M,Lietzau L.New J.Chem[J].2005,29:72.
[42]Kirsch P,Heckmeier M,Tarumi K.,Liq.Cryst[J]. 1999,26:449.
[43]Schadt M Buchecker R,Villiger A.Liq.Cryst[J].1990, 7:519-536.
[44]Kelly S M.Liq.Cryst[J].1996,20:493-515.
[45]Kirsch P,Bremer M,Taugerbeck A,et al.Angew. Chem.Int.Ed[J].2001,40(8):1480-1484.
[46]Kirsch P,Bremer M,Huber F,H.Lannert,et al.J. Am.Chem.Soc[J].2001,123:5414.
[47]KikuchiH,Yokota M,Hisakado Y,et al.Nature Materials[J].2002,1(1):64-68.
[48]Cao W Y,Munoz A,PalffyMuhoray P,et al.Nature Materials[J].2002,1(2):111-113.
Tendency of the Fluorinated Liquid Crystal Materials
Li Wen-bo,Jiang Yi,CHEN Xin-bing,AN Zhong-wei*
(The school of Chemistry and Materials Science,Shaanxi Normal University,Xi′an 710062,China)
The recent progress of the development and application of fluorinated liquid crystal was summarized.It was Emphasized on the effect of their properties on fluorine atom introduced at different position of the non-fluoring molecules by the comparison of their physical parameters,such as phase transition behavior, dielectric property,birefringence and viscosity.The significant improvement of those properties had been exhibited by a proper substitution of fluorine,which had matched the rapid development requests of liquid crystal display.
Fluorinated liquid crystal;liquid crystal display;structures and properties
1006-4184(2010)08-0001-07
2010-07-08
李文博(1985-),女,山西运城人,硕士,主要从事染料敏化太阳能、液晶材料的研究。
