茶油中总酚的测定方法
2010-09-11钟冬莲
丁 明,钟冬莲
(中国林业科学研究院 亚热带林业研究所,浙江 富阳 311400)
油茶 (Camellia oleifera)为山茶科山茶属多年生木本植物。广布于亚热带地区,在我国长江流域及以南各省普遍栽培。茶油为油茶籽制得的食用油脂,又名茶籽油或山茶油,色清质纯,营养丰富,略带茶油特有的芬芳,是一种高级食用油。茶油具有较强的抗氧化能力,贮藏试验研究表明,茶油的氧化稳定性明显高于菜籽油、花生油等植物油[1-2]。酚酸在抗氧化性能中起重要作用,同时也是茶油色泽的物质之一,酚酸还可能茶油中苦味的来源之一[3]。
目前各种植物的酚酸总量测定方法文献报道很多,主要采用液液萃取后用 FeCl3法和 Folin-Ciocaltea比色法,但尚未见茶油中总酚测定的报道。采用对传统的液液萃取的方法和固相萃取提取方法进行比较和验证,建立了固相萃取Folin-Ciocaltea比色法测定茶油总酚的含量的方法,为进一步研究茶油中酚类物质奠定一定基础。
1 材料与方法
1.1 材料
采集不同等级的浸出和压榨的茶油4种:江西常山山神精炼高烹油 (J1)和压榨毛油 (M1),建德霞雾精炼高烹油 (J2)和压榨毛油 (M2)。
UVPC-2401(日本岛津公司),Diol-SPE 500 mg/3 mL固相萃取小柱 (美国waters),0.1 mg分析天平 (梅特勒),恒温真空干燥箱 (上海高精),723型可见分光光度计,150 mL分液漏斗,旋转蒸发仪,氮吹仪 。咖啡酸 (AR)、碳酸钠 (AR)、甲醇 (AR)、乙醇 (AR)、甲醇 (色谱醇)、乙腈(AR)、正己烷 (AR)、乙酸乙酯 (AR)。Folinciocaltea试剂:将 50 g Na2WO4·2H2O(AR)、12.5 g Na2MO4·2H2O(AR)、350 mL蒸馏水、85%25 mL H3PO4(AR)、50 mL浓HCl(AR)均置于磨口回流装置中,用文火回流10 h(回流过程中不使液体沸腾,只维持在缓慢冒气泡阶段)后,再往装置中加入75 g Li2SO4(AR)、25 mL蒸馏水、数滴液溴,沸腾15 min,以除去过量的溴,最后冷却,定容至500 mL,即 Folin-Ciocaltea试剂,使用时加入1倍体积的蒸馏水使酸的浓度为1 mol·L-1。
1.2 方法
1.2.1 标准溶液配制
精确称取咖啡酸标准品100 mg,用少量甲醇溶解并用蒸馏水定容到100 mL,得1.0 mg·mL-1的对照品标准溶液。
1.2.2 标准曲线的建立
分别量取上述标准液 2.5,5.0,7.5,10.0,15.0,20.0,25.0 mL于7支50 mL容量瓶中,蒸馏水定容,制备成浓度0.05~0.5 mg·mL-1的咖啡酸标准液。分别吸取各浓度标准液0.5 mL于7支50 mL容量瓶中,另取1支做空白,各加25 mL蒸馏水,摇匀,再分别加0.5 mL Folin-Ciocaltea试剂,充分摇匀。3 min后,加入10% 碳酸钠溶液(10 g碳酸钠溶入100 g水)1.0 mL,混匀定容。在35℃下反应120 min,于 725 nm波长下比色,测定吸光度,建立标准曲线。
1.2.3 样品处理
液液萃取。取一定量毛油,用溶剂等体积萃取3次,合并萃取液,在40℃ 真空浓缩至近干,用相应溶剂5 mL分多次洗出于10 mL离心管 中,10 000 r·min-1下离心10 min,冷冻脱脂后吸取上层醇相于5 mL刻度管中,相应溶剂定容,得到总酚提取物溶液。用Folin-Ciocalteau法定量。
固相萃取。取一定量毛油,用适量正己烷溶解,固相萃取小柱用适量正己烷活化,上样,上样后再用适量正己烷溶解油样,并用适量正己烷∶乙酸乙酯(9∶1)洗脱酯溶性物质,然后用10 mL溶剂洗脱酚酸并收集,40℃下氮气吹干,再用1 mL相应溶剂洗出于1 mL离心管中,10 000 r·min-1下离心10 min,冷冻脱酯,得到总酚提取物溶液。用Folin-Ciocalteau法定量。
1.2.4 反应体系
取一定体积待测溶液用蒸馏水定容至25 mL,再依次加入 0.5 mL Folin-Ciocaltea试剂 (静置 3 min),10%碳酸钠溶液1 mL,蒸馏水定容到50 mL,35℃下反应120 min,于725 nm波长下测定吸光度。
2 结果与分析
2.1 标准曲线
建立吸光度 (D)与咖啡酸浓度 (X)标准曲线,在0.05~0.5 mg·mL-1浓度范围内,线性回归方程为D=1.097 9X-0.014 4,相关系数R2=0.996 9。
2.2 固相萃取小柱及洗脱溶剂
分别试验C18、硅胶、弗罗里硅土以及二醇基等固相萃取小柱,发现Diol-SPE 500 mg/3 mL固相萃取小柱 (美国waters)效果明显较好,这可能与酚类物质极性较大,在二醇基等固相萃取小柱具有良好的保留作用相关。
分别采用100%甲醇,80%甲醇,80%乙醇,90%乙醇,95%乙醇,100%乙腈,100%乙醇作为洗脱溶剂按固相萃取后测定。由表1可见90%的乙醇洗脱效果最好,测得的总酚含量最高。这可能与茶油总除了极性较大的酸性酚类物质外还有较多的中性酚类物质,因此90%的乙醇洗脱比较完全而且乙醇价格便宜、对人体毒害小,是一种较好的提取溶剂。
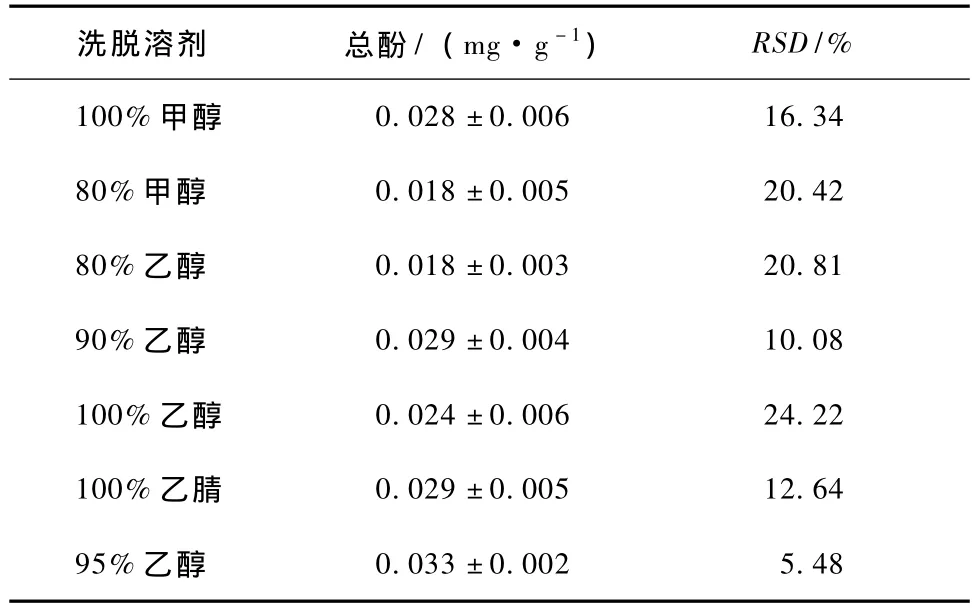
表1 茶油不同溶液萃取总酚的效果
2.3 液液萃取与固相萃取方法比较
在样品中添加0.02,0.04,0.06 mg单个浓度水平的标准,分别用液液萃取和固相萃取方法测吸光度,得出总酚的含量,以加标测得的量减去原样的量,除以加标量,计算回收率。由表2可知,固相萃取的添加平均回收率达99.36% ~110.02%,明显高于液液萃取的72.03% ~81.33%,酚类物质是一类带有非极性基团的极性化合物,因此,液液萃取不能完全萃取以及液液萃取由于萃取历时较长加上浓缩时加热等过程使较多的酚类物质被氧化而导致回收率明显下降。在固相萃取中随着标准的添加量的增加,回收率有较大幅度的下降,这与固相萃取小柱柱容量有关,当添加过多的标准使小柱过载从而导致回收率下降。
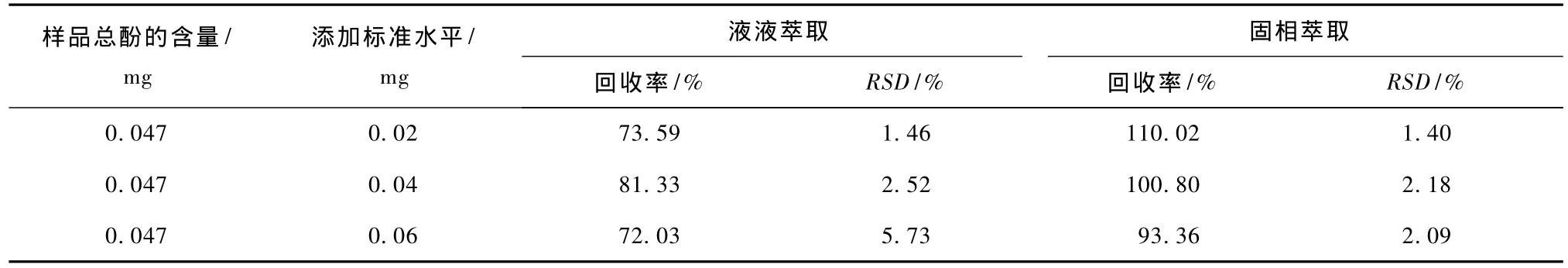
表2 加标回收试验结果(n=5)
2.4 稳定性实验
取1油样按上述样品溶液制备及测定方法,于4℃放置 0,2,4,6,8,15,21 h测定吸光度值。从表3可以看出,由于酚类物质被氧化,其总量值略有下降的趋势,但6 h内溶液稳定性良好,随着时间的延长,有较大幅度的下降,RSD为3.98%。
2.5 精密度
取茶油样品按固相萃取方法提取及测定方法,重复测定 5次,结果如表 4所示,得RSD为0.36%(n=5)。

表3 稳定性实验结果
2.6 重现性
称取相同质量的茶油5份,按固相萃取方法及测定方法,测定吸光度值,结果如表5所示,得相对标准偏差为3.53%,表明具有良好的重现性。

表4 精密度实验结果

表5 重现性实验结果
2.7 实际样品的测定
按固相萃取方法测定不同厂家的浸出油和压榨油中总酚,结果如表6所示。由表6可见,经过精炼的茶油总酚含量明显低于毛油,不同厂家的趋势也相同,可见茶油在经过脱酸、脱臭等处理后,将大部分的酚类物质去除,其抗氧化能力大大减弱;而毛油因只经压榨处理,保留大部分的酚类物质。
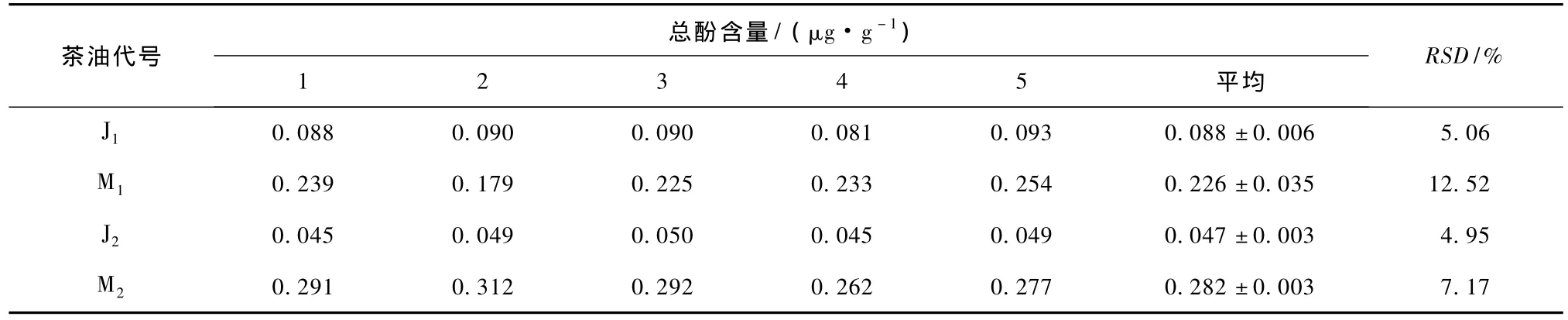
表6 不同茶油样品中的总酚含量
3 小结
通过液液萃取与固相萃取的比较可见,采用正己烷溶解,经二醇基固相萃取小柱分离富集后,90%乙醇洗脱并收集,40℃下氮气吹干,再用1 mL相应溶剂洗出于离心管中,10 000 r·min-1下离心10 min,冷冻脱酯,用Folin-Ciocalteau法测定茶油中的总酚含量,回收率高、灵敏度高,精密度、准确度好,而且操作简单、快速又节约成本,实为较好测定茶油中总酚的方法。
[1]丛林美,姚小华,费学谦.长期储藏对茶油酸值和过氧化值的影响 [J].林业科学研究,2007,20(2):246-250.
[2]程建华,杨卫民,张凤枰,等.油样短期存放条件对过氧化值测定的影响 [J].中国油脂,2004,29(2):55-58.
[3]Mailer R. Chemistry and quality of olive oil[J].Profitable&sustainable Pimary Industies, 2006 (8):227-230.
