爬山虎茎粉对水体中氨氮的吸附特性
2010-09-09刘海伟王海云董元华中国科学院南京土壤研究所土壤与农业可持续发展国家重点实验室江苏南京20008中国科学院研究生院北京00049
刘海伟,刘 云,王海云,董元华*(.中国科学院南京土壤研究所,土壤与农业可持续发展国家重点实验室,江苏 南京 20008;2.中国科学院研究生院,北京 00049)
爬山虎茎粉对水体中氨氮的吸附特性
刘海伟1,2,刘 云1,王海云1,董元华1*(1.中国科学院南京土壤研究所,土壤与农业可持续发展国家重点实验室,江苏 南京 210008;2.中国科学院研究生院,北京 100049)
为从植物材料中筛选适宜的氨氮吸附材料,通过批实验研究了爬山虎茎在不同初始pH值、振荡时间、初始浓度和温度下对水溶液中氨氮的吸附情况,进而分析了吸附等温线、动力学和热力学特性.结果表明,爬山虎茎已经达到或超过矿物吸附氨氮的水平.氨氮吸附最适pH值为5~9.吸附过程基本在第18h达到平衡,控速步骤主要是膜扩散和粒内扩散.等温吸附符合Langmuir模型,最大吸附量在15,25,35°C下分别为3.18,4.69,5.19mg/g.热力学参数ΔG°、ΔH°和ΔS°表明,爬山虎茎对氨氮的吸附属于自发的吸热反应,且属于物理吸附.因此,爬山虎茎可以作为开发氨氮吸附剂的原材料.
铵离子;吸附剂;等温线;动力学;热力学
Abstract:Batch experiments were carried out to study adsorption characteristics of ammonia from aqueous solution onto Boston ivy (Parthenocissus tricuspidata Planch) stem powder. Effect of pH, initial ammonia concentration, contact time and temperature on adsorption of ammonium were investigated as well. The results showed that the ammonia adsorption capacity of Boston ivy stem powder could be comparable to those of minerals. The optimum pH range for ammonia adsorption was 5~9. The adsorption reached equilibrium at about 18 h, and the rate-controlling steps were film diffusion and intraparticle diffusion. The equilibrium data fitted well with the Langmuir model and the maximum adsorption capacities was 3.18, 4.69 and 5.19 mg/g at 15, 25 and 35°C respectively. Thermodynamic study proved that the adsorption process was a spontaneously endothermic process, and implied that ammonia adsorption by Boston ivy stem powder might be physisorption. Therefore, the Boston ivy stem could be a considerable raw material to develop the ammonia adsorbent.
Key words:ammonium ion;adsorbent;isotherms;kinetics;thermodynamics
过量氨氮进入河流、湖泊等水体后会引起水体富营养化,减少水中溶解氧,毒害鱼类等水生生物.常用废水中氨氮的处理法有硝化反硝化法、吹脱与气提法和化学沉淀法等.其中吸附法和离子交换法因为更加经济高效和环境友好,受到越来越多的关注.对氨氮吸附效果较好且研究比较多的吸附剂包括斜发沸石[1]和丝光沸石[2]等.此外,凹凸棒石[3]和竹炭[4]对水体中的氨氮也有较好的吸附作用.植物材料是自然界中另一种良好的吸附材料,其富含纤维素、半纤维素和木质素,因此表面可能会有大量的极性基团,如醇基、醛基、酮基、羧基、酚基和醚基等,这些基团在一定程度上有束缚污染物的能力[5].因此,植物材料可去除水体中的重金属、染料、硝态氮、磷和酚类物质等[6-7].然而,植物材料吸附去除水体中氨氮的研究尚未见报道,因此本文研究植物材料爬山虎茎粉对水体中氨氮吸附的等温线、动力学和热力学特性,分析不同初始pH值对吸附的影响,为开发植物材料成为氨氮吸附剂提供参考.
1 材料与方法
1.1材料
供试植物爬山虎(Parthenocissus tricuspidata Planch)采集于南京郊区.爬山虎茎分离并用水清洗其表面去除灰尘和可溶杂质后,室内风干.样品在105℃下杀青15min后,在70℃烘10h.粉碎,过30目筛,置于自封袋中作为吸附剂备用.
1.2主要仪器
傅立叶转换红外光谱仪(Nexus 870型,美国Thermo Nicolet公司),微电泳仪(JS94H型,上海中晨数字技术设备有限公司),恒温振荡器(SHA-C型,常州国华电器有限公司),低速台式大容量离心机(RJ-TDL-5A型,无锡市瑞江分析仪器有限公司), pH计(PHS-3CT型, 上海康仪仪器有限公司).
1.3实验方法
吸附实验采用批处理法进行.称取0.2000g爬山虎茎粉置于50mL离心管中,加入25mL一定浓度的氨氮溶液.在25℃下250r/min振荡24h以达到吸附平衡.平衡后离心管在4000r/min下离心5min,上清液用0.45µm微孔滤膜过滤.用蒸馏和滴定法[8]测定滤液中氨氮浓度.空白实验以去离子水代替氨氮溶液.
pH值、氨氮浓度、温度和振荡时间对爬山虎茎吸附氨氮的影响实验按批处理法进行.初始pH值的影响实验,溶液初始pH值设2~12共11个处理,用0.1mol/L的HCl或NaOH溶液调节;各溶液氨氮含量均为25mg/L.反应氨氮浓度和温度的影响实验,氨氮浓度设为10,25,50,100,200, 500,800,1000mg/L,振荡温度分别为15,25,35℃.振荡时间影响实验中,氨氮浓度为25和100mg/L,振荡时间范围为1~24h,定时取样检测.除pH值影响实验外,其他实验溶液的初始pH值为氨氮溶液自然值(pH5).
爬山虎茎表面zeta电位的测定:用0.1mol/ LHCl或NaOH溶液调节0.001mol/LNaCl溶液的pH值分别为1.5、3、4、5、6、7、8、9、10和11.各溶液50mL置于三角瓶中,分别加入0.03g过200目筛的爬山虎茎粉.振荡12h,重新调节各溶液pH值,再重复2次振荡和调节pH值.静置12h,先测各溶液pH值,再用微电泳仪测定各溶液中材料表面zeta电位.
爬山虎茎粉吸附氨氮前后的红外光谱(FTIR)采用KBr压片法测得,分辨率2cm-1,光谱范围为400~4000cm-1.爬山虎茎粉的比表面积采用氮吸附法测定.
1.4数据处理
氨氮的去除率(%)和吸附量(q, mg/g)分别用下列公式计算
去除率(%) = (C0−Ce)/C0×100 (1)
吸附量q=(C0−Ce)V/M (2)式中: C0和Ce分别是初始和吸附平衡后溶液中氨氮浓度,mg/L;V是加入溶液的体积, L; M是吸附剂质量,g.
2 结果和讨论
2.1爬山虎茎材料的特性
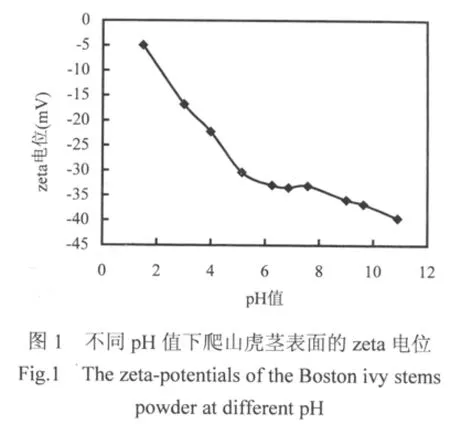
爬山虎茎粉的BET比表面积为0.53m2/g, Langmuir比表面积为0.81m2/g.图1所示爬山虎茎表面zeta电位在pH1.5~11都是负值,其范围为−39.60~−4.94mV.这表明静电引力有利于表面带负电荷的爬山虎茎对阳离子NH4+的吸附.Zeta电位随着pH值增加而降低,即随着pH值增加爬山虎茎表面所带负电荷增多.等电位点(pI)可能在0.5左右,pH值低于此值,爬山虎茎表面将带正电荷.
氨氮吸附前后爬山虎茎的傅立叶转换红外光谱(FTIR)见图2.其中,3700~3000cm-1的宽峰由于—OH的伸缩振动,在2922和2854cm-1的峰分别是因为—CH3和—CH2—的振动,在1736和1620cm-1出现C=O的伸缩振动峰,而1319到1242cm-1之间的峰则可能由于-OH或C-O的弯曲振动,而1200~950cm-1范围内一系列峰是由于C—O振动[9].
氨氮吸附后红外吸收峰有偏移,如吸附前3325,1645,1149,1103cm-1,吸附后分别为3342, 1649,1155,1101cm-1,对应的化学键有O—H、C=O和C—O,说明这几种化学键可能和吸附有关或受吸附的影响.爬山虎茎表面带负电荷的大小也是由其表面-COOH和—OH的数量所决定[10],因此—COOH和—OH可能是氨氮吸附的活性基团.而且,代表N-H和C-N振动的1552cm-1附近,在吸附前峰未分开,而在吸附后出现明显的小峰,证明吸附实验后氨氮已经结合于爬山虎茎表面.

2.2初始pH值对氨氮吸附的影响
pH值是影响氨氮吸附的重要因素,氨氮吸附量随初始pH值上升先增加后减小.氨氮吸附的最适初始pH值为5~9(图3).偏高和偏低的pH值都不利于爬山虎茎对氨氮的吸附.
在水溶液中,氨氮存在反应NH4++OH−↔NH3+H2O.Emerson等[11]曾报道溶液中氨氮的形态主要受pH值和温度的影响,氨氮溶液中[NH3]/[NH4+]=10pH−pK,而pK是一个仅与温度有关的常数,在25°C时其值为9.24.所以,当pH<7时溶液中NH4+为主要存在形式,当pH>7时,溶液中NH4+迅速减少,分子形态的NH3相应增加,因此不利于NH4+的吸附.另一方面,图1表明zeta电位随着pH值降低而增加,所以在溶液pH值降低时,爬山虎茎表面所带负电荷减少,静电引力减小,也不利于NH4+的吸附.所以pH值对爬山虎茎吸附氨氮的影响与氨氮形态特征和吸附剂表面特性都有关.这与前人用矿物吸附氨氮的研究结果基本一致.Karadag等[12]和Ji等[13]报道沸石和改性斜发沸石对氨氮吸附的最佳pH值分别为5~8和5~7.并且,他们认为在pH值降低时矿物对氨氮的吸附量之所以减少,是因为H+与NH4+对吸附材料表面活性位点的竞争.pH值降低爬山虎茎吸附氨氮减少也可能有这方面原因.

2.3吸附动力学
为探索氨氮吸附随振荡时间的变化趋势,采用25,100mg/L两个氨氮浓度进行吸附批实验,吸附剂添加量8g/L.所得爬山虎茎对氨氮吸附的动力学曲线见图4.随着吸附时间的增加,氨氮吸附先是缓慢增加,后急速增加,基本在18h进入吸附平衡.平衡时水中氨氮的去除率在氨氮浓度为25mg/L时为63.96%.3个阶段中氨氮吸附量急速增加的中间阶段(10~16h)是吸附的关键步骤.
动力学数据以Lagergren准一级方程、准二级方程和粒内扩散方程拟合[14],整体拟合效果都较差(R2<0.75,R2<0.38,R2<0.80).图4所示吸附过程明显可以分成3个阶段,3个阶段分别用粒内扩散方程进行拟合,结果见表1.吸附的关键步骤中间阶段符合粒内扩散方程(R2>0.95).多孔介质上的吸附过程通常有容积扩散、膜扩散、粒内扩散和溶质在表面的吸附4个步骤,其中可能决定着整个吸附速率及吸附容量的限速步骤为速度较慢的膜扩散或粒内扩散[15].当混合不均匀、吸附质浓度低、吸附剂颗粒细小、吸附质对吸附剂有很高的亲和力时,膜扩散成为限速步骤.反之,则粒内扩散成为限速步骤.因此爬山虎茎吸附氨氮的过程可能是膜扩散和粒内扩散综合作用的结果.吸附初始阶段由速率较慢的膜扩散控制,中间吸附速度较快的阶段由粒内扩散所控制,因此形成S形的动力学曲线.Lei等[16]研究表明沸石等矿物材料吸附氨氮也分为3个阶段,但由于初始阶段速度较快,研究者们经常把前2阶段视为同一阶段,所以动力学曲线一般是L型[3-4,12].矿物吸附氨氮过程多符合准二级方程,且粒内扩散通常为其主要控速步骤[17].

图4 接触时间对氨氮吸附的影响Fig.4 Effect of contact time on ammonia adsorption
2.4吸附等温线
从图5可见,氨氮的吸附量随初始氨氮浓度的增加而增加.在氨氮低浓度10mg/L时,氨氮去除率已达到100%,相应吸附量为1.25mg/g.氨氮吸附的等温线是经典的L型,因此用Langmuir和Freundlich两个模型进行数据拟合,拟合曲线见图5,计算出的参数值列于表2.Langmuir线性表达式为Ce/q=1/bqm+Ce/qm,Freundlich线性表达式为lnq=lnK+lnCe/n.其中,b(L/mg)和K(mg/g)分别是Langmuir和Freundlich常数,qm是单分子层最大吸附量(mg/g),n是与吸附强度有关的指数.3个温度下的等温线数据Langmuir模型(R2≥0.99)比Freundlich方程(R2≥0.91)更能描述等温吸附过程.Langmuir模型中qm表示单分子层理论最大吸附量,可以在一定程度反映吸附剂的吸附能力.在15,25,35℃下qm分别为3.18,4.69,5.19mg/g.表3说明,爬山虎茎吸附剂已经达到或超过天然矿物材料对氨氮的吸附水平.分离常数RL=1/(1+bC0)是Langmuir模型的另一个表达方式:0<RL<1表示良性吸附,RL>1表示不利于吸附,RL=1表示线性吸附,RL=0表示不可逆吸附[6].由于Langmuir模型中b>0,所以各浓度下均0<RL<1,爬山虎茎对氨氮的吸附属于良性吸附.Freundlich模型的1/n<1也说明,爬山虎茎对氨氮的吸附为良性吸附[6].

表1 粒内扩散方程对氨氮吸附拟合的相关系数Table 1 Correlation coefficient of intraparticle diffusion model in fitting the ammonia adsorption

图5 爬山虎茎对氨氮吸附的等温线Fig.5 Adsorption isotherms of ammonia nitrogen onto Boston ivy stem powder

表2 Langmuir模型和Freundlich模型的拟合常数Table 2 Parameters of Langmuir and Freundlich adsorption isotherms

表3 各种天然矿物材料对氨氮的最大吸附量Table 3 Maximum ammonia adsorption capability ofnatural minerals from Langmuir model
2.5吸附热力学
如图5所示,随着温度的升高,爬山虎茎对氨氮的吸附量增加,说明高温有利于氨氮的吸附.由公式Kd=(C0−Ce)V/(Ce×M)计算分配系数Kd,焓变ΔH°和熵变ΔS°的值由lnKd对1/T作图的斜率和截距通过公式lnKd=ΔS°/R−ΔH°/(RT)来计算,自由能变ΔG°则由公式ΔG°=ΔH°−ΔS°T计算[20].其中T是反应体系的开尔文温度(K),R是气体常数[8.314J/(mol·K)].由表4可见,ΔG°在所有氨氮浓度和温度下都是负值,表明过程是自发进行的,且随温度增加而有增加趋势.ΔH°都是正值,表明吸附过程是吸热的,所以升温有利于反应.ΔS°是正值说明氨氮吸附后体系的无序性增加.Yu等[21]认为物理吸附的自由能变范围为-20~0kJ/mol,而化学吸附自由能变为-400~-80kJ/mol,而Alkan等[22]认为化学吸附焓变为40~120kJ/mol,而物理吸附焓变则小于化学吸附焓变,经常为负值.本实验中爬山虎茎对氨氮吸附ΔG°在-2.78~ -14.24kJ/mol之间,ΔH°范围为3.65~17.15kJ/mol,因此爬山虎茎对氨氮吸附可能是物理吸附. Karadag等[17]通过热力学参数说明斜发沸石对氨氮的吸附也具有物理吸附的特点.

表4 氨氮吸附的热力学参数Table 4 Thermodynamic parameters of ammonia adsorption
3 结语
爬山虎茎对氨氮的等温吸附最符合Langmuir模型,理论最大吸附量在15,25,35℃下分别为3.18,4.69,5.19mg/g,达到或超过了矿物对氨氮的最大吸附量.18h吸附基本达到平衡,吸附前期控速步骤为膜扩散,后期控速步骤为粒内扩散.热力学结果证明爬山虎茎对氨氮的吸附属于自发的吸热反应.热力学结果还说明爬山虎茎对氨氮的吸附可能属于物理吸附.吸附的活性基团可能是-COOH和–OH.pH值影响了氨氮的形态和爬山虎茎表面电位从而影响到氨氮的吸附,吸附最适pH值为5~9.
[1] 温东辉,唐孝炎.天然斜发沸石对溶液中NH4+的物化作用机理[J]. 中国环境科学, 2003,23(5):509-514.
[2] Nguyen M L, Tanner C C. Ammonium removal from wastewaters using natural New Zealand zeolites [J]. New Zeal. J. Agr. Res., 1998,41:427-446.
[3] 王雅萍,刘 云,董元华,等.凹凸棒石粘土对氨氮废水吸附性能的研究 [J]. 农业环境科学学报, 2008,27(4):1525-1529.
[4] 张爱莉,朱义年,纪锐琳,等.竹炭对氨氮的吸附性能及其影响因素的研究 [J]. 环境科学与技术, 2008,31(6):19-21,50.
[5] Pagnanelli F, Mainelli S, Veglio F, et al. Heavy metal removal by olive pomace: biosorbent characterization and equilibriummodeling [J]. Chem. Eng. Sci., 2003,58:4709-4717.
[6] Ho Y S, Chiang T H, Hsueh Y M. Removal of basic dye from aqueous solution using tree fern as a biosorbent [J]. Process Biochem., 2005,40:119-124
[7] Eberhardt T L, Min S. Biosorbents prepared from wood particles treated with anionic polymer and iron salt: Effect of particle size on phosphate adsorption [J]. Bioresour. Technol., 2008,99:626-630.
[8] APHA (American Public Health Association), AWWA (American Water Works Association) and WEF (Water Environment Federation). Standard Methods for the Examination of Water and Wastewater [M]. 20th ed. Method 4500-NH3C. Washington D.C.: APHA, 1998:4–105.
[9] 卢涌泉,邓振华.实用红外光谱解析 [M]. 北京:电子工业出版社, 1989:21-34.
[10] Feng N, Guo X, Liang S. Adsorption study of copper(II) by chemically modified orange peel [J]. J. Hazard. Mater., 2009,164: 1286-1292.
[11] Emerson K, Russo R C., Lund R E. et al. Aqueous ammonia equilibrium calculation: effect of pH and temperature [J]. J. Fish. Res. Board Can., 1975,32:2379–2383.
[12] Karadag D, Koc Y, Turan M, et al. A comparative study of linear and non-linear regression analysis for ammonium exchange by clinoptilolite zeolite [J]. J. Hazard. Mater., 2007,144:432-437.
[13] Ji Z, Yuan J, Li X. Removal of ammonium from wastewater using calcium form clinoptilolite [J]. J. Hazard. Mater., 2007,141: 483-488.
[14] Karaca S, Gurses A, Ejder M, et al. Kinetic modeling of liquid phase adsorption of phosphate on dolomite [J]. J. Colloid Interface Sci., 2004,277:257-263.
[15] Ho Y S, Wase D A J, Forster C F. Kinetic studies of competitive heavy metal adsorption by sphagnum moss peat [J]. Environ. Technol., 1996,17:71-77.
[16] Lei L, Li X, Zhang X. Ammonium removal from aqueous solutions using microwave-treated natural Chinese zeolite [J]. Sep. Purif. Technol., 2008,58:359-366.
[17] Karadag D, Koc Y, Turan M, et al. Removal of ammonium ion from aqueous solution using natural Turkish clinoptilolite [J]. J. Hazard. Mater., 2006,136:604-609.
[18] Wang Y, Lin F, Pang W. Ammonium exchange in aqueous solution using Chinese natural clinoptilolite and modified zeolite [J]. J. Hazard. Mater., 2007,142:160-164.
[19] Liang Z, Ni J. Improving the ammonium ion uptake onto natural zeolite by using an integrated modification process [J]. J. Hazard. Mater., 2009,166:52-60.
[20] Chen C L, Wang X K. Adsorption of Ni(II) from aqueous solution using oxidized multiwall carbon nanotubes [J]. Ind. Eng. Chem. Res., 2006,45:9144-9149.
[21] Yu Y, Zhuang Y Y, Wang Z H. Adsorption of water-soluble dye onto functionalized resin [J]. J. Colloid Interface Sci., 2001,242: 288-293.
[22] Alkan M, Demirbaş O, Çelikçapa S, et al. Sorption of acid red 57 from aqueous solution onto sepiolite [J]. J. Hazard. Mater., 2004, B116:135-145.
致谢:感谢本单位徐仁扣研究员、马毅杰研究员、姜军老师、黄玉娟老师和袁金华博士等人在材料性质实验中的指导与帮助.作者简介:刘海伟(1981-),男,山东郓城人,中国科学院南京土壤研究所博士研究生,主要从事污染生态学研究.发表论文5篇.
Adsorption of ammonia nitrogen from aqueous solution by Boston ivy stem powder.
LIU Hai-wei1,2, LIU Yun1, WANG Hai-yun1, DONG Yuan-hua1*(1.State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China;2.Graduate University of Chinese Academy of Sciences, Beijing 100049, China). China Environmental Science, 2010,30(5):683~688
X171
A
1000-6923(2010)05-0683-06
2009-10-10
“十一五”国家科技支撑计划重点项目(2006BAD10B05);国家自然科学基金资助项目(20907058);江苏省自然科学基金资助项目(BK2008499)
* 通讯作者, 研究员, yhdong@issas.ac.cn
