功率超声处理甲基橙废水的实验研究
2010-09-03梁山景程建萍陈长琦
梁山景, 程建萍, 陈长琦
(1.合肥工业大学 资源与环境工程学院,安徽 合肥 230009;2.合肥工业大学 机械与汽车工程学院,安徽 合肥 230009)
随着印染与染料工业的发展,其生产废水量逐年增加,约占工业废水总排放量的1/10,全世界每年排放到环境中的染料污染物大约占其生产总量的15%,已成为全球主要环境污染源之一[1]。这类废水含有毒有害物质,CODCr浓度高,成分复杂,色度深且可生化性差,对环境危害极大,若不经过处理直接排放,将给生态环境带来严重的危害[2,3]。但是传统的污水处理方法处理染料废水效果很不理想[4]。超声氧化技术是近年来兴起的一种高级氧化技术,能有效地改善和去除染料废水中的有机物,受到人们越来越多的重视。但超声降解过程的反应机理十分复杂,偶氮染料大部分是结构复杂的有机化合物,降解过程不是一步完成的基元反应,而是由多步基元反应组成的复杂反应,因此准确地推导出超声降解的动力学模型与作用机理是非常困难的[5]。甲基橙是最简单的偶氮双苯环染料,因此用甲基橙作为偶氮染料的代表,更容易揭示超声降解偶氮染料的机理。本实验以甲基橙为研究对象,通过实验观察超声对甲基橙模拟废水的pH值、CODCr值的影响,对比加入自由基清除剂前后溶液的紫外光谱图形变化情况,并采用HPLC-MS检测中间产物,为揭示超声降解偶氮染料的反应机理提供一些基本的实验数据和理论依据。
1 实 验
1.1 实验仪器与试剂
实验仪器如下:超声波清洗槽式声化学发生器(其频率40 kHz、电功率400 W,三和超声波工程有限公司),pHS-3C型酸度计(上海分析仪器厂),HH-5化学耗氧量测定仪(江苏江分电分析仪器有限公司),UV1201-紫外/可见分光光谱仪(北京瑞利分析仪器公司),HP100型高效液相色谱-质谱仪。甲基橙、浓硫酸、氢氧化钠、正丁醇等试剂均为分析纯。甲基橙结构如图1所示。甲基橙的性质如下:pH≥4.4时,其主要显色团是偶氮基,显黄色;pH≤3.1时,其主要显色团是对醌基,显红色;3.1<pH<4.4时,水溶液显橙色。

图1 甲基橙结构
1.2 实验与分析方法
配制质量浓度为10 mg/L、pH值约为3.00的甲基橙模拟废水(其中采用硫酸和氢氧化钠调节酸度)[6-8],取1 L放入超声波发生器中,每隔30 min取1次样测脱色率,每隔20 min取1次样测CODCr。
模拟废水的pH值由pHS-3C型酸度计测定;CODCr值采用HH-5型化学耗氧量测定仪测定;对甲基橙废水进行波长 200~800 nm的紫外/可见光谱全程扫描,取最大吸收波长505 nm处的吸光度进行定量分析计算。甲基橙废水的脱色率为:E=(A0-At)/A0×100%,其中,A0为溶液的初始吸光度;At为溶液降解后的吸光度。最后采用高效液相色谱-质谱仪来联合测定超声降解甲基橙的中间产物。
2 结果与讨论
2.1 超声时间对超声降解效果的影响
2.1.1 超声时间对废水脱色效果的影响
超声时间对甲基橙模拟废水脱色效果的影响如图2所示。
甲基橙的紫外光谱图在505 nm附近有一明显的吸收峰,这是与苯环共轭体系特征吸收峰。图2中,从上到下依次是甲基橙废水经超声 0、30 、60、90、120、150 min 后的紫外光谱图,可以看到甲基橙溶液的特征吸收峰峰高在逐渐下降,说明甲基橙在超声过程中,共轭发色体系遭到超声破坏,吸光度变小,废水脱色明显。
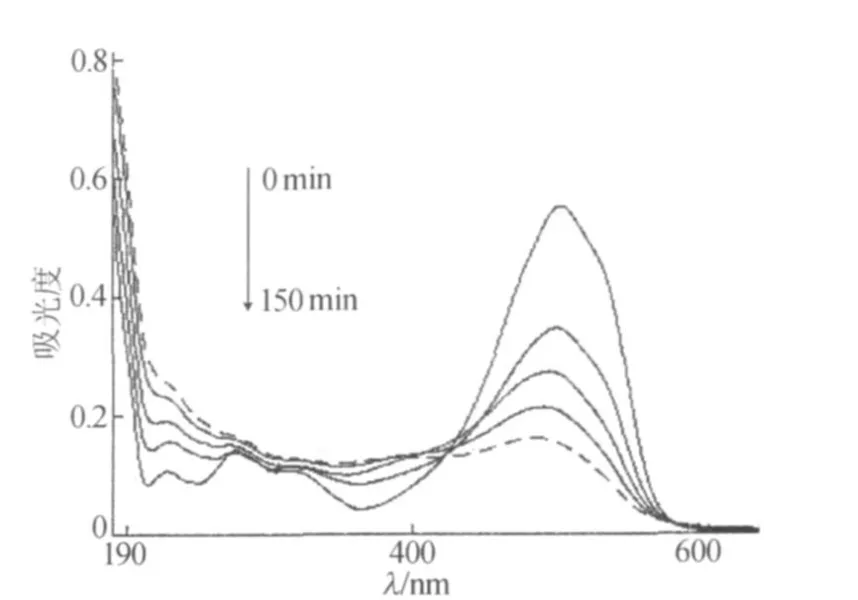
图2 超声时间对脱色的影响
2.1.2 超声时间对废水pH值的影响
超声时间对甲基橙模拟废水的pH值影响如图3所示。

图3 超声时间对溶液pH值的影响
图3 表明甲基橙废水的pH值随着超声时间的延长在一直下降,这说明在超声降解过程中可能有酸性物质产生,这与后续没有发现中间产物,甲基橙被直接氧化成CO2和H2O的结果符合。
2.1.3 超声时间对废水CODCr的影响
超声时间对甲基橙模拟废水的CODCr降解率的影响如图4所示。
从图4可以看出,经过180 min的超声降解,甲基橙的 CODCr降解率可达近70%,而且前100 min内,CODCr降解率随超声时间的增加上升很快,在超声100 min时,CODCr降解率就可达到60%左右,以后CODCr降解率随超声时间的变化不大,超声时间超过180 min后,再继续超声意义不大。这可能是由于甲基橙被不断降解、矿化,溶液中有机物浓度不断变小,溶液中有机物与◦OH和其它自由基接触的几率变小,从而导致超声一段时间后CODCr降解率变化不显著。
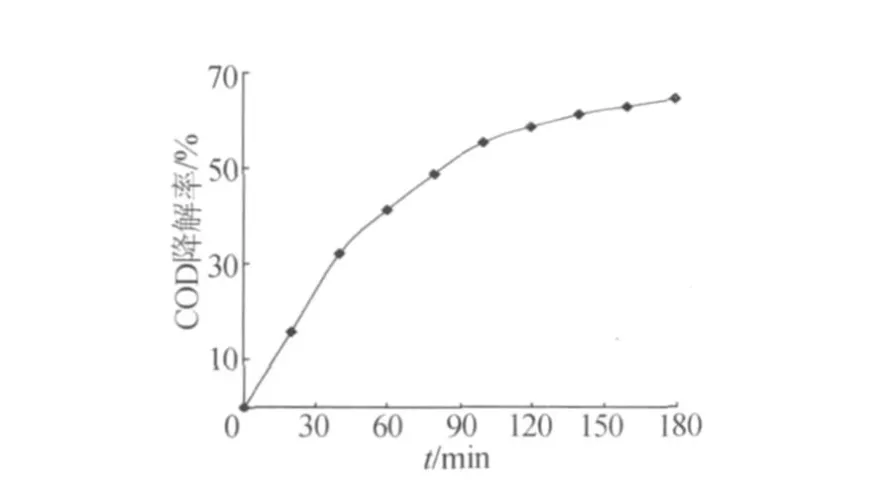
图4 超声时间对CODCr降解率的影响
2.2 甲基橙初始质量浓度和体系温度的影响
图5 所示表明经过180 min的超声处理,初始质量浓度分别为10、30、50 mg/L的模拟废水的脱色率分别达到84.4%、30.1%、26.8%。初始质量浓度越小,超声对其的脱色率越明显。这是因为对于极性难挥发溶质甲基橙染料,空化点随着溶液质量浓度升高而趋于饱和,从而降低反应速率,使脱色率降低。
体系的温度也直接影响着模拟废水的降解率,水温过高时,在声波负压半周期内废水会沸腾从而减小空化产生的高压,同时空化泡会立即充满水汽从而降低空化产生的高温,因而降低降解率。本实验所用超声波发生器为非恒温清洗槽式发生器,经实验测得在实验过程中温度会上升,然后保持平衡,全程温度保持在25~43℃之间,在此温度区间内,甲基橙降解速率无明显变化[9]。

图5 初始质量浓度对废水脱色率的影响
2.3 自由基清除剂对废水降解的影响
向甲基橙模拟废水中以体积比1∶1000的比例添加自由基清除剂正丁醇[10],进行超声对比实验,每间隔30 min取样,实验结果如图6所示。
从图6可以看出,未添加自由基清除剂正丁醇的甲基橙溶液超声后在505 nm处的吸光度下降明显,而添加了正丁醇的试样,吸光度变化很小,即脱色明显减弱,如未添加自由基清除剂正丁醇的试样通过180 min的超声处理,甲基橙脱色率达到了84%,而添加了正丁醇的试样,甲基橙的脱色率仅为31%。其原因可能是:甲基橙是亲水性难挥发的有机物,它很难扩散到疏水性的空化泡内直接被超声空化产生的高温所热解,主要是在本体溶液中和空化泡的气-液界面上被空化产生的◦OH等自由基所氧化,由于正丁醇的加入,消耗掉了声空化效应产生的◦OH等自由基,从而抑制了甲基橙的降解脱色反应。因此,推测甲基橙的主要超声降解方式是通过◦OH自由基氧化。

图6 自由基清除剂正丁醇对废水脱色的影响
2.4 HPLC-MS测定模拟废水的中间产物
高效液相色谱分析采用HP100型高效液相色谱-质谱仪(HPLC-MS)。色谱条件:色谱柱为Cl8BDS(250 mm ×4.6 mm ×5 μ m);进样量 5 μ L;流动相为:V甲醇/V水=9∶1;流速为 0.8 mL/min;紫外检测器,检测波长254 nm。质谱条件:干燥气流速为5 L/min,燥气温度350℃;雾化气电压2.1×105Pa;裂解电压37.5 eV[11]。测定结果如图7、图8所示。
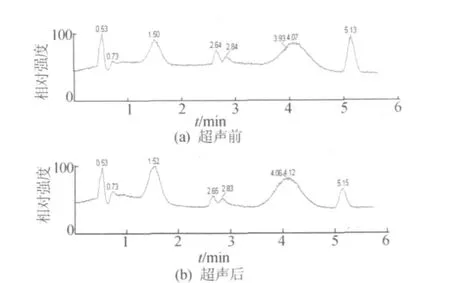
图7 超声前和超声180 min后的甲基橙试样的液相色谱分离图
对比图7超声前后甲基橙溶液的液相色谱图,2个试样除了在5.13 min左右处的出峰峰高有明显降低外,其它各峰均无明显变化,其原因可能是:5.13 min处的组分为甲基橙,在经超声处理后,5.13 min处峰高明显降低,甲基橙模拟废水被超声直接降解,没有新的峰产生,其它杂质峰也没什么变化,可以断定被超声降解的甲基橙被直接氧化成水和二氧化碳,无稳定的中间产物。
分析停留时间5.13 min峰的质谱,结果如图8所示。由于是在酸性条件下,甲基橙中的Na会离解,图8中质荷比 m/z为 305、224、215的峰的可能分子片段如图 9所示。因此可以确定5.13 min处的组分为甲基橙。


3 结 论
(1)对初始pH值为3.00,浓度为10 mg/L的甲基橙模拟废水进行超声降解,随着超声时间的延长,废水的pH值和色度不断减小,CODCr的降解率先快后慢。
(2)通过添加自由基清除剂等方法,推测出超声波降解甲基橙主要是通过◦OH等自由基氧化作用。
(3)甲基橙模拟废水被氧化分解,没有检测到稳定的中间产物,甲基橙最终被氧化成二氧化碳和水。
[1]王 侃,陈英旭,叶芬霞.SiO2负载的T iO2光催化剂可见光催化降解染料污染物[J].催化学报,2004,25(12):931-936.
[2]程建萍,陈长琦,殷福才,等.超声预处理强化印染废水的生物降解性[J].合肥工业大学学报:自然科学版,2008,31(10):1548-1551.
[3]Inoue M,Okada F,Saurai A,et al.A new development of dyestuffs degradation system using ultrasound[J].Ultrasonics Sonochemistry,2006,13(4):313-320.
[4]Rehorek A,Tauber M,Gubitz G.Application of power ultrasound for azo dye deg radation[J].Ultrasonics Sonochemistry,2004,11(3/4):177-182.
[5]Entezari M H,Mostafai M,Sarafraz-Yazdi A.A combination of ultrasound and a bio-catalyst:removal of 2-chlorophenol from aqueous solution[J].Ultrasonics Sonochemistry,2006,13(1):37-41.
[6]Okitsu K,lwasaki K,Yobiko Y,et a1.Sonochemical degradation of azo dyes in aqueous solution:a new heterogeneous kinetics model taking into account the local concentration of OH radicals and azo dyes[J].Ultrasonics Sonochemistry,2005,12(4):255-262.
[7]Wang Jun,Guo Baodong,Zhang Zhaohong,et al.Sonocatalytic deg radation of methyl orange in the presence of(nanometer and ordinary)anatase TiO2powders[J].Journal of Environmental Sciences,2005,17(3):414-418.
[8]岑科达,殷福才,程建萍,等.超声降解水溶性偶氮染料甲基橙的实验研究[J].合肥工业大学学报:自然科学版,2007,30(1):77-81.
[9]汤立新.甲基橙溶液的超声波降解研究[J].化学工业与工程技术,2003,24(6):16-17.
[10]Zheng Weixi,Maurin M,Tarr M A.Enhancement of sonochemical degradation of phenol using hydrogen atom scavengers[J].Ultrasonics Sonochemistry,2005, 12(4):313-317.
[11]张乃东,张曼霞,彭永臻.S2O82-派生氧化法催化降解水中的甲基橙[J].催化学报,2006,27(5):445-448.
