小鼠放射性肺损伤动物模型的建立与鉴定*
2010-08-14李梦侠曾林立杨镇洲
周 芊,王 东,李梦侠,曾林立,王 阁,杨镇洲
(第三军医大学大坪医院野战外科研究所肿瘤中心,重庆 400042)
放疗是胸部肿瘤最主要的治疗手段之一,而放射性肺炎(radiation pneumonitis,RP)作为胸部肿瘤放疗常见的严重并发症和剂量限制因素,其发生率达5%~15%,一旦发生,通常引起严重的临床后果[1]。因此,对放射性肺损伤病理过程及发生机制的研究越来越受到各国学者的重视,建立一种合适的放射性肺炎动物模型以及稳定、准确的鉴定方法是进一步深入研究所必须的。为此,本研究建立了放射性肺损伤小鼠动物模型,并对模型进行了病理组织学和血清学鉴定,为今后研究放射性肺损伤防护提供基础。
1 材料与方法
1.1 实验材料 体质量17~21 g成年健康雌性昆明小鼠72只,购自第三军医大学大坪医院野战外科研究所实验动物中心。数字化直线加速器(瑞典ELEKTA公司)、普通光学显微镜(BX-50,Olympus,日本)、蛋白核酸分析仪(美国Bio-Rad公司)、5804型台式冷冻离心机(德国 Eppendorf)、PROTEAN Ⅱ中型垂直电泳仪(美国 Bio-Rad公司)、TGF-β1小鼠单抗试剂盒(美国 Biosource)等。
1.2 全胸照射方法 速眠新Ⅱ(1.5 mg/kg)肌肉注射,全身麻醉小鼠,将小鼠仰卧位固定于治疗床上,以5 mm铅板防护动物头部和腹部。照射组小鼠使用直线加速器产生的8 m V X射线,经前胸野单次照射小鼠肺脏中平面 20 Gy,剂量率为200 cGy/min,动物与放射源距离为100 cm,射野范围为10 cm×10 cm。对照组小鼠给予麻醉后佯装照射。
1.3 鼠肺大体标本观察 于照射后1、3 d和1、2、4、8周6个时相点麻醉小鼠,先结扎气管再剖开胸腔分离主气管,并快速将气管及双肺剥离出胸腔,观察肺的大体结构改变。
1.4 组织病理学观察 选取小鼠右肺组织予10%甲醛固定,常规石蜡包埋切片,作HE染色和利用M asson三联染色(肺组织胶原纤维染色)评价肺组织切片纤维化程度,光镜观察病理组织结构改变。
1.5 酶联免疫(ELISA)法检测 于照射后1、3 d和1、2、4、8周6个时相点,每组取3只小鼠眼静脉血1.5~2 m L,25℃下放置30 min,4000 r/min离心5 min,取血清0.5 m L置于1.5 m L聚丙二醇试管内,血清转化生长因子(TGF-β1)含量测定按说明书进行操作。用包被缓冲液稀释兔抗鼠IgG单克隆抗体包被酶标板,稀释度分别为1∶5000、1∶10000、1∶20000、1∶40000,每一浓度包被 3个纵行,每孔100μL,4 ℃过夜,每孔均作复孔。次日,将酶标板洗涤3次,5%BSA封闭,每孔200μL,37℃孵育2 h,洗涤3次。在横行包被孔中依次加入阴性对照血清,弱阳性抗原液及强阳性抗原液,每孔100μL,37℃孵育1 h,洗涤3次。在每一包被浓度的一个纵行中分别加入按1∶2000、1∶5000、1∶10000稀释的上述多克隆抗体,每孔100μL,37℃孵育1 h,洗涤3次。在每一包被浓度的一个纵行中分别加入按1∶5000稀释的HRP标记羊抗兔IgG抗体,每孔 100μL,37℃孵育45 min,洗涤3次。加 TMB底物,室温避光显色 15~20 min,用2 mol/L H2SO4终止反应,读取OD450值。以OD值为纵坐标,以标准品浓度为横坐标,绘制标准曲线。根据血清样品的OD值在标准曲线上查出其浓度。
2 结 果
2.1 大体观察 小鼠全肺照射后4周,照射野内被毛明显脱落。解剖标本显示:对照组小鼠肺脏外观呈粉红色,表面光滑,弹性良好;照射组肺脏轻度肿胀、充血,表面和切面可见散在出血点,照射后8周全肺呈暗红色。

图1 小鼠肺照射后组织形态学改变(HE×400)
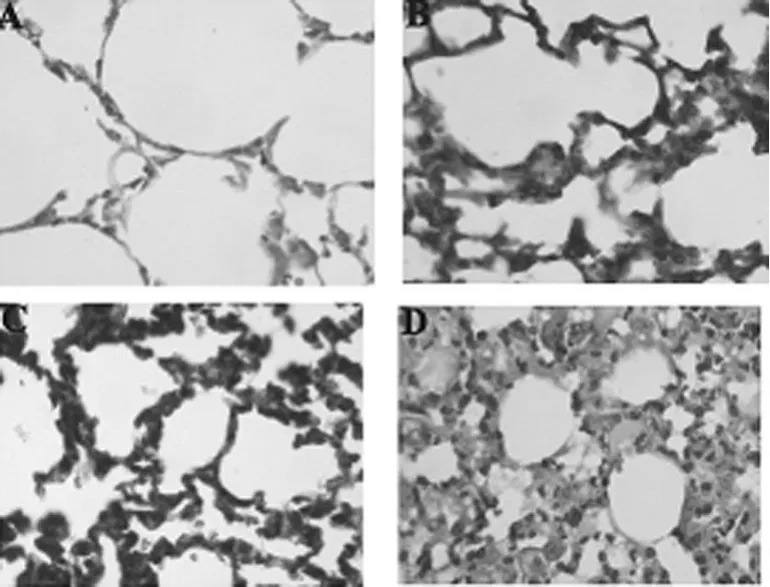
图2 小鼠肺组织Masson三联染色显示肺组织受照射后胶原纤维的变化(M asson×400)
2.2 HE染色和Masson染色组织学观察 对照组小鼠肺组织结构正常,肺间质未见充血,毛细血管壁完整,肺泡及细支气管腔无炎性渗出,见图1A。而照射组小鼠肺组织照射后1、3、7、14 d病变以渗出为主,肺间质及肺毛细血管充血、水肿,肺泡腔及细支气管内见较多的淋巴细胞,间质水肿致肺泡壁轻度增厚,部分肺泡间含水肿液,见图1B。照射后4、8周病变以慢性炎症为主,支气管和血管周围可见以淋巴细胞为主的炎症细胞浸润,肺泡壁增厚,肺泡腔变小,肺泡间隔及部分肺泡腔内可见纤维素样渗出物,见图1C。Masson三联染色:可见肺间质蓝色胶原纤维沉积,对照组可见少许纤维组织,见图2A;照射组照射后2周纤维组织开始增生,见图2B,照射后4、8周肺纤维化形成,肺结构紊乱,并可见大量染成绿色的胶原纤维,见图2C、D。
2.3 血清 TGF-β1检测结果 照射后 1周血清 TGF-β1含量明显增高,此后逐渐增高,第8周达高峰,与对照组比较差异有统计学意义(P<0.01),见图 3。
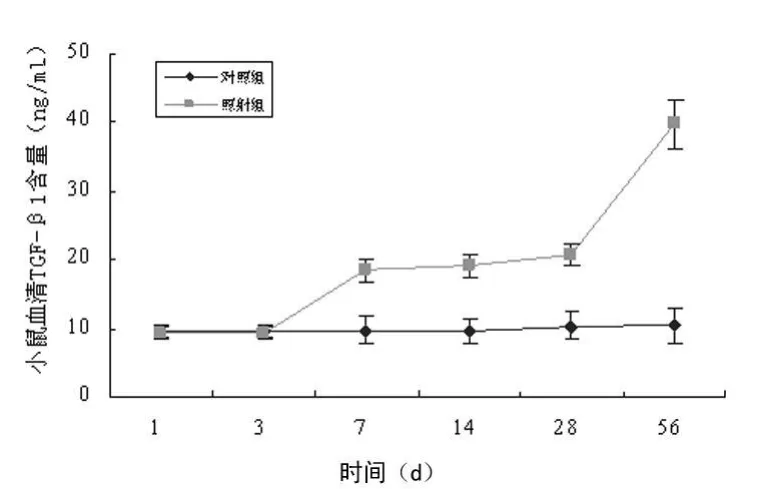
图3 各组小鼠血清TGF-β1含量检测
3 讨 论
放射性肺损伤动物模型建立对进一步研究放射性肺损伤机制及防治至关重要。综合遗传背景、操作难易程度、费用等因素,由于小鼠体积小、成本低,易于建立并方便快捷,目前认为建立放射性肺损伤鼠类动物模型比较适合且应用最为广泛。本研究应用昆明小鼠建立了放射性肺损伤模型,该小鼠特点是抗病力和适应力强、成活率高。
放射性肺损伤与照射剂量、受照体积和部位等因素相关,研究者可根据研究目的来选择照射剂量。进行放射肺损伤的长期效应研究,国外有学者给予4 Gy或7 Gy单次照射小鼠肺组织,应用呼吸频率和致死率来评价1年后放射性肺损伤,也有研究者采用13.5 Gy单次照射小鼠并持续观察24周[1-2]。杨明会等[3]报道对比大鼠一次性给予30 Gy或3 Gy、每周2次、总剂量30 Gy的照射,组织学证实两组均能引发典型的放射性肺炎和肺纤维化,但26周后发现小剂量多次照射组大鼠存活率高。对放射肺损伤进行短期研究,目前多采用大分割单次照射法。孟玲玲等[4]采用6 m V X线单次照射小鼠右肺30 Gy,观察至照射后2个月。虽然小剂量多次照射被认为更符合临床常规治疗剂量,但目前大家也逐步开始关注全身立体定向治疗时的大分割照射,故在本实验中仍采用20 Gy全肺单次照射构建放射性肺炎模型。本研究结果表明,通过全肺20 Gy单次照射雌性昆明小鼠,成功地复制出典型的放射性肺炎小鼠动物模型。
国内外学者研究认为放射性肺损伤的病理形态学改变主要是肺间质充血水肿,肺泡内渗出物增加,炎细胞浸润,后期纤维结缔组织增生,肺泡萎缩[5-6]。本研究结果基本与之相符,照射组2周内以渗出为主,4周后病变以慢性炎症为主,肺泡间隔及部分肺泡腔内可见纤维素样的渗出物。因而,通过病理观察证实本放射性肺炎小鼠模型成功建立。目前比较认同的放射性肺损伤发生的机制为放疗产生的活性氧直接作用于实质细胞并通过改变细胞因子的微环境而启动一系列的“分子级联”反应,随着活性氧自由基的增多,导致脂质过氧化、DNA和蛋白质的氧化以及致炎因子的进一步激活,最终导致纤维化形成[7-8]。国内外学者对这些生物因子进行了大量研究,目前比较一致的观点认为血清TGF-β1水平可以作为放射性肺损伤的预测因子,与急性放射性肺炎尤其是放射性纤维化密切相关。本实验发现放疗后小鼠血清TGF-β1含量呈现逐渐升高过程,与对照组比较差异有统计学意义(P<0.01),这与Machtay等[2]研究结果类似,只是在发生改变所对应的时相点和含量的高低上有所差别。
[1]T ravis EL,De Luca AM.Protection of mouse lung by WR-2721 after fractionated doses of irradiation[J].Int J Radiat Oncol Biol Phys,1985,11(3):521.
[2]Machtay M ,Scherpereel A ,Santiago J,et al.Systemic polyethylene glycol-modified(PEGylated)superoxide dismutase and catalase mixture attenuates radiation pulmonary fibrosis in the C57/bl6 mouse[J].Radiother Oncol,2006,81(2):196.
[3]杨明会,张利军,冯林春,等.小剂量多次照射大鼠放射性肺损伤模型的评价[J].军医进修学院学报,2006,27(6):415.
[4]孟玲玲,冯林春,石怀银,等.苦参碱防治放射性肺损伤的实验观察[J].军医进修学院学报,2008,29(2):134.
[5]Szabo S,Ghosh SN ,Fish BL ,et al.Cellular inflammatory infiltrate in pneumonitis induced by a single moderate dose of thoracic x radiation in rats[J].Radiat Res,2010,173(4):545.
[6]Kiazimov KI.Pathogenesis,diagnostics and treatment of radiation pneumonitis induced by radiotherapy of lung cancer[J].Georgian Med New s,2009,174:115.
[7]Ghafoori P,Marks LB,Vujaskovic Z,et al.Radiation-induced lung injury.Assessment,management,and prevention[J].Oncology(Williston Park),2008 ,22(1):37.
[8]Zhao W,Robbins ME.Inflammation and chronic oxidative stress in radiation-induced late normal tissue injury:therapeutic implications[J].Curr Med Chem,2009,16(2):130.
