用于评估心室辅助装置的人体循环系统半实物仿真模型
2010-08-08作者李虹磊杨明李世阳
【作者】李虹磊,杨明,李世阳
上海交通大学仪器科学与工程系,上海, 200240
心脏由于各种原因导致其泵血功能下降,心室辅助装置用人工制造的机械装置,部分或完全替代心脏的泵血功能,保证全身组织和器官的血液供应[1]。自心室辅助装置的研究开始以来,国内外研究者相继进行了各种方法的心室辅助在体实验(包括动物实验与临床试验),但在体实验的风险大、费用高且不易重复进行。在心室辅助装置的设计和评估过程中,体外模拟实验是在体实验的一个重要补充和替代。在心室辅助装置的在体实验中,辅助装置与实际心血管系统相互作用的效果往往决定了整个系统工作的成败。因此,在体外模拟实验中,要完全真实地模拟出在体实验中心血管系统与辅助装置相互作用的生理环境,便成了研究的重点,也是难点。
目前,在心室辅助系统体外模拟实验中采用的仿真方法主要包括:① 数学模型研究,即将建立的心室辅助装置动态数学模型,嵌入到原有的心血管系统数学模型中,进行数学模型交互研究[2-3]。② 物理模型研究,即在模拟心血管系统的物理实验平台上进行辅助装置的实物仿真[4-6]。对于纯粹的数学建模研究方法而言,心血管系统的数学模型历经长时间的发展,已经比较细化且成熟,如哈佛-麻省理工(Harvard-MIT)的RCVSIM (Research Cardiovascular Simulator)[7-8];然而对心室辅助装置建立的数学模型却往往是复杂且不准确的。这是因为器件与心血管系统的相互作用取决于物理特性,如非线性摩擦力等各种影响其能量有效传递的因素,而这些特性往往难于建模。而且,样机阶段对器形结构的反复修改也不适于采用固化的数学模型。在物理实验平台上进行心室辅助装置流体力学研究也存在类似的问题。人体心血管系统不仅异常复杂,而且影响血液循环动力学性能的各种因素互相影响,但模拟心血管系统的物理实验平台却往往采用简化的物理水力模型,仅从辅助装置流体负载的角度来仿真。因而,虽然在物理平台上采用心室辅助装置实物进行测试具有准确直观的效果,但是物理模型仍然不能准确地反映出心室辅助装置对心血管系统的血液动力学影响。
本文在上述两种体外模拟实验的仿真方法的基础上,提出了将心室辅助装置实物在成熟的心血管循环系统数学模型上进行实时评估的半实物仿真(Hardware-in-the-loop Simulation)方法,并将该方法用于气动直接心室辅助装置样机的体外评估。对实际设计的心室辅助装置对于心血管系统的辅助效果进行有效的评价,更加真实地再现直接心室辅助装置系统的工作状态,有助于及时发现和改进心室辅助装置自身设计的缺陷,可对结构和控制算法进行优化。
1 半实物仿真系统的构建
1.1 半实物仿真系统的组成
半实物仿真,又称为硬件在回路(Hardware-In-Loop,HIL)仿真,是指在数学仿真模型中,把部分仿真模型用实物代替的一种实时仿真。这种方式特别适用于当某些系统的部件和现象尚无合适的模型或难以建模时,可以用物理部件作为仿真模型的一部分。将硬件和软件系统相结合的半实物实时仿真,比纯数学模型仿真更接近实际,逼真性好,实用价值大,且仿真过程更加灵活,仿真结果有更高的可信度[9-10]。其常应用于工程领域,如导航制导与控制、飞行器设计等方向。本文将该仿真思想用于对设计的心室辅助装置进行实时有效的体外实验评估,于活体实验之前获得较为准确的器械的工作特性,可大大缩短了医疗器械的设计周期。
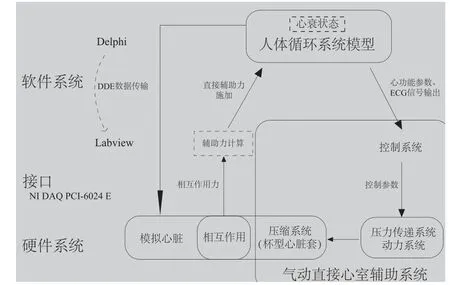
图1 气动直接心室辅助下的人体循环系统半实物仿真系统框图Fig.1 The structure of the hardware-in-the-loop simulation of the DMVA-assisted cardiovascular system
基于半实物仿真思想,对新设计的气动直接心室辅助装置样机进行工作性能测试。仿真平台的整体框图如图1所示。该系统由气动直接心室辅助装置(包括控制器、气体致动器、传感器和软质心脏套杯件)、模拟心脏和上位机的人体循环系统模型仿真软件组成。杯型心脏套包裹在模拟心脏外,通过气体致动,与自然心跳同步地施加挤压力和膨胀力来辅助心脏泵血和回血。同时,通过传感器记录作用力,作为对心脏的直接辅助力实时送入不同心衰程度下的人体心血管数学模型。该辅助力也构成了本半实物仿真系统的一部分接口。经过仿真计算得到的辅助作用下的血液动力学参数,作为反馈送入辅助装置的控制器,以此研究该装置对不同心衰状况下的心脏的实时辅助效果,为进一步的反馈控制提供依据。
1.2 直接心室辅助下的心血管循环系统数学模型
目前,心血管系统建模常分为分布参数模型和集中参数模型两种。集中参数模拟电网络模型因其简洁实用,在心室血液循环系统的工作机理、控制等方面的研究中有广泛的应用[11]。本研究根据该半实物仿真系统的需要,在RCVSIM[15]和PHYSBE[12]等成熟的心血管系统集中参数电网络模型的基础上加以改进和发展,侧重在左右心室(软硬件接口处)进行细化,而在体周循环处则采用集中式简化模型,将头、躯干、手臂和腿一并作为外周循环考虑,以便更好地仿真出各种心力衰竭疾病对心脏四个腔室的生理影响,及更具体地评估直接心室辅助的效果。同时,在循环系统模型的基础上,将直接心室辅助装置等效为两个分别与左右心室串联的电压源[13],建立了直接心室辅助下的人体心血管系统数学模型(如图2)。
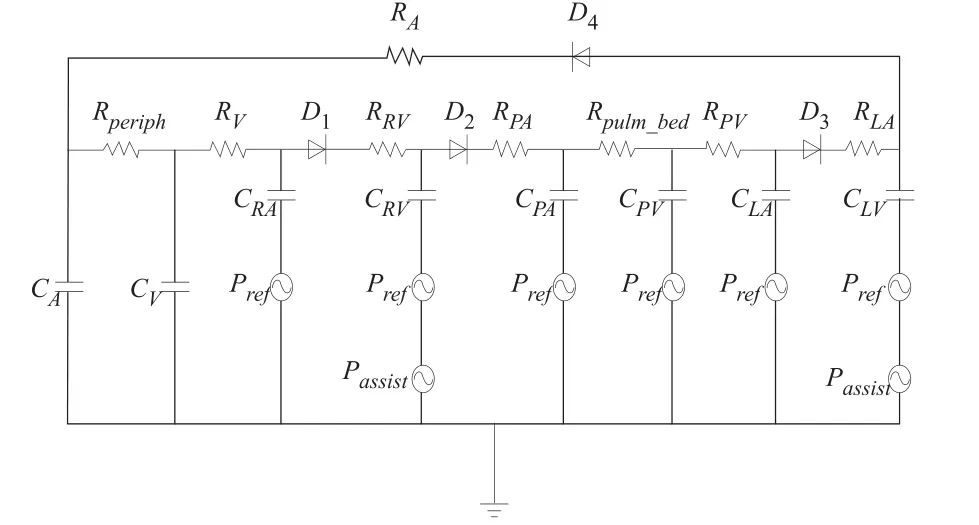
图2 加入直接心室辅助的人体心血管模型Fig.2 DMVA-assisted human cardiovascular model
本模型包含:心脏的左右心室(下标LV, RV)和左右心房(LA, RA);系统动、静脉血管(A, V)和周身毛细血管(Periph);肺循环的动、静脉血管(PA, PV)和肺部毛细血管(Pulm_bed);粘性血液的流阻R;血管顺应性C;血流流量Q;人体的心脏瓣膜(表示二尖瓣、肺动脉瓣、三尖瓣和主动脉瓣)。在该模型中,人体的动脉与静脉单元之间通过集中的外周循环单元将其沟通,并将左心室作为动脉系统的源,右心房作为静脉系统的汇流点,再由肺循环将左右心部分连接起来,形成一个闭环的循环系统。该模型中的流阻参数和血液顺应性选于参考文献[14]中的结构参数;心室压、肺循环的动静脉血压的参考压力都是胸内压Pref;心脏的泵血功能采用Suga和Shroff等人提出的改进的泵模型[4],[15]:左右心室的压力-容积(P-V)关系由时变倒电容EHV(t)来表示,心室顺应性CHV随时间周期变化,(周期的大小决定于收缩末期、舒张末期的顺应性以及心律的大小);心肌的阻抗特性RHV则反映了心室的瞬时血流对其内压力的影响,它们之间的关系为:
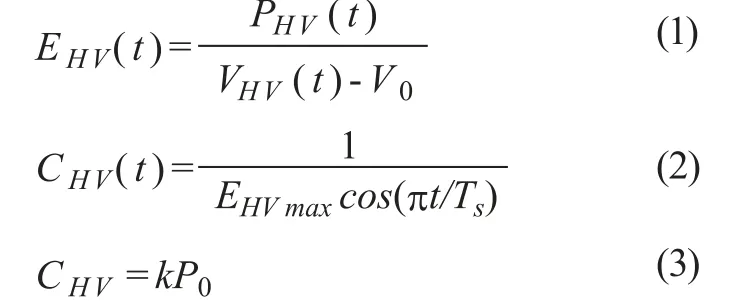
式中,VHV(t)为左(右)心室的血容量,V0为左(右)心室无压力时的血容量,Ts为心动周期的收缩时间,P0为等容收缩压力。
利用上述动态模型,可计算任一点的血流和血压波形,任意时刻全身血液分布状况,并可将外部作用(如本文的直接心室辅助压力)耦合到模型上,通过仿真实验来观察外部作用与生理循环的关系和相互作用规律。由于直接心室辅助装置直接作用于心室表面,其作用力与自然衰竭心脏的心肌收缩力串联叠加、共同起作用[13]。因此,可在上述人体心血管系统电网络模型的基础上,将直接心室辅助装置等效为两个分别与左右心室串联的电压源,电压源的值为辅助力,由外部的压力传感器采集输入。这样一个在直接心室辅助下的人体心血管系统半实物仿真回路便构成了。当需要仿真正常的心血管循环系统时,将模型中的直接心室辅助压力源(Passist)作短路处理,并将电路相应参数从心衰状态恢复到正常状态[13]。直接心室辅助在衰竭心脏上的总体作用可以表示为:
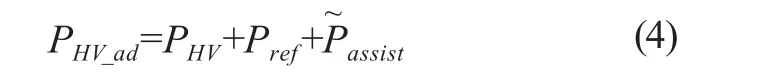
式中,PHV表示左(右)心室衰竭心肌自然收缩压力,Pref表示参考胸内压,表示左(右)心室辅助对左(右)心室的作用压力。
1.3 软硬件接口
本系统的人体心血管系统软件模型通过接口与硬件直接心室辅助装置相连。对于直接心室辅助而言,辅助装置与心脏表面的相互作用尤为重要,但由于该相互作用力难以准确建模,必须通过实际物理测试得到。本系统中,通过将辅助作用力施加到一个模拟心脏实物上进而实现对该力的测量。承受该作用力的模拟心脏便成为本系统软硬件的接口。
为了实现最佳地控制施加于心肌的压力,心室辅助装置缩胀腔室设计成贴合心脏外形的杯状心脏套,由生物相容性较好的柔性材料制成,并在结构设计上保持了最低刚性。这样,缩胀腔室的变形主要决定于心肌的机械特性,保证了即使在很大充盈容量下,缩胀腔室的压力仍能与施加于心肌上的压力相近似,从而使动力单元产生的能量几乎全部传递给心肌[17]:

其中,Pi表示任意时刻的杯形件腔室内压,沿腔室膨胀方向的力为正,沿腔室收缩方向的力为负。Pvi表示对应时刻的模拟心脏内的心室压,△Pi表示进行有效腔室膨胀的杯形件腔室内压力的增或减量。
如前所述,压缩腔室的压力差在任何充盈度下都接近于施加在心肌上的压力,因此采用精密气压计采集杯形件压缩腔室和模拟心脏内的压力Pi和Pvi,并结合材料特性以及实验测试,取一损耗参数δ,则有效施加在心肌上的辅助压力为:
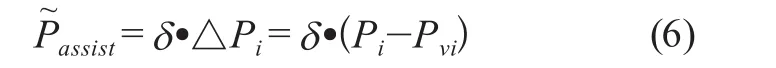
2 实验方法及结果
2.1 实验方法
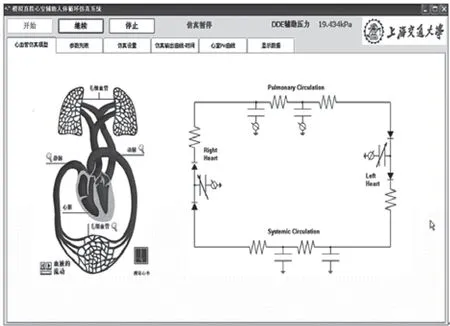
图3 加入直接心室辅助的人体心血管模型程序界面Fig.3 User interface of human cardiovascular model with DMVA
本文的软件模型均以图2中加有直接心室辅助的人体循环系统电网络模型为基础,采用图形化用户界面友好的Delphi语言实现,成为可动态实时运行的循环模型(如图3)。仿真的对象是左心室局部缺血的心衰患者,设定缺血率为33%,通过将左心室的顺应性下降到正常值的33%来仿真[16]。对照组为正常人。心率保持为70 bps,心动周期为0.8 s,收缩占空比为40%,其中收缩约0.3s,舒张约0.5s。计算步长为0.001 s。在每一个时间间隔内,从左右心室开始依次计算和更新每一个模块的血压和血流量。
软件和硬件的接口以及对硬件系统的反馈控制采用Labview语言实现。杯形件的腔室内压和模拟心脏的心室压由气压传感器实时采集,通过NI的PCI6024E板卡上的模拟输入端输入到Labview程序进行分析处理,而后通过DDE数据传输直接导入到人体模拟循环系统的Delphi程序中。由Delphi程序仿真得到的心功能参数经过分析处理,作为反馈控制的参数也通过同样的数据通道从板卡的模拟输出端实时输出。
需要注意,直接心室辅助装置是通过直接加载外力作用于心肌表面实现辅助泵、回血的,因此必须严格控制与自然心率同步作用,否则可能会进一步削弱心脏的泵血功能,甚至对心肌表面造成损伤。在本实验中,同步控制信号由人体模拟循环系统的上位机软件根据设定的心率、收缩期占空比等参数而定,并经由NI板卡的AO端输出。
开始实验前,将辅助装置的气动杯形件通过柔性网袋固定在模拟心脏上,将模拟心脏的液囊充盈到体积最大状态,同时让辅助装置的杯形件处于完全排空状态,用真空泵抽气的办法使杯形件与模拟心脏外囊紧密贴合。开始实验,通过程序控制,使模拟心脏工作在循环系统软件模型设定的心衰状态下。当其血液动力学指标趋于稳定后,启动气动直接心室辅助系统,与自然心跳同步地施加辅助压力,经过4-5个心跳周期,整个系统重新归为稳态,此时开始记录各种反映心功能的生理指标。为了全面评估施加直接心室辅助的血液动力学效果,需要观测的指标包括:左右心室的压力、容量、主动脉的压力和心输出量。此外,压力容积环(P-V Loop)也是评价心脏血液动力学功能的有效手段。
2.2 实验结果与讨论
严重心力衰竭在辅助前后的心功能状态可以从图4-5中获得。正常状况下,主动脉高压90~140 mmHg,低压60~90 mmHg,左心室收缩压略高于主动脉高压,左心室舒张末期压力为0~10 mmHg[18,19]。当心力衰竭时,左心室舒张末期的压力将高于17.97 mmHg。此外,当心衰发生时,心肌收缩力下降,左心室舒张末期和收缩末期容积同时增加,此时P-V环面积较正常状态相对减小[1]、[18]。严重心衰时的血液动力学仿真结果如图4所示,左心室压力最大约99.72 mmHg,左心室舒张末期压力约21.21 mmHg,主动脉压力在75.42~99.72 mmHg之间,这些结果均与文献[1]、[18]、[19]的结论一致。通过半实物仿真施加直接心室辅助后的结果如图5所示,左心室压力最大值回升至124.45 mmHg, 左心室舒张末期压力约为8.44 mmHg,主动脉压力大约在90.70~124.45 mmHg之间,同时P-V环的面积也相对图4心衰状态有所增大,表明心输出量也随之增大。通过计算得出,加入心室辅助装置前后的心输出量由原先的4.52 L/min回升至5.65 L/min。这些也均与文献[1]、[18]、[19]中的健康人血液动力学指标相近似。
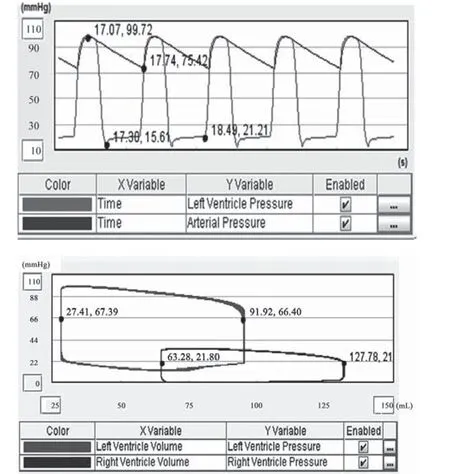
图4 心力衰竭状态下左心室压、主动脉压及左右心室压力容积环曲线Fig.4 Left ventricular, arterial pressure and P-V loop of both ventricles under CHF
以上半实物仿真的结果表明该直接心室辅助装置能够有效地辅助心脏泵血,改善心衰病人的血液动力学指标, 如心输出量的提升,对舒张期回血量的促进等。在本心室辅助系统中,致动医用电磁阀组件的响应速度是关系到辅助装置与心动周期同步的核心技术,必须结合电磁阀组的实际响应性能调整触发控制时机,适应心律的不断变化,准确地实现与心动周期同步。
3 结论及展望
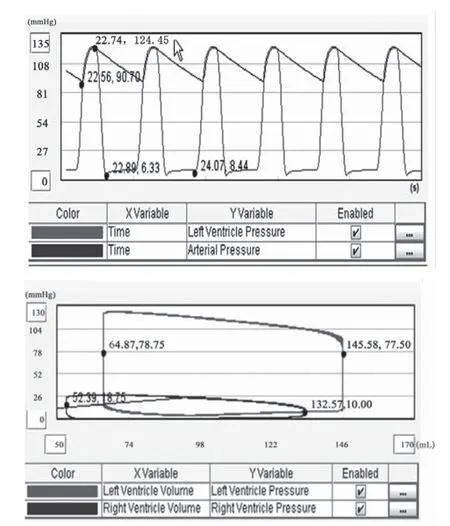
图5 心衰状态施加直接心室辅助下左心室压、主动脉压及左右心室压力容积环曲线Fig.5 Left ventricular, arterial pressure and P-V loop of both ventricles under DMVA-assisted CHF
上述实验证明了用半实物仿真的方式评估和改进心室辅助装置(尤其从控制方法的角度)的可行性和优势,与动物实验相比,其重复性好,且方便建立不同心功能状况的模型,可在短时间内进行大量的实验;与纯数学建模仿真相比,其建立在实体装置的物理特性基础上,实时呈现心室辅助装置与心脏的动态交互作用。
在今后的工作中,用于半实物仿真的人体心血管系统模型可以进一步细化,尤其是在辅助作用施加的心脏四个腔室部分。此外,还需补充冠脉循环单元,以分析辅助压力对冠脉血流的影响。还可以进一步考虑包括动脉反馈系统、心肺循环反馈系统和神经系统对呼吸和心率耦合机制等在内的一系列调节机制。当然,模型的复杂化必须与计算的时效性相平衡,以实现实时反馈控制的半实物仿真的需求。
[1]马爱群.心力衰竭[M].北京:人民卫生出版社.2004.
[2]Wu Y., Allaire P., et al.An advanced physiological controller design for a left ventricular assist device to prevent left ventricular collapse[J].Artificial Organs.2003, 27:926–30.
[3]Ferrari G., Kozarski M., et al.modelling of cardiovascular system: development of a hybrid (numerical-physical) model[J].Artificial Organs.2003, 26(12):1104–14.
[4]白净.生理系统的仿真与建模[M].北京:清华大学出版社.1994
[5]Wu Y., Allaire P., et al.In-vitro test of an adaptive flowcontroller for a continuous flow LVAD[J].In: Proceedings of American control conference.2004, 1647–1648.
[6]Kozarski M., Ferrari G., et al.A hybrid mock circulatory system: development and testing of an electro-hydraulic impedance simulator[J].Artificial Organs, 2003, 26(1):53–63.
[7]Goldberger AL, Amaral LAN, et al.PhysioBank, PhysioToolkit,and PhysioNet: Components of a New Research Resource for Complex Physiologic Signals[J].Circulation.2000, 101 (23):215- 220.
[8]Research Cardiovascular Simulator (RCVSIM) of Harvard-MIT.http://www.physionet.org.
[9]Ersal T., Fathy H.K., et al.A review of proper modeling techniques[J].Journal of Dynamic Systems, Measurement and Control, Transactions of the ASME 2008130 (6): 0610081-06100813.
[10]刘延斌、金光,半实物仿真技术的发展现状[J].光机电信息.2003, 1:27-32.
[11]Melchior FM, Srinivasan RS, et al.Mathematical Modeling of human cardiovascular system for simulation of orthostatic response[J].Am.J.Physiol (Heart Circ.Physiol.) 1992262(31):1920-1933.
[12]McLeod J, PHYSBE: a physiological simulation benchmark experiment[J].SIMULATION, 1966, 7, 6, 324-329.
[13]李世阳,杨明,等.心力衰竭及其在直接心室辅助下的建模仿真研究 [J].上海交通大学学报.2008, 42(5): 817-821.
[14]T Heldt, EB Shim, et al.Computational modeling of cardiovascular response to orthostatic stress[J].J.Appl.Physiol..2002, 92(3):1239-1254.
[15]陈丽琳,吴效明,等.心血管循环系统的建模仿真[J].北京生物医学工程.200625(3): 256-260.
[16]Ferrari G, Kozarski M, et al.modelling of cardiovascular system: development of a hybrid (numerical-physical) model.Int[J].J.Artif.Organs, 2003, 26(12): 1104-14.
[17]李卫民.直接机械性心室辅助[J].实用心脑肺血管病杂志,2002.4,10(2): 111-114.
[18]张子彬.充血性心力衰竭[M].北京:科学技术文献出版社,1997, 1-129.
[19]柳兆荣,李惜惜.血流动力学原理和方法[M].上海:复旦大学出版社,1997, 333-339.
[20]B.Hanson, M.Levesley, et al.Hardware-in-the-loopsimulation of the cardiovascular system, with assist device testing application[J].Medical Engineering & Physics, 2007, 29(3):367-374.
[21]F.M.Colacino, M.Arabia, et al.Modeling, analysis, and validation of a pneumatically driven left ventricle for use in mock circulatory systems[J].Medical Engineering & Physics 2007, (29): 829-839.
[22]杨明,臧旺福.直接心室辅助致动方法的现状与发展 [J].生物医学工程学进展,2008, 29(1): 37-41.
