盐酸青藤碱延迟起释型缓释片释药的处方和工艺影响因素
2010-07-25耿燕娜
耿燕娜, 张 瑜
(1.河南大学药物研究所,河南 开封475004;2.河南大学淮河医院,河南开封475000)
口服择时释药系统是近年来发展的新型控释制剂,选择在疾病发作的时候,在预定的时间内自动释放有效剂量的药物,从而保证疗效,降低药物毒副作用,提高病人顺应性[1],主要包括择时缓释释药和择时脉冲释药两大类,其中择时缓释释药具有时滞后缓慢释药特性,可实现择时释药,同时在较长时间内维持稳定的血药浓度,减少用药次数,因此,成为口服择时释药系统研究的热点。关节炎及类风湿性关节炎患者的关节僵硬呈现昼夜节律变化,在凌晨3点左右加重,俗称“晨僵”[2]。如果患者在睡前服用延迟起释型缓释制剂,药物在预定的滞后时间(疾病发作前)释放,可有效预防和治疗疾病,并且时滞后药物缓慢释放,长时间有效维持平稳血药浓度,减少药物可能引发的副作用。盐酸青藤碱是从中药青风藤中提取的有效生物碱单体,药用多为其盐酸盐,主要用于治疗风湿、类风湿性疾病,疗效显著[3]。本文以干法包衣技术制备盐酸青藤碱延迟型缓释片,考察片芯骨架材料的种类(HPMC K15M、HPMC K4M、黄原胶和卡拉胶)和用量、外层衣膜骨架材料的种类和用量、衣膜材料制备工艺、缓释片硬度等因素对制剂释药情况的影响,为制备符合时辰治疗要求的盐酸青藤碱延迟型缓释片提供实验基础。
1 仪器与药品
RCZ—8A智能药物溶出仪(天津大学精密仪器厂);UV-2000型紫外可见分光光度计(尤尼柯上海仪器有限公司);17冲旋转式压片机(上海天和制药机械厂);78X片剂四用测定仪(上海黄海药检仪器厂);盐酸青藤碱(西安赛邦医药科技有限公司,纯度98%以上,批号20070802);羟丙基甲基纤维素(HPMC K15M、HPMC K4M,上海 colorcon公司赠送);卡拉胶(CKC101,成都协力魔芋科学种植加工园有限公司);黄原胶(山东阜丰发酵有限公司);其它辅料均为药用级。
2 方法和结果
2.1 盐酸青藤碱延迟起释型缓释片的制备
2.1.1 片芯的制备 将盐酸青藤碱与骨架材料、淀粉等辅料混合均匀,采用粉末直接压片法制备7 mm平冲片芯(每片含盐酸青藤碱120 mg,片重180 mg)。
2.1.2 外层衣膜材料的制备 湿法制粒:将骨架材料、淀粉等辅料混合均匀,加入适量15%聚乙烯吡咯烷酮(w/v)乙醇溶液制软材,过40目筛制粒,50℃干燥,整粒,加入1%(w/w)滑石粉,混合均匀,备用。
粉末直接混合:将骨架材料、淀粉及处方中其他辅料混匀,备用。除考察包衣层衣膜材料制备工艺影响外,其他影响因素考察时均采用粉末直接混合制备衣膜材料。
2.1.3 延迟缓释片的制备 将半量的外层衣膜材料置10 mm冲模中,铺平;然后将盐酸青藤碱片芯置于模孔中央,轻压使片芯一半进入衣膜层中,再将半量衣膜材料加入冲模中,压片,即得(外层衣膜重270 mg)。
2.2 标准曲线的制备 精密称取干燥至恒重的盐酸青藤碱对照品适量,用纯化水稀释配制系列浓度盐酸青藤碱溶液(分别为 2.03、4.06、8.12、16.24、32.48、48.72 mg/L),在265 nm 波长处测定吸光度,以吸光度A对浓度C进行线性回归,得标准曲线方程:
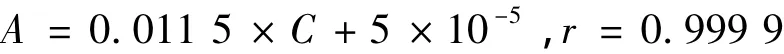
表明在纯化水中,盐酸青藤碱浓度在2.03~48.72 mg/L内,吸光度与其浓度间线性关系良好。
2.3 体外释放度的测定 取盐酸青藤碱延迟缓释片,按《中国药典》(2005版)二部附录XC项下第一法(转篮法),以新鲜脱气纯化水为释放介质,体积500 mL,转速(100 ±1)r/min,温度(37 ±0.5)℃,分别于 2、4、5、6、7、8、9、10、12、15 和 24 h 取样 5 mL(同时补充等量新鲜介质),滤过,取续滤液适当稀释后于265 nm波长处测定吸光度,计算药物累积释放百分数。
2.4 延迟缓释片释放度数据处理
2.4.1 释药曲线相似性评价 目前,对于药物释放曲线的相似性评价,多采用由Moore和Flanner提出的相似因子(f2)法,此法已被FDA指导原则所采用[4]。f2值的计算公式如下:
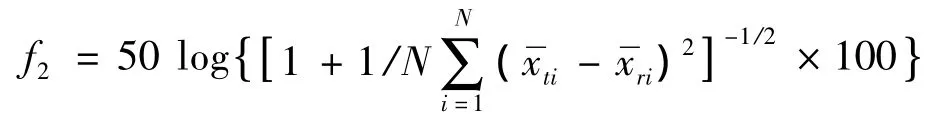
2.4.2 释药时滞的计算 对于择时释药系统,通常用药物累积释放达10%的时间代表药物开始释放时间,即释药时滞Tlag[5]。体外释放度测定发现,各制剂的药物释放曲线均呈S型,因此,采用统计软件SPSS16.0对释药曲线进行拟合,并根据拟合公式计算得出释药时滞(Tlag),并对各因素水平的Tlag进行t检验,评价各因素水平对Tlag的影响。
3 延迟缓释片体外释药的影响因素研究
3.1 片芯骨架材料的影响 固定衣膜处方和片芯中其它辅料不变,分别采用黄原胶、卡拉胶、HPMC K15M和HPMC K4M作为片芯骨架材料(用量均为片芯重量的20%),制备缓释片,测定体外释放度,结果见图1。

图1 片芯骨架材料种类对药物释放的影响
由图1可知,不同片芯骨架材料(分别为黄原胶、卡拉胶、HPMC K15M和HPMC K4M)缓释片的释药时滞分别为(4.4882 ±0.0648)h、(4.2663 ±0.0388)h、(4.1595 ± 0.0357)h 和(4.0308 ±0.1163)h,以HPMC K15M为对照,进行统计分析。结果发现,HPMC K4M和HPMC K15M的释药时滞无差异(P>0.05),但时滞后的药物释放有差异(f2值为47.4),HPMC K4M作为骨架材料的缓释片释放较快,15h时药物已基本释放完全,这与HPMC K4M黏度较低,溶蚀快有关,而HPMC K15M为骨架材料的缓释片可在24 h内缓慢释放,达到每天服药一次的设计要求;骨架材料为卡拉胶和黄原胶时,药物的释药时滞有显著性差异(P<0.05),对时滞后的药物释放无差异(f2值分别为69.7和64.0),但释药24 h后药物仍未完全释放,这与盐酸青藤碱本身带正电荷,黄原胶和卡拉胶两种材料均带负电荷,骨架材料可能通过静电吸附而影响药物完全释放有关[6,7]。
3.2 片芯中骨架材料用量的影响 固定包衣层,改变片芯中HPMC K15M的用量(分别为片芯重量的10%、15%、20%),制备缓释片,测定体外释放度,结果见图2。

图2 片芯中HPMC K15M用量对药物释放的影响
由图2可知,不同片芯HPMC K15M用量(分别为10%、15%、20%)的缓释片的释药时滞分别为(3.6795 ± 0.0703)h、(3.7950 ± 0.1963)h 和(4.1595 ±0.0358)h,以 20%用量为对照,进行统计分析。结果发现,片芯骨架材料的用量对释药时滞有显著性影响(P<0.05),并且时滞后的药物释放有影响,随其用量增加,时滞延长。缓释片释药过程中,随着外层衣膜的溶蚀,释放介质渗入片芯,片芯药物溶解后,扩散通过凝胶层释放,当片芯骨架材料用量增加时,骨架材料遇水形成凝胶层强度增加,药物扩散释放受阻,释药时滞延长,同时药物释放速度减慢。
3.3 衣膜中骨架材料种类的影响 固定片芯和衣膜中其他辅料不变,分别用黄原胶、卡拉胶、HPMC K15M、HPMC K4M作为衣膜的骨架材料(用量均为衣膜重量40%)制备缓释片,测定体外释放度,结果见图3。
由图3可知,不同衣膜骨架材料(分别为卡拉胶、HPMC K4M、黄原胶和HPMC K15M)的缓释片释药时滞分别为(1.4394 ±0.0071)h、(3.0437 ±0.4597)h、(3.8278 ± 0.1910)h 和(4.1595 ±0.0358)h,以HPMC K15M为对照,进行统计分析。结果发现,骨架材料种类对时滞有显著性差异(P<0.05),并且对时滞后药物释放也有影响(f2值分别为26.6、36.5 和49.4)。其中卡拉胶形成的凝胶强度弱,外层衣膜很快溶蚀,时滞短,并且卡拉胶与药物可发生电荷静电相吸作用,影响其完全释放;HPMC K4M、黄原胶和HPMC K15M则存在明显的释药时滞,其中黄原胶与卡拉胶一样,会影响药物的完全释放,而HPMC不影响药物的完全释放,但不同规格HPMC的释药情况有所不同,HPMC K15的黏度高于HPMC K4M,释药时滞延长,这与衣膜凝胶强度增加,其溶蚀减慢,影响介质渗入片芯溶解药物有关,并且衣膜凝胶层的强度增加,药物释放有所减慢。

图3 衣膜中骨架材料种类对药物释放的影响
3.4 衣膜中骨架材料用量的影响 固定片芯,改变衣膜中HPMC K15M的用量(分别为衣膜重量的20%、30%、40%)制备缓释片,测定体外释放度,结果见图4。
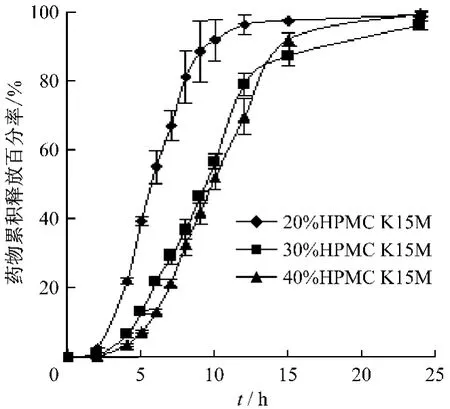
图4 衣膜中HPMC K15M用量对药物释放的影响
由图4可知,衣膜中不同HPMC K15M用量(分别为衣膜重量的20%、30%和40%)缓释片释药时滞分别为(2.8788 ± 0.0224)h、(4.1595 ± 0.0358)h和(4.7997 ±0.0903)h,以 30%用量为对照,进行统计分析。结果发现,HPMC K15M的用量对时滞有显著差异(P<0.05),随着HPMC K15M用量的增加,释药时滞延长,这与衣膜中骨架材料用量增加,形成的凝胶层强度增加,不易溶蚀,释放介质不易渗入片芯,药物开始释放时间延长有关[8,9],同时释药速率随HPMC K15M用量增加而降低趋势减缓,释放曲线相似程度增加(表现为HPMC K15M用量20%与30%比较,f2值为28.2,30%与40%比较,f2值为64.3)。提示,通过调整衣膜中骨架材料用量,可实现不同释药时滞,并影响时滞后的药物释放。
3.5 衣膜材料制备工艺的影响 固定处方组成,分别采用不同衣膜材料制备工艺制备缓释片,测定体外释放度,结果见图5。

图5 衣膜材料制备工艺对药物释放的影响
由图5可知,湿法制粒压片和粉末直接压片的释药时滞分别为(4.2910 ±0.1025)h 和(4.1595±0.0358)h,进行统计分析,结果发现,衣膜材料制备工艺对释药时滞无显著性影响(P>0.05),并且不影响释药速度(f2值为67.4)。提示,可根据辅料的性质和生产条件选择相应的制备工艺进行生产操作。
3.6 压力的影响 固定处方组成,制备不同硬度分别为(4±1)、(7±1)、(10±1)kg的缓释片,测定体外释放度,结果见图6。
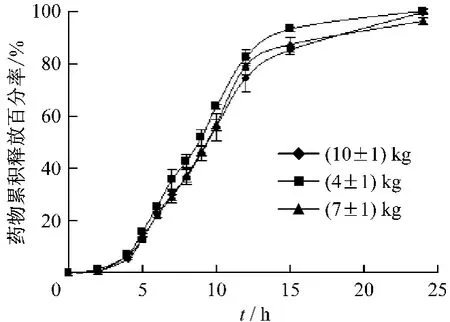
图6 压力对药物释放的影响
由图6可知,压力由小到大缓释片的释药时滞分别为(3.7693 ±0.0357)h、(4.1595 ±0.0358)h和(4.1996±0.0984)h,其中(4±1)kg与(7±1)kg的缓释片释药时滞有显著性差异(P<0.05),(7±1)kg与(10±1)kg的缓释片释药时滞无显著性差异(P>0.05),这与压力增大,造成衣膜材料的凝胶强度增加,溶蚀速率减慢有关,尤其当压力较小时更为明显,当压力增大到一定范围(7±1)kg时,释药时滞变化不明显;压力对释药时滞后的药物释放无影响(f2值分别为66.6和81.0)。
4 讨论
盐酸青藤碱延迟起释型缓释片的体外释药过程为:外层衣膜表面的骨架材料遇水形成凝胶层,介质渗入较慢,衣膜内侧和片芯仍保持干燥,片芯药物没有释放,存在释药时滞;随着释药过程进行,衣膜中骨架材料逐渐水化溶蚀并不断剥落,凝胶层溶蚀变薄,介质渗透进入片芯,药物溶解后,扩散通过外层凝胶衣膜释放,同时随着介质不断渗入片芯,片芯骨架材料遇水凝胶化,与外层未完全溶蚀的衣膜凝胶层混为一体,有效控制片芯药物的缓慢释放;释药后期,整个制剂的骨架材料完全水化,并且溶蚀加剧,药物几乎完全释放出来。在处方工艺设计时,应考虑各因素对制剂的释药延迟情况和时滞后药物的缓慢释放两方面的影响,其中外衣层膜的溶蚀速率是决定制剂释药时滞的关键,而衣膜溶蚀速度与衣膜中骨架材料种类和用量有关,衣膜和片芯中骨架材料种类和用量对时滞后药物的释放影响较大,提示可通过上述因素调节制剂的择时释药时间和释药速度,以满足制剂时辰治疗的设计要求。
[1]张立超,胡晋红,朱全刚,等.疾病的昼夜节律及脉冲给药系统[J].中国医院药学杂志,2000,20(12):738-739.
[2]何绍雄.时间药理学与时间治疗学[M].天津:天津科学技术出版社,1994:259-268.
[3]刘 强,周莉玲,李 锐.青藤碱的研究概况[J].中草药,1997,28(4):247-249.
[4]Moore J W,Flanner H H.Mathematical comparison of dissolution profiles[J].Pharm Technol,1996,20(1):64-73.
[5]范田园,魏树礼,严文伟,等.盐酸地尔硫卓爆破型脉冲控释片研究[J].药学学报,2002,37(3):221-225.
[6]刘 凌,薛 毅,王亚南,等.κ-卡拉胶胶凝特性研究[J].郑州轻工业学院学报,1999,14(1):65-68.
[7]王学艳,赵振宇,寇 欣,等.黄原胶的性质及其在制剂中的应用[J].中国药学杂志,1996,31(10):581-583.
[8]王宝庆,陆新汉,唐 星,等.乌拉地尔HPMC骨架片的研制及释放度的考察[J].沈阳药科大学学报,2001,18(1):5-8.
[9]董志超,蒋雪涛.羟丙基甲基纤维素的性质对药物亲水性骨架片溶出度的影响[J].药学学报,1994,29(12):920-924.