从一道习题解答谈水的Λm和Λ
2010-07-02王树国袁誉洪李金林
王树国 袁誉洪 李金林
(中南民族大学化学与材料科学学院 湖北武汉430074)
从一道习题解答谈水的Λm和Λ
王树国 袁誉洪 李金林
(中南民族大学化学与材料科学学院 湖北武汉430074)
电解质的摩尔电导率Λm是指把含有1mol电解质的溶液置于相距单位距离的电导池的两个平行电极之间时具有的电导。摩尔电导率受溶液的浓度影响,不管是强电解质还是弱电解质,随着溶液浓度的减小,摩尔电导率增大。就是指溶液无限稀释时的摩尔电导率。这里的溶液是用水作溶剂,那对于纯水的Λm和又作何理解呢?下面以一道常见的习题的解答来谈谈笔者的看法,权作引玉之砖。该习题出自南京大学傅献彩等编的《物理化学》(下册)第5版第57页(习题18)[1]。
“根据如下数据,求H2O(l)在298K时解离成H+和OH-并达到平衡时的解离度和离子积常数。已知298K时,纯水的电导率κ(H2O)=5.5×10-6S·m-1,(H+)=3.498×10-2S·m2·mol-1(OH-)=1.98×10-2S·m2·mol-1,水的密度为997.09kg·m-3。”
不少物理化学教材或参考书上有与此相似的例题或习题,一般的解答为[2]:
解:
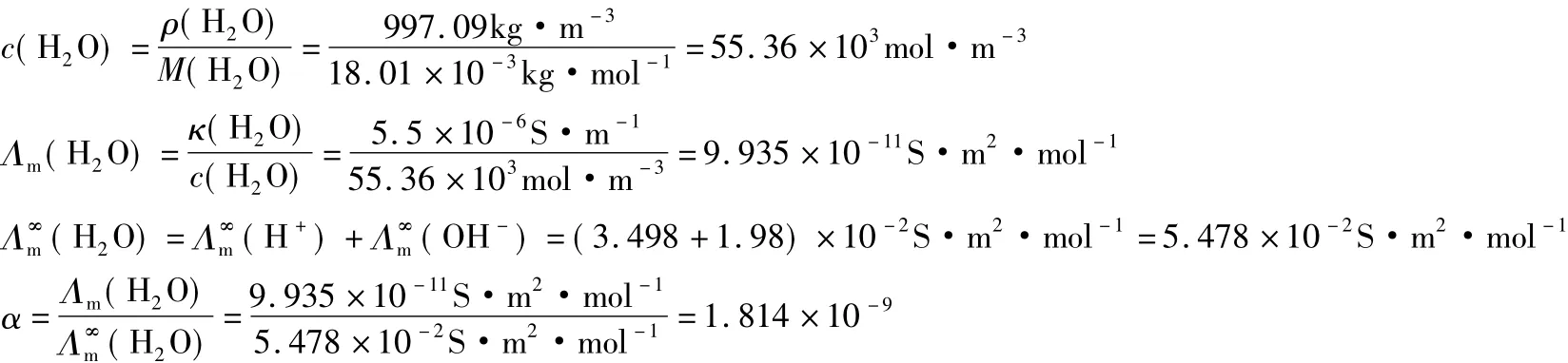
水的离解度极小,其平均活度因子近似等于1。

以上解答中,Λm(H2O)和(H2O)针对的对象都是纯水,为什么对同一个溶液(水又充当溶剂的角色),Λm(H2O)和(H2O)有如此大的悬殊呢?其实二者的“H2O”含意是不一样的,前者是指总的水,而后者是指电离了的那部分水。水的电离度很小,未电离的水是大量的,满足的“无限稀释”的要求,因此可认为:Λm(H2O(电离))=(H2O),上述习题可解答如下:
解:水的电离度很小,把电离的部分水看作溶质,满足“无限稀释”的要求,即:
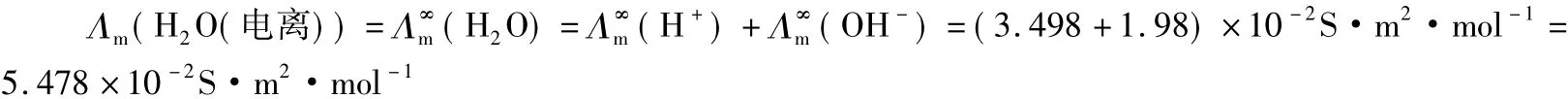
则有

从上述解答可进一步理解Λm(H2O)和(H2O)中的“H2O”含意的差别。
[1] 傅献彩,沈文霞,姚天扬,等.物理化学.第5版.北京:高等教育出版社,2006
[2] 孙德坤,沈文霞,姚天扬,等.物理化学学习指导.北京:高等教育出版社,2007
