左室功能不全所致的慢性心力衰竭患者心肺运动试验声明实施和解释建议(1)
2010-06-15刘杰李寿霖编译胡大一审校
刘杰,李寿霖编译,胡大一审校
心肺运动试验(CPET)是能向医生提供重要信息、评估包括肺、心血管、造血、神经心理和骨骼肌系统在内的运动整合反应的无创性试验方法。测定运动中的呼出气体可以最好地估计功能容量,对受损的严重程度分级,客观评估干预效果,客观追踪疾病进展,以及鉴别运动容量减低的心、肺原因。为了在日常临床实践中更好地使用这一方法,阐明概念、对CPET标准化是必要的。由欧洲心脏病学会心脏康复和运动生理工作组发起、意大利心脏康复预防特别工作组起草的左室功能不全所致的慢性心力衰竭(CHF)患者心肺运动试验总结声明于2007年公布。
近年来,下列因素促进了CPET的应用:①运动生理学的发展以及认识到了运动整合反应在临床评估中的重要性;②已经证明CPET数据是评估和处理CHF患者的重要而可靠的测量指标,而静息的肺功能和心功能检查不能可靠地预测运动能力和功能容量;③运动耐量指标比静息的测量指标能更好地预测总的健康状态和预后;④CPET对运动受限和心肺功能提供了可重复性的指标,是危险分层和选择恰当治疗方法的有用试验方法;⑤具有强大数据采集、处理和个体监测能力的自动运动系统的技术发展。
委员会通力合作,基于当前的科学知识和技术进步,制定了关于CPET在左室功能不全的CHF患者中应用的综合、实用、及时、概念统一性的文件,包括了对CPET的解释、实施标准化和临床应用等推荐建议。建议以现有的最好证据、当前流行的科学知识和专家意见为基础,以发现那些有争议的、不能达成共识的领域,并提出可能的解决途径。
面向的读者包括CPET操作者、根据CPET结果进行临床决策制定者和开具运动处方者,而对致力于CPET领域信息扩充并用于临床评估的临床读者将特别有用。
文件分三部分:①适宜CHF的CPET参数解释;②在CHF中如何实施CPET;③CPET在CHF中的解释和未来应用。
第一部分 适宜CHF的心肺运动试验参数定义
CPET能为机体对运动的反应提供全面的评估,包括了肺、心血管、造血、神经心理和骨骼肌系统。这些信息是通过研究个别器官系统所不能获得的。无创、动态的生理学观察对极量和次极量运动反应进行评估,能向医生提供临床决策的相关信息。由于静息心肺功能检查不能可靠预测运动能力和功能容量,并且,运动耐量指标比静息参数能更好的预测总的健康状态和预后,CPET在处理CHF中的应用逐渐增加。本声明基于当代科学知识和技术进步,就CPET在心力衰竭中的临床应用和解释提供建议:重点强调CPET的临床适应证、标准化问题和解释策略。
本声明由欧洲心脏病学会心脏康复和运动生理工作组发起,目的是针对左室功能不全所致的CHF患者应用CPET的话题,产生综合性的、概念统一性文件。
CPET是充分确立的适用于多个临床情况的诊断试验方法。不同心肺疾病患者的运动反应存在显著的重叠。对于CHF患者来说,其适应证、实施和解释均具有特殊性。
该文件共有8个部分:①CPET的定义;②CPET在CHF中的适应证;③安全性;④仪器设备;⑤运动方案;⑥实施方式;⑦数据报告和⑧解释。
CPET的定义
CPET为机体对运动的整合反应提供全面的评估,可以对肺、心血管、造血、神经心理和骨骼肌系统进行综合评价。这种无创、动态的生理评估允许对极量和次极量运动反应进行评价。一般在症状限制性的最大运动耐量试验中,除了监测心电信号、血压和血氧饱和度之外,还包括呼吸气体交换、摄氧量(VO2)、二氧化碳排出量(VCO2)和分钟通气量(VE)的测定。稳态条件下经口测定的VO2和VCO2相当于机体总的O2消耗量和CO2生成量。
下面讨论呼吸气体交换参数的临床意义和重要性。
氧摄取量(VO2)
运动期间工作输出、VO2、心率(HR)和心输出量(CO)之间近似线性关系。VO2取决于细胞O2消耗和O2的运输速率。可通过血流量和组织对O2的利用计算VO2。

SV表示心搏量,C(A-V)O2diff为动静脉O2差。
一些因素可影响VO2:①血液的携氧能力(取决于可用的血红蛋白(Hb),Hb-O2饱和/分离曲线随温度、CO2和pH移动);②心功能(HR、SV);③外周血流的区域分布和局部分配;④组织对O2的利用(毛细血管密度、线粒体密度和功能、充分的灌注和组织弥散)。在正常人中这些影响VO2的因素也同样影响CHF患者的运动反应。
VO2-功率(WR)关系(VO2/WR)
正常情况下,VO2随外部做功(功率输出)的增加而呈线性增加。外部功率以瓦(W)为单位的精确测定可以测定这一关系。自行车测力计可以测定外部做功。VO2对外部功率的斜率反映了化学能向机械做功的代谢转化以及肌肉骨骼系统的机械能力。VO2相对于外部功率的变化率决定斜率,正常人在自行车测力计上进行递增运动试验的斜率大约为10~11 ml/min/W,不受性别、年龄和身高的影响。
有氧代谢能力应该直接测定,因为从静息指标、功率或次极量运动方案中得来的估计值受生理机制和方法学不精确性的限制而不可靠。反过来,在正常个体和CHF患者中直接测定是可靠和可重复性的。正常或的主要决定因素是遗传因素和运动肌群的量。和也依赖性别、年龄和体重,并受训练的影响。或的下降是运动能力下降的总体“指示剂”。运动受限的潜在具体原因可通过观察其他变量的反应形式加以确定。
CO2生成量()
在短时运动期间,糖原主要为肌肉利用以提供能量,O2耗量与CO2生成之间的关系几乎是等分子的。因此,进行性运动期间,在较低的功率范围内,的增加几乎与的增加一样多,平均与的关系略微小于1.0。
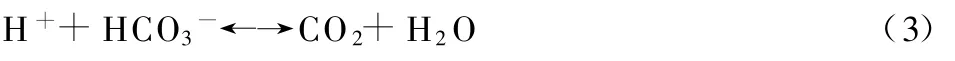
当组织中乳酸(H+)增加时,反应向右侧驱动,产生多于有氧代谢时生成的CO2。过多的CO2也可来自因过度通气(表现为动脉低碳酸血症)造成的机体CO2的储存减少。由于运动期间VE与成比例密切耦联,分析 VE与的关系是有用的。精确测定CO2的生成也很重要,因为它是计算一些衍生变量的基础,包括(1)呼吸交换比率,(2)生理死腔与潮气量的比值和(3)肺泡通气量。
稳态条件下RQ=1.0表示为碳水化合物代谢,RQ<1.0表示为碳水化合物与脂肪(RQ≈0.7)或与蛋白质(RQ≈0.8)的混合代谢。在真正的稳态下,血液和气体运输系统与组织代谢保持同步,因此RER可用作代谢事件(RQ)的粗略指标。但在无氧阈值以上,RER>1.0也可由乳酸来源的CO2或过度通气所造成,因为CO2的组织溶解度是 O2的20倍以上,并且HCO3-和蛋白质是组织运输CO2的显著形式,而O2运输的惟一显著形式是与血红蛋白结合。
这一指标为CPET期间所实施的运动水平提供了指示:在RER未达到1.1以上时,通常认为试验是次极量的。若患者在达到此值前停止运动,应该考虑心脏以外的其他限制因素。这一信息可对CHF提供重要的预后价值:在极量CPET试验(峰值运动时RQ>1.1)期间发生运动耐量受损(反映于<10 ml/min/kg与高死亡率相关。
无氧阈值(AT)
AT也称作乳酸阈值、气体交换阈值或通气阈值,是VE的增加与VO2和做功的增加不成比例的点。它表示递增运动期间肌肉组织转向无氧代谢作为额外能量来源的理论点:乳酸开始堆积,由血清中碳酸氢盐系统缓冲,导致CO2的生成增加,产生反射性过度通气。根据方程(3),它被认为是运动期间动脉乳酸升高速率增加所致代谢性酸中毒发生的估计指标。
在AT以下水平做功满足了大部分的日常活动。大多数的重大心血管疾病患者AT下降。训练提高AT,可显著增加个体进行持续次极量活动的能力,提高生活质量。
描述这一转变点的命名学差异反映了关于在AT点肌肉和血液乳酸增加的潜在生理机制存在争议。尽管有关AT的传统观点受到支持,但其他学者对这一观点持有质疑。如果不同的肌群在不同的时间达到无氧代谢,转变点将是平滑的,可能很难精确确定一个截然分界的点,即AT。
机制
人们对AT的起因存在争议:当运动强度增加时,氧运输与氧化能力之间的失衡以及所调动的肌纤维类型可能均促成乳酸的增加。对于后一种机制,在氧化酶与糖酵解酶的平衡中,即“有氧”与“无氧”代谢的平衡中,肌纤维的类型有所不同。在低强度运动中,所调动的是以氧化代谢为主的纤维,但随运动强度的增加,主要依赖糖酵解途径的纤维被激活,从而增加乳酸的生成。
因此,AT这一术语应该在描述的意义上使用。不同乳酸来源的相对贡献也可随疾病的不同而不同。例如在心力衰竭中,不仅有氧运输能力的降低,也存在肌纤维组成和代谢的变化,以至于随运动强度的增加,的上升速率开始下降而乳酸的上升速率过早增加。
不管机制如何,随运动强度增加而血中乳酸的增加具有重要的生理后果。首先,乳酸的堆积降低血液和间质液的pH值,最终将会损害细胞的功能。第二,pH的降低以及与之相关的其他事件使机体试图通过降低动脉CO2分压()来缓冲酸增加,从而可能刺激通气。第三,pH的降低使氧离曲线右移,增加O2向肌肉的运输(即所谓的波尔效应(Bohr effect))。当O2饱和度下降时,工作肌毛细血管床末端的PO2的确保持不变。因乳酸堆积影响细胞功能,运动期间乳酸升高的幅度及其相对于变化而升高的形式,在运动试验中可能是有用的指标。再者,乳酸堆积发生越早,长期持久的越低。
临床应用
AT界定了几乎完全由有氧代谢完成的运动强度的上限。AT以下的做功功率可基本上无限的持续,而在AT以上功率的进行性增加将导致运动耐量的进行性降低。不爱活动的正常个体,其A T出现于预计值的50%~60%。正常值范围可延伸至35%~80%。AT的测定具有年龄、运动方式和方案特异性。
AT测定作为心肺适能的指标,有助于制订运动处方、监测训练效果。当未达到AT时(如在一些严重慢阻肺患者),或AT不能经通气反应测定时(如存在振荡形式),使用峰功率、和心率的百分比作为参照,仍可制订运动处方。
测定
现有几种方法测定AT,包括有创(乳酸和标准碳酸氢盐)和无创法(通气当量法[、潮气末呼出氧压(PE)、潮气末呼出CO2压(PE)]、V-斜率法和改良 V-斜率法)。
有创方法尽管具有科学和生理学的重要性,但很少用于临床实践。在临床上,随着运动强度的增大,通过观察和VE相对于的变化形式,可以无创性地测定乳酸酸中毒。
改良 V-斜率法:由于评估的复杂性,开始的V-斜率法已被简化的方法所取代。改良V-斜率法则是确定斜率的变化点,在无过度通气的情况下测定的增加快于的增加时的。
当使用这些方法检测AT时,应该注意有创和无创方法测定的AT具有很好的相关性,但不一定是肯定的生理性联系,运动时不寻常的呼吸形式(如振荡呼吸)可对AT的测定产生不利影响。
CHF患者典型的AT下降与运动耐量的下降有关。由于AT测定了可持续的O2摄取,是心肺运动能力的客观参数,可从次极量运动试验中得出,因此对它的计算不仅可提供辅助信息,而且是对的补充。因此它不受患者努力不足或检查者过早终止试验等因素的影响。作为常规,低于预计值40%的A T值视为异常。最近的资料建议阈值<11 ml/min/kg作为预后不良的指标。
然而,在综合征晚期的大多数患者,如NYHA心功能Ⅲ、Ⅳ级,常常不能发现明确的A T值,这主要发生于振荡呼吸时。AT不受患者主观努力的影响。低时检测到正常的AT值提示为次极量运动。因测定问题,AT从来不能取代作为CHF患者的功能容量或预后指标。在大多数日常活动甚至静息时,患者的代谢接近甚至超过AT。
通气
运动期间通气(VE)增加是运动肌代谢需求增加时稳态控制动脉血气和酸碱平衡状态的主要途径之一。尽管VE与气体交换(代谢需要)耦联的机制尚不完全清楚,但运动中通气反应的一些指标可评估通气反应的正常或不足。
运动期间最常评估的通气指标包括总的分钟通气量(VE)的变化和呼吸形式(潮气量VT和呼吸频率 f),同时也评估通气储备。不经常评价的指标是通气时间(吸气时间TI和总时间)和潮气量相对于特定肺容量(如VT/VC)的变化。
最近,吸气容量(IC)的变化和运动中通气受限的更全面评估指标也得以应用。因为通气是呼吸力学最优化与气体交换的维持之间的平衡,许多通气指标均表示这些联合的要素,如通气效率(VE/或 VE/)。
运动中VE的增加与潮气量(VT)和频率(f)的增加均有关。健康个体低水平运动时通气的增加主要来自VT的增加。随着运动的进行,直到峰值运动的70%~80%,VT和 f均增加,之后 f占主导。VT通常在肺活量(VC)的50%~60%保持平台,但有相当大的变异。
在CHF患者,即便在静息状态下也观察到通气形式的变化。呼吸计量研究显示用力VC和总肺容量的减小,而用力呼气肺活量相对保持正常。这种总的呼吸限制形式归因于间质水肿造成的肺实质僵硬度增加和随后的纤维化,可能也源于心脏增大的压迫作用。值得注意的是,总肺容量的减小与肺毛细血管楔压有关,这种异常在药物治疗或心脏移植后具有部分的可逆性,表明这种异常可能归因于液体的失衡,而不是永久性的变化如纤维化。
在充血状态下,CHF导致肺毛细血管楔压异常增加,促成间质水肿提前形成或加重,从而导致运动期间肺顺应性异常、动态地减低。这些异常导致运动期间的呼吸形式以低潮气量和高呼吸频率为特征。
再者,不要忘记心脏增大对肺的直接压迫作用,因为已经观察到心脏移植后2/3以上的肺活量改善可归因于心脏的减小。尽管存在限制性的呼吸改变,通气能力似乎并未限制CHF患者的运动能力,因为运动期间通气的增加大约是正常对照个体的2倍。
通气能力可通过第一秒用力呼气量(FEV1)乘以假定的最高呼吸频率(通常为35%~40)来估算,给出了理论上可以获得的分钟通气量,称为最大自愿通气(MVV)。为了评估通气能力是否限制运动时的气体交换,将MVV与峰值运动时测定的实际最大分钟通气量相关联(peakVE/MVV)。对于正常个体,此比值约为0.6~0.8,但对于阻塞性或限制性肺病患者或训练有素的运动员,当肺容量减小或循环和肌肉气体交换能力增加时,此值可增大。但在主观努力不足的患者中评价VE/M VV关系时应该小心。CHF患者的VE/M VV低于正常人;这可能源于肌肉和循环气体交换能力的降低。
肺弥散能力
气体弥散遵循Fick定律:
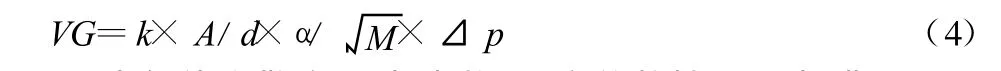
VG为气体弥散率,k为常数(温度依赖性),A为膜面积,d为膜厚度,α为气体溶解度,M为气体分子量,⊿p为气体跨膜压差。因此,肺泡弥散率与肺泡面积、O2和CO2的溶解度以及O2和CO2的平均肺泡-毛细血管压力差成正比,与肺泡-毛细血管膜厚度成反比。因CO2的溶解度高,其穿过肺泡-毛细血管膜的速度比O2快约23倍。因此,肺的任何弥散受限都将主要影响O2而非CO2的弥散。可以预计,在理论上影响CO2弥散的任何肺弥散受限都必然已经导致危及生命的O2弥散障碍。除了肺泡-毛细血管膜的大小和特征外,O2的弥散还依赖毛细血管的O2含量(即O2摄取对O2分压变化的比率)。这取决于毛细血管血容量、血红蛋白浓度和O2与血红蛋白反应的速率。因此,在血红蛋白浓度正常的前提下,肺的弥散能力(DL)有两个决定因子:肺泡-毛细血管膜阻力的通透性(DM)和毛细血管血容量(Qc)。因此,肺弥散的总阻力可以描述为:

CHF患者的肺弥散能力(DL)下降,并与心力衰竭的严重程度相关。主要的促成因素是DM的降低,而毛细血管血容量是可变的。DM的降低源于间质水肿和纤维化,这两者均是可逆的。使用血管紧张素转换酶抑制剂(ACEI)和抗醛固酮药物可改善弥散能力,与VE/和VD/VT的改善相平行。
然而有证据表明即便在心脏移植的数年后DM仍保持低下。CHF患者的这种弥散能力降低是否真正导致运动受限和运动中的通气反应增强,这一问题一直未得到解决。DM与密切相关,但一方面已经显示由于间质水肿的形成,DM在运动期间可能降低,另一方面DM可能增加,但增加的程度很有限并伴随着VC的增加,致使DL保持不变。
然而,弥散能力似乎并未限制肺泡氧耗量,即动脉低氧血症并非CHF的典型发现。因此,弥散能力(或DM)和运动容量指标之间的相关性可能未揭示一种因果关系,而是反映了一种常见的决定因子,即运动时的血流动力学反应不良,伴有左室充盈压的升高和肺毛细血管楔压的持续增加。
肺灌注
肺循环以低血管张力为特征,并且在血流增加时肺血管阻力进一步降低。因而肺动脉压力较低,当心输出量增加时仅轻度增高。除了这种整体的血流动力学特征外,肺内局部的血流分布受毛细血管前阻力小血管的紧密调节。局部血流分布的主要调节因子是低氧性血管收缩(Euler-Liljestrand机制);肺泡氧分压的降低导致血管张力增高和相关肺腔的血流减少。这样就形成了肺通气与灌注的匹配,减少肺内分流和死腔通气。许多血管扩张剂(一氧化氮、前列环素)和血管收缩剂(血栓素、内皮素-1)参与调节过程。
CHF左室充盈压的升高导致肺静脉高压。肺动脉压因肺血管阻力的增加而进一步升高。对瓣膜置换术前后二尖瓣狭窄患者的血流动力学研究显示肺静脉压正常后肺血管阻力迅速下降,这表明肺血管张力的增加是对肺静脉压升高的直接反应。血管张力的增加来自基础的血管舒张活动的受损和血管收缩刺激的增高。已经显示心力衰竭患者肺血管内皮细胞NO的释放减少和继发性肺动脉高压,但可被乙酰胆碱所刺激。前列环素的合成减少而血栓素的合成增加。心力衰竭中内皮素-1的水平升高,伴有肺ET-B受体的下调,产生肺血管收缩。
这些机制不仅导致总的肺血管阻力增加,而且导致肺局部血流分布受损(来自荧光显像研究证据)。这导致尽管通气分布正常但灌注不规则。CHF患者运动期间不能充分减少这种匹配不良,可导致运动容量减低。
(未完,待续)
