草莓内生细菌的分离及草莓灰霉病菌拮抗菌的筛选鉴定
2010-06-12戴美学
李 娜, 戴美学
(山东师范大学生命科学学院,济南 250014)
植物内生细菌在植物体内有稳定的生存空间,一旦进入植物体内,即可独立繁殖和传递,并占据有利的生态位点来防止病原菌的入侵[1]。因此有益的内生细菌有可能成为生物防治中很有发展潜力的生防因子。
草莓灰霉病是导致草莓产量和质量降低的主要限制因素之一[2]。目前,对草莓灰霉病的防治以化学手段为主,但研究表明随着灰霉抗性菌株的增加,化学防治的优势正在下降[3-4],且存在农药残留问题[5]。因此安全、低毒的生物防治已成为研究的热点,作为生物制剂的木霉和酵母菌已在灰霉病的防治中发挥重大作用[6-7]。研究证明生物制剂如能阻止或减少灰霉菌对于草莓花朵的侵染,就能有效地控制灰霉病害[8],而内生细菌能发挥该项作用。
草莓内生细菌具有通过产生吲哚乙酸和溶解有机磷来促进植株生长的作用[9],但对其生防作用的研究国内外尚未有报道。本文对防治草莓灰霉病菌的内生细菌进行筛选,并对一株高效菌株SL6进行了鉴定。
1 材料与方法
1.1 材料
1.1.1 样品
董家草莓基地3个大棚中生长旺盛的草莓,在不同层次,不同区域以五点取样法取草莓根、茎、叶。
1.1.2 培养基
PDA:马铃薯200g,葡萄糖20g,琼脂20g,水1 000mL,pH 自然;NA:牛肉膏3.5g,蛋白胨10g,NaCl 5g,琼脂20g、水1 000mL,pH7.0~7.2。
1.1.3 靶标病原菌
草莓灰霉病菌(BotrytiscinereaPers.ex Fr.),本试验室保存菌种。
1.1.4 引物
16SR1(AGAAAGGAGGTGATCCAGCC);16SF1(AGAGTTTGATCC TGGCTCAG)由上海生工生物技术有限公司合成。
1.2 方法
1.2.1 草莓内生菌的分离
1.2.1.1 表面消毒时间的选择
为了既能保证植物组织的青翠,以获得较多的内生菌,又能保证表面消毒彻底,需要通过一系列试验寻找恰当的HgCl2消毒时间。将草莓根、茎、叶用0.1%HgCl2处 理1、1.5、2、2.5、3、3.5、4min。然后将处理后的根、茎、叶在NA培养基,28℃培养箱中培养3~5d,观察是否有菌的生长。
1.2.1.2 表面消毒
将植物组织用清水冲洗干净,无菌水冲洗10次,在75%乙醇中消毒5min,无菌水冲洗3次,最佳0.1%HgCl2时间消毒后,无菌水冲洗3次。
1.2.1.3 内生细菌的分离
将检出的消毒彻底的组织采用五点取样法剪成0.5cm×0.5cm左右的小块,组织匀浆器研磨充分,依次稀释,取原液、10-1、10-2、10-3稀释度的组织液0.1mL涂布于NA平板,每种样品3个重复,37℃培养箱中倒置培养2~5d。
1.2.1.4 内生细菌的纯化
培养3~5d后,挑取不同形态的菌落于NA平板上画线纯化。
1.2.2 拮抗细菌的筛选与拮抗性能测定
1.2.2.1 草莓灰霉菌拮抗菌的筛选
采用对峙培养法,取直径8mm的靶标菌菌饼置于PDA平板(d=90mm)中央,用接种环挑取纯化好的菌种点接在距平板中央3cm处的4个角点上,25℃培养7d后测量抑菌带宽。每处理设3个重复。选出对病原菌生长有抑制作用,且被抑病原菌丝边缘平齐、拮抗作用持久的菌株。
1.2.2.2 拮抗菌株的拮抗性能测定
进入复筛的菌株,按上述方法做对峙试验,以接种靶标菌饼的平板做对照,每处理设3个重复,25℃培养3~5d,直到对照平板布满灰霉菌,测量抑菌圈半径(细菌菌落中心至病原菌菌丝边缘)。
1.2.2.3 SL6发酵滤液的抑菌作用测定
抑菌效果最佳的SL6菌株在37℃振荡培养3d后,发酵液离心(12 000r/min,20min),取上清液用细菌过滤器(0.25μm)除菌,得无菌发酵液,取1mL发酵滤液加入到熔化的25mL PDA培养基中,混匀后制平板,以不加发酵滤液的PDA培养基为对照。同步接种草莓灰霉病菌菌丝块,每个处理重复3次,于25℃培养箱中培养,待对照板菌丝触及平板边缘开始测量,计算加入滤液的平板菌丝生长直径的平均值,利用公式可得出其抑菌率。对无菌发酵滤液进行梯度稀释后,同样方式,测其稀释后的抑菌率。挑取经过滤液处理及对照平板上的边缘菌丝,在扫描电镜下观察菌丝形态。
抑菌率=(对照板菌丝直径一处理板菌丝直径)/(对照板菌丝直径一霉菌菌块初始直径)×100%。
1.2.3 拮抗细菌的初步鉴定
根据拮抗细菌菌株的形态、培养性状和生理生化特性的测定结果,参考《伯杰细菌鉴定手册》和《常见细菌系统鉴定手册》对菌株进行鉴定[10-11]。
1.2.4 拮抗细菌的分子鉴定
抽提拮抗菌总DNA,利用16SrDNA细菌通用引物R1和F1进行PCR扩增。扩增产物回收,送至上海生工生物科技公司测序。测序结果用Blast软件在GenBank中进行同源性比较。
1.2.5 菌株系统发育分析和系统发育树构建
从GenBank中查找已经测序的同属菌的16S rDNA序列用ClustalX进行多序列比对分析,再用MEGA4软件中Neighbor-Joining法构建系统发育树,并进行1 000次Bootstraps检验。
2 结果
2.1 选择HgCl2消毒时间
由表1可以看出,草莓根、茎、叶所需的0.1%HgCl2最佳消毒时间不同,根部所需处理时间最长,需3.5min。叶所需时间为3min,茎部需要2.5min,这可能与植物各个器官的生理结构相关。
2.2 各组织中内生细菌的数量
由表2可知,草莓的各个组织结构中均有内生细菌定殖,但不同组织中内生细菌分布的密度不同,草莓茎部内生细菌的含量为2.29×104~3.95×104cfu/g鲜重,叶中为3.22×103~9.66×103cfu/g鲜重,草莓根部的内生细菌的含量最少,为2.8×101~5.3×101cfu/g。根据菌落形态、颜色及分离部位的不同,共纯化得内生细菌54株。且不同组织结构中内生菌的种类也不相同,茎中分得形态颜色不同的菌株27株,叶中15株,根中12株。可见,内生细菌的分布密度及种类均与所在植物的部位相关。
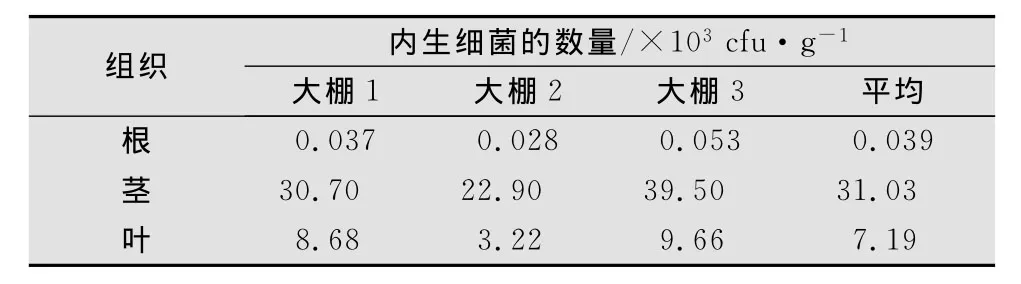
表2 草莓不同组织中内生细菌的含量
2.3 拮抗内生细菌的抑菌效果及形态学和生理生化特性的鉴定
2.3.1 拮抗内生细菌的拮抗能力测定
平板对峙试验测定结果表明,5株内生细菌具有较为明显的拮抗作用,抑菌半径最低为7mm,最高的SL6可达15mm(表3、图1)。

表3 5株内生拮抗菌株的抑菌能力1)
2.3.2 SL6发酵滤液的拮抗作用
通过对于生长直径的测量,运用公式得出,SL6的发酵滤液对草莓灰霉病菌菌丝的抑制率达97.6%(图2)。稀释100倍后,抑菌率为53.7%,有较好的抑菌效果(图3)。扫描电镜下对混有发酵液及空白对照平板上菌丝的形态观察显示,对照菌丝光滑、修长,滤液处理组菌丝部分膨大变形甚至断裂,原生质体溢出(图4)。与平板对峙试验中,对菌丝的作用一致。推测是活性物质的溶菌作用所致。具体的活性物质成分还有待于进一步的研究。

图1 SL6抑菌效果
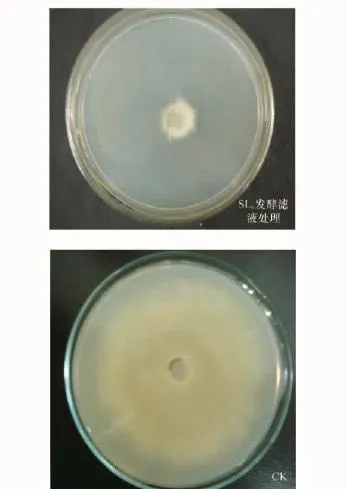
图2 SL6无菌发酵液的拮抗活性检测
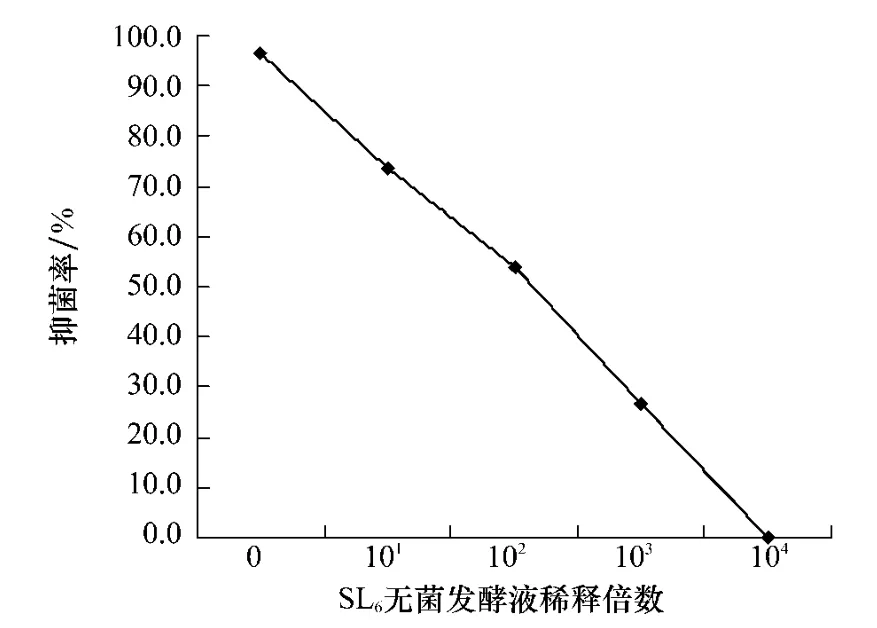
图3 SL6无菌发酵液稀释后的抑菌效果
2.3.2 拮抗内生菌的形态学和生理生化测定结果
通过形态学观察和生理生化特征的测定,对草莓灰霉病菌有抗菌作用的5株内生细菌进行了初步鉴定,结果见表4、5。
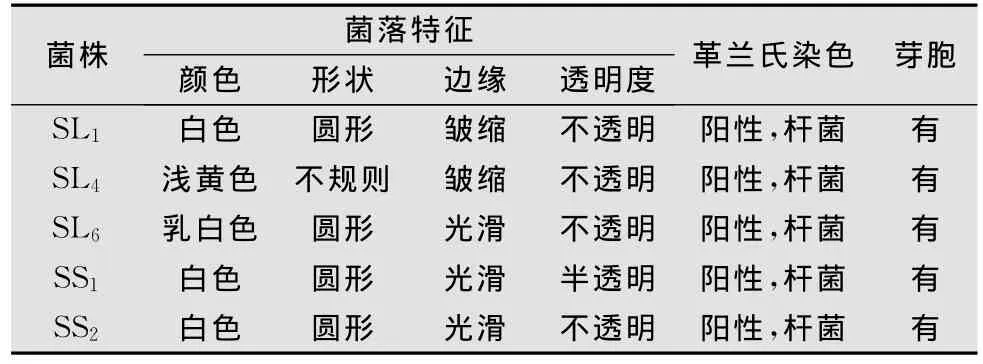
表4 5株内生拮抗菌形态及染色特征

表5 5株内生拮抗菌生理生化测定结果1)

图4 SL6无菌发酵液对菌丝的抑制作用
5株菌株幼龄培养物均成杆状,革兰氏阳性,芽胞为卵圆球形,以周生鞭毛运动,好氧或兼性厌氧,革兰氏阳性,接触酶反应呈阳性,不产生吲哚,确定其均归属于芽胞杆菌属(Bacillussp.)[10-11]。
2.3.3 菌株SL6系统发育分析
菌株SL6的16SrDNA PCR产物长度为1 487bp,此序列在GenBank数据库中的注册序列号为FJ948786.1。由构建出的系统发育树可知,SL6与芽胞杆菌属的菌株同源性高,与枯草芽胞杆菌(Bacillussubtilis)DCC1106(EU276080)在同一分支上,结合生理生化鉴定结果,可鉴定菌株SL6为枯草芽胞杆菌。系统发育树见图5。
3 讨论
内生细菌定殖在植物的内部[12],通常能够促进植物的生长,且不会对植物的组织器官造成伤害[13],是植物组织内的正常菌群,可以通过组织学方法或从表面严格消毒的植物组织和汁液中分离获得[14]。本研究表明,草莓根、茎、叶组织中均存在大量内生细菌,各组织内生细菌的密度不同,范围在2.8×101~3.95×104cfu/g鲜重之间。

图5 菌株SL6的系统发育树
本研究通过设计不同的梯度来确定升汞的最佳消毒时间,以达到使分离的内生细菌尽可能真实地反映植物内的微生物群落的效果。过长的消毒时间导致内生细菌种群密度减少;消毒时间较短,附生细菌会干扰内生细菌密度的计算;且不同组织器官,因其构造的不同,需要的消毒时间也会有差异。
内生菌种有很多抗性菌株,具有提取各种抗菌物质的潜力[15-16],是生物防治中起重要作用的生防因子。目前,从植物内部分离得到的生防细菌已有多种,如:王书同从番茄植株中分离得到一株内生枯草芽胞杆菌对番茄灰霉病菌的抑制率达71.1%[17],但对草莓内生细菌生防作用的研究,目前国内外尚未报道,本研究从草莓中筛选得到内生枯草芽胞杆菌SL6,其无菌发酵液对草莓灰霉病菌的抑制率可达97.6%,具有生防菌的潜能。对其发酵滤液进行分析可知是抗菌蛋白在起作用,但分离纯化的方法有待进一步研究,以期得到在病害生物防治中能起作用的抗菌蛋白。
[1]Hallmann J,Quadt-Hallmann W F,Mahaffee A,et al.Bacterial endophytes in the agricultural crops[J].Can J Microbiol,1997,43:895-914.
[2]Jarvis W R.The biology ofBotrytis[M].Academic Press,1980:1-17.
[3]Rosslenbroich H J,Stuebler D.Botrytiscinerea-history of chemical control and novel fungicides for its management[J].Crop Prot,2000,19:557-561.
[4]Yourman L F,Jeffers S N.Resistance to benzimidazole and dicarboximide fungicides in greenhouse isolates ofBotrytis cinerea[J].Plant Dis,1999,83:569-575.
[5]Washington W S,Shanmuganathan N.Fungicide control of strawberry fruit rots and the field occurrence of resistance ofBotrytiscinereato iprodione,benomyl and dichlofluanid[J].Crop Protection,1992,11(4):355-360.
[6]Sutton J C.Evaluation of micro-organisms for biocontrol:Botrytiscinereaand strawberry,a case study[M].Advances in Plant Pathology,1995:173-190.
[7]Lima G,Ippolito A.Effectiveness ofAureobasidiumpullulansandCandidaoleophilaagainst postharvest strawberry rots[J].Postharv Biol And Technol,1997,10:169-178.
[8]Pedro Boff,Jürgen Köhl,Matthijs Gerlagh,et al.Biocontrol of grey mould byUlocladiumatrumapplied at different flower and fruit stages of strawberry[J].BioControl,2002,47:193-206.
[9]Armando C F Dias,Francisco E C Costa,Fernando D Andreote,et al.Isolation of micropropagated strawberry endophytic bacteria and assessment of their potential for plant growth promotion[J].World J Microbiol Biotechnol,2009,25:189-195.
[10]Buchanan(布坎南)RE,Gibbons(吉本斯)NE.伯杰细菌鉴定手册[M].第八版.北京:科学出版社,1984.
[11]东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001.
[12]Kobayashi D Y,Palumbo J D.Bacterial endophytes and their effects on plants and uses in agriculture[J].Microbial Endophytes,2000:199-233.
[13]Ladha J K,Reddy P M.Steps towards nitrogen fixation in rice[J].International Rice Research Institute,2003:33-46.
[14]Stone J K,Bacon C W,White J F Jr.An overview of endophytic microbes:endophytisMdefined[M].New York:Marcel Dekker,2000:3-29.
[15]Strobel G A.Endophytes as sources of bioactive products[J].Microbes Infect,2003,5:535-544.
[16]Sun L J,Lu Z X.Advance on antibiotics produced by endophytes[J].Food Ferment Ind(China),2005,31:39-41.
[17]Wang Shutong,Hu Tongle,Jiao Yanling,et al.Isolation and characterization ofBacillussubtilisEB-28,an endophytic bacteriuMstrain displaying biocontrol activity againstBotrytiscinereaPers[J].Frontiers of Agriculture in China,2009,3(3):247-252.
