硫辛酸和弥可保治疗糖尿病周围神经病变的研究
2010-06-07彭永德
张 颖,彭永德
(上海交通大学附属第一人民医院内分泌科,糖尿病研究室,上海 200080)
糖尿病神经病变(diabetic neuropathy)是糖尿病最常见、最复杂的并发症[1]。虽然积极的血糖控制是预防糖尿病神经病变发生的关键,但却很难逆转已存在的病变。目前认为其发生与代谢紊乱、非酶糖基化、微血管病变引起的神经缺血低氧等因素有关,临床以疼痛、麻木及感觉减退为主,严重者可引起自发性疼痛,表现为晨轻暮重,疼痛剧烈时严重影响患者的生活质量。虽然良好的血糖控制可延缓糖尿病神经病变的发生,但对于已经发生的神经病变目前尚缺乏疗效显著的治疗手段。
临床上甲钴胺(弥可保,Mecobalamin)对糖尿病神经病变有一定的疗效,但治疗效果尚不能令人满意。研究显示,线粒体超氧化物产生过多是导致包括糖尿病慢性并发症的共同机制。因此,近几年,临床上使用α-硫辛酸(α-lipoic acid)治疗糖尿病神经病变患者,且收到较满意的效果[2]。本研究通过对比静脉使用弥可保或硫辛酸前、治疗2周后及两组间患者血糖、糖化血红蛋白水平、症状总评分、神经传导速度等指标的变化,以更好地评估弥可保和硫辛酸治疗糖尿病周围神经病变的安全性及有效性。
1 资料与方法
1.1 一般资料
伴有不同程度的糖尿病周围神经病变的2型糖尿病患者共40例,排除其他原因所致的周围神经病变,随机分为硫辛酸治疗组和弥可保治疗组,每组各20例。硫辛酸组中,男11例,女9例;弥可保组中,男10例,女10例。两组患者的性别构成、年龄、糖尿病病程、糖化血红蛋白比较,差异均无统计学意义,见表1。
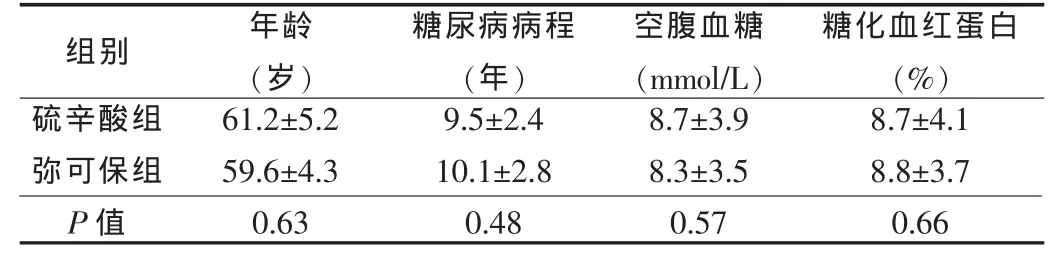
表1 两组患者一般情况比较(x±s)
1.2 方法
硫辛酸组:硫辛酸静脉滴注,600 mg/d,用药2周;弥可保组:弥可保静脉滴注,500μg/d,用药2周。在治疗期间,保持两组患者血糖、血压的稳定。两组糖尿病患者,均于治疗前晨起静脉采血测定血糖、血电解质、肝肾功能、糖化血红蛋白,进行神经症状评分,并测定神经传导速度。治疗过程中每天监测血糖、血压,同时观察记录两组患者在治疗过程中出现的副作用。共治疗2周,治疗结束后重复进行开始时的项目检测。
1.3 统计学处理
研究中所得计量资料以均数±标准差(x±s)表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
两组患者治疗后与治疗前空腹血糖、糖化血红蛋白、腓浅神经传导速度、症状评分比较,差异均有统计学意义(P<0.05),见表2、3。两组间治疗后的空腹血糖、糖化血红蛋白、腓浅神经传导速度、症状评分、肝肾功能比较,差异均无统计学意义(P>0.05),见表 4。
由运动和感觉症状(包括阴性和阳性症状)测验所得的评分是评估神经病变症状的独立指标。治疗后较治疗前无论是阳性症状(如刺痛、烧灼感、感觉过敏或麻木等),还是阴性症状(痛、温、触觉丧失),均较基线水平有显著改善(P<0.01)。见表 2、3。
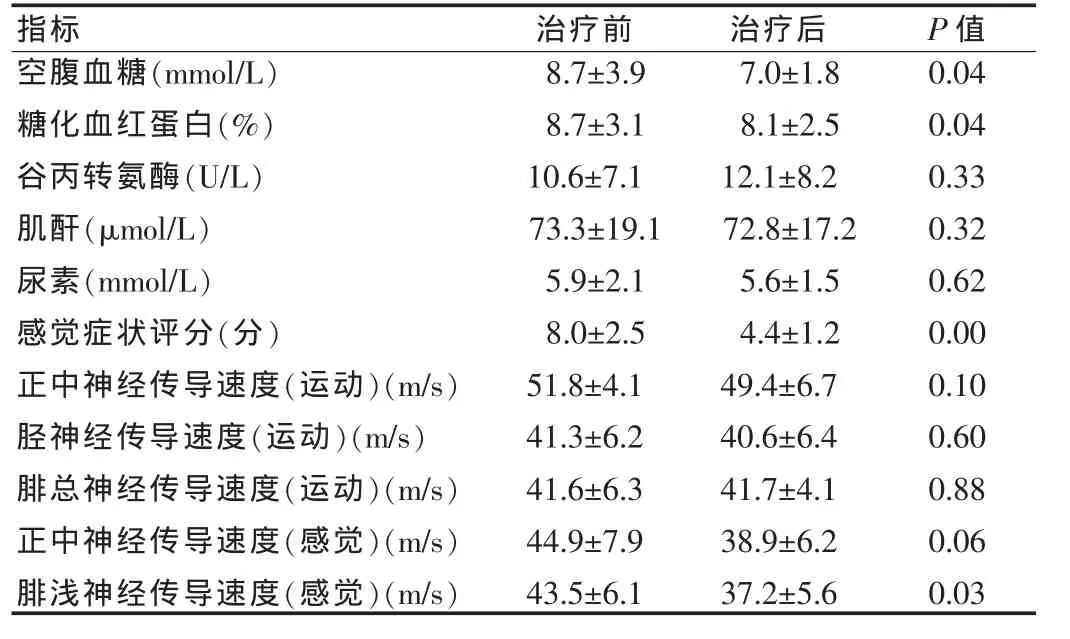
表2 硫辛酸组治疗前后各项指标比较(x±s)
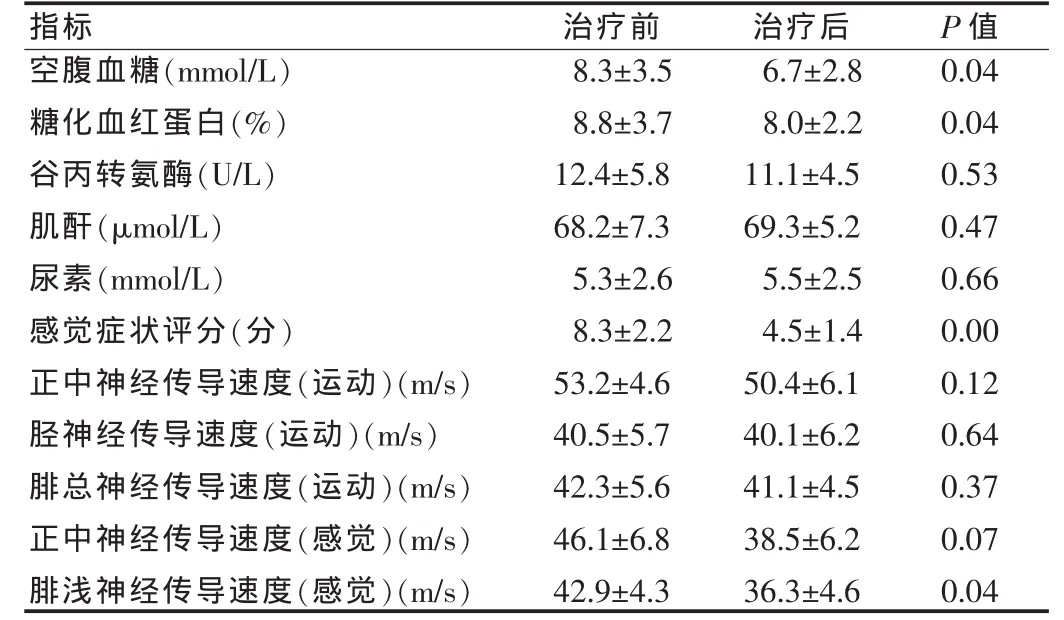
表3 弥可保组治疗前后各项指标比较(x±s)
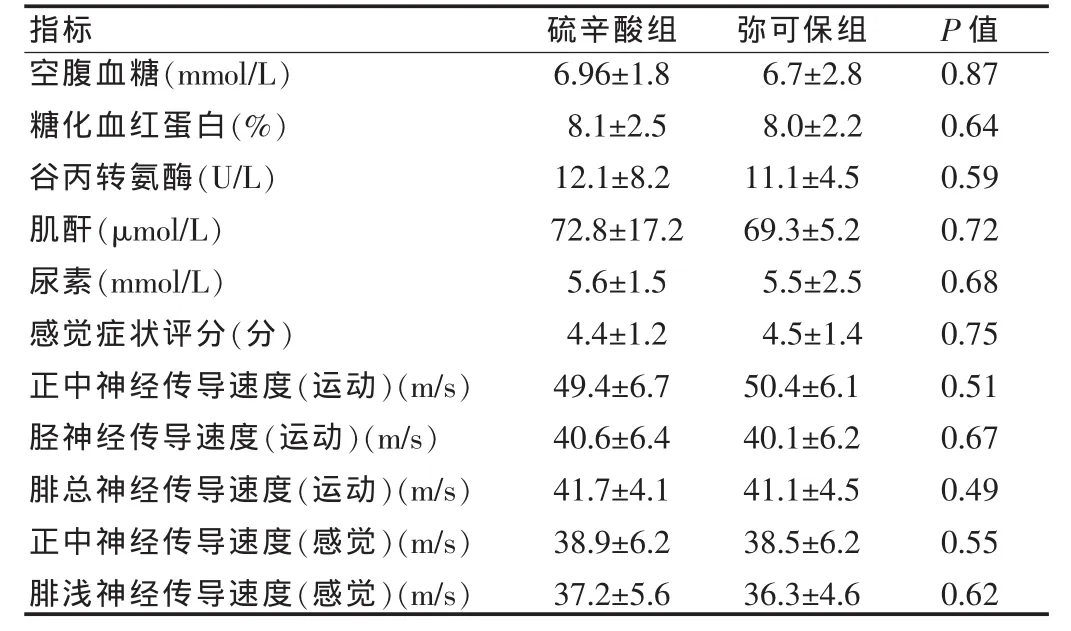
表4 两组治疗后各项指标比较(x±s)
3 讨论
糖尿病神经病变是常见并发症之一,可累及包括自主神经和周围神经在内的所有神经,尤以下肢的感觉神经最早受累,出现麻木、自发性疼痛、感觉异常等各种临床症状,累及自主神经时可出现出汗异常、残余尿增多、直立性低血压、腹泻与便秘交替等症状。糖尿病神经病变发病率高,治疗效果欠佳,且严重影响患者的生活质量,亟待有更有效的药物进行治疗。目前对糖尿病神经病变发病机制尚未完全阐明,较公认的为与血管障碍、代谢紊乱及神经营养因子减少有关,导致以阶段性脱髓鞘为主要病理改变的神经纤维脱髓鞘改变及变性坏死。
弥可保通过自身甲基化的功能,参与体内甲基转移作用,从而促进神经组织内的核酸、蛋白质及脂肪的新陈代谢,加速DNA、RNA的合成,并通过促进髓鞘的主要构成脂质——卵磷脂的合成,加快修复损伤的神经组织,因而起到改善神经组织传递及代谢障碍的作用。此外,该药还具有抑制神经组织异常兴奋传导的作用。因此,被广泛地应用于临床。
α-硫辛酸是一种强力的抗氧化剂[3],可强效清除氧自由基、再生体内其他抗氧化剂、螯合金属离子,同时抑制脂质过氧化、增加神经营养血管血流量、改善神经传导速度,还可以阻断蛋白质糖基化,缓解糖尿病相关的神经性疼痛。另外,还能增加神经Na+-K+-ATP酶活性,保护血管内皮功能。在实验性糖尿病和人体中硫辛酸均被证实可预防神经传导异常,改善神经传导特性、神经内微循环和神经细胞Na+-K+-ATP酶活性,因此可以改善神经病变的阳性感觉症状[4]。有研究对包括1 258例受试者在内的4项随机、双盲、安慰剂对照、平行组临床试验进行了荟萃分析,结果显示,α-硫辛酸600 mg/d、静脉滴注3周,可显著改善各种糖尿病周围神经病变的临床症状,尤其以疼痛和麻木改善最为显著,并增加神经反应性和传导速度[5]。
本研究通过应用综合神经病变四项阳性感觉症状指标的总症状评分作为主要终点指标来评价药物对糖尿病神经病变的作用[6]。研究提示,静脉应用硫辛酸或弥可保2周均可明显改善神经病变的临床症状(疼痛、麻木感、感觉异常和烧灼感)。笔者认为,无论神经病变查体结果或神经损害程度为何,这四项症状本身就能严重伤害患者的健康状态,影响患者的生活质量。有研究认为,神经病变阳性感觉症状是独立于阴性症状(痛、温、触、位置、振动觉等其他感觉丧失)而存在的。作为临床医生,我们评判药物的疗效不仅仅是神经传导速度的改善,还有患者主观症状的好转。本研究中,两组患者的阳性感觉症状评分及神经传导速度均较治疗前有所改善,且两组治疗后各项指标间差异无统计学意义,说明硫辛酸和弥可保均对糖尿病周围神经病变有一定的治疗效果,且对糖尿病的疼痛症状均能起到缓解作用。
另外,在临床上我们发现,在某些初发的多发性神经病变患者中,阳性症状可以非常明显,但神经系统查体及神经传导速度检查可仅有少许异常甚至正常。此后,随着神经病变的进一步发展,阳性感觉症状逐渐减退,阴性症状和神经损害可能进一步明显与恶化。而且,我们还注意到阳性感觉症状比阴性症状更让人苦恼,会迫使患者就诊以求缓解疼痛,并且比阴性症状或神经损害更容易影响患者的工作、生活及社会责任,甚至引起精神症状[7-8]。这类患者如果使用弥可保治疗,不仅不能减轻疼痛,有一部分患者还有症状加剧的主诉,而此类患者经使用硫辛酸后症状有较大程度的缓解。这些神经病变阳性症状被认为是由于细纤维感觉神经受损所致。虽然镇痛剂、抗癫痫药及安定药可以缓解神经病变阳性感觉症状,但是通过其他机制,如改善神经病理生理状况,也可以改善这些症状,这可能与硫辛酸的抗氧化作用有关。动物实验和组织培养的研究表明,自由基介导的氧化应激与糖尿病多发性神经病变的发生有关,可以引起神经血管损伤,从而导致神经细胞内低氧,继而出现神经功能障碍。应用生理性的抗氧化剂,包括硫辛酸(强力亲脂性自由基清除剂),提供了一个潜在的治疗基础。糖尿病患者外周神经也存在氧化应激的迹象。糖尿病中造成氧化应激的原因可能有几种,包括糖化作用、过渡金属区隔化的丧失以及糖尿病组织细胞出现的低氧状态,导致患者体内的脂质氢过氧化物水平、DNA加合物水平、羰基蛋白水平增加。硫辛酸由于有抗氧化作用,特别适于防治由氧族、氮族的活泼产物过盛而引起的糖尿病并发症。在糖尿病后期并发症的处理中,治疗神经疼痛症状和改善生活质量也同样具有很突出的作用。
[1]Vileikyte L,Peyrot M,Gonzalez JS,et al.Predictors of depressive symptoms in persons with diabetic peripheral neuropathy:a longitudinal study[J].Diabetologia,2009,52(7):1265-1273.
[2]Ziegler D,Ametov A,Barinov A,et al.Oral treatment with alpha-lipoic acid improves symptomatic diabetic polyneuropathy:the SYDNEY 2 trial[J].Diabetes Care,2006,29(11):2365-2370.
[3]Ziegler D,Reljanovic M,Mehnert H,et al.Alpha-lipoic acid in the treatment of diabetic polyneuropathy in Germany:current evidence from clinical trials[J].Exp Clin Endocr Diabetes,1999,107:421-430.
[4]Dyck PJ,Thomas PK.Diabetic Neuropathy[M].2nd ed.Philadelphia:W.B.Saunders Company,1999:317-329.
[5]Ziegler D,Hanefeld M,Ruhnau KJ,et al.Treatment of symptomatic diabetic polyneuropathy with the antioxidant alpha-lipoic acid:a 7-month multicenter randomized controlled trial(ALADIN III Study).ALADIN III Study Group.Alpha-lipoic acid in diabetic neuropathy[J].Diabetes Care,1999,22(8):1296-1301.
[6]Ankova T,Cherninkova S,Koev D.Treatment for diabetic mononeuropathy with alpha-lipoic acid[J].Int JClin Pract,2005,59(6):645-650.
[7]Apfel SC,Asbury AK,Bril V,et al.Positive neuropathic sensory symptoms as endpoints in diabetic neuropathy trials[J].JNeurol Sci,2001,189:3-6.
[8]The Diabetes Control and Complications Trial Research Group.The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus[J].N Engl JMed,1993,329:977-986.
