制备方法对Pt/CA催化剂电化学性能的影响*
2010-06-05魏松丽吴丁财符若文
魏松丽,吴丁财,符若文
(中山大学化学与化学工程学院∥聚合物复合材料及功能材料教育部重点实验室,广东 广州 510275)
直接甲醇燃料电池(DMFC)具有能量损耗少、低污染、能量密度高、噪声低等优点,被认为是未来电动汽车动力及其它民用场合最有希望的化学电源[1-2]。目前,直接甲醇燃料电池的制备关键技术已经成熟,但DMFC多采用价格昂贵的金属铂作为催化剂,限制了其应用[3-4]。为了降低成本,减少铂的用量,提高铂的分散度,现普遍采用的方法之一是选择具有高比表面积的材料如石墨、活性炭等作为载体。
炭气凝胶是一种由纳米炭颗粒相互连结而成的轻质纳米中孔炭材料。其孔隙率高达80%~98%,孔隙尺寸小于50 nm,比表面积高达400~1 100 m2/g。此外,炭气凝胶的网络炭骨架还具有优良的导电性能,导电率为10~40 S/cm[5]。它可以根据需要生产成不同的形状,如块状、珠状和薄膜纸状,并且通过调节间苯二酚与催化剂的比例和凝胶的浓度,可以控制炭气凝胶的孔径尺寸,从而能够合成所需要的结构,因此炭气凝胶成为理想的DMFC电催化剂载体。DMFC中通常采用w=20% Pt/C作为阳极催化剂。采用不同的制备工艺,得到的Pt颗粒大小不同,Pt(111)与Pt(100)晶面暴露程度也不同。Pt催化剂的催化活性受颗粒尺寸影响,而Pt(111)与Pt(100)晶面对阳极催化反应具有不同的催化活性[6-7]。因而有必要研究不同制备方法得到的Pt/CA催化剂对DMFC中催化剂的催化活性的影响。
本文应用中山大学材料科学研究所符若文小组开发出的常压干燥制备技术制备的炭气凝胶为载体,分别以甲醛、硼氢化钠和乙二醇为还原剂制备了w=20%负载量的DMFC阳极催化剂Pt/CA。考察了制备方法对Pt/CA催化剂电化学性能的影响。
1 实验部分
1.1 炭气凝胶的制备
采用甲醛和间苯二酚为单体,蒸馏水为溶剂,十六烷基三甲基溴化铵(CTAB)为催化剂,根据设定配方混合均匀,在体积约为20 mL的小瓶中封装好,置于75 ℃水浴中恒温5 d,使其发生溶胶-凝胶反应,并经老化得到有机凝胶。到达预定反应时间后,将样品从小瓶中取出,直接放于室温中自然干燥1 d,然后在红外灯下(约为60 ℃)烘1 d,最后放入烘箱中110 ℃烘干3 h,得到有机气凝胶。将干燥好的有机气凝胶放入炭化炉内,在800 mL/min氮气保护下以5 ℃/min的升温速率从室温加热到900 ℃,并在此温度下保持2 h,进行炭化;然后,让其自然冷却至室温,得到炭气凝胶,记为CA。
1.2 Pt/CA催化剂的制备
采用乙二醇还原法制备催化剂,具体步骤为:称取80 mg炭气凝胶,于乙二醇溶液中超声振荡30 min制得碳浆,在快速搅拌下向其中加入一定体积的氯铂酸溶液(ρ(Pt)=14.8 mg/mL),搅拌一定时间至形成均匀浆液。在惰性气体保护下滴加2.0 mol/L的NaOH(EG溶液),调节浆液至碱性,升温至130 ℃还原一定时间,然后降至室温。过滤所得黑色产物并用大量去离子水洗涤,80 ℃真空干燥8 h,即得w=20% Pt负载量的Pt/CA-EG催化剂。本论文中所有样品以Pt/CA-XX表示,其中XX表示所用还原剂。
采用甲醛还原法制备催化剂的步骤为:称取80 mg炭气凝胶,在乙醇-水混合溶液中超声分散,制得碳浆。在快速搅拌下加入氯铂酸溶液,搅拌2 h至形成均匀浆液,加入NaOH水溶液调节至碱性,滴加过量甲醛,在惰性气体保护下于80 ℃反应2 h后降至室温,过滤干燥同EG法,即得w=20% Pt负载量的Pt/CA-HCHO催化剂。
采用硼氢化钠还原法制备催化剂的步骤为:称取80 mg炭气凝胶超声分散于去离子水中,制得碳浆。在快速搅拌下加入氯铂酸溶液,搅拌2 h至形成均匀浆液,在室温和酸性条件下,缓慢滴加过量的NaBH4溶液(0.01 mol/L),强烈搅拌1 h,过滤干燥同EG法,即得w=20% Pt负载量的Pt/CA-NaBH4催化剂。
1.3 物化性能和电化学性能表征
采用日本理学RIGAKU D/MAX 2200 VPC型X射线衍射仪测定催化剂的晶体结构,Cu Kα射线源,扫描速度为10°/min;采用美国热电TJA公司的IRIS Advantage全谱直读等离子体发射光谱仪(ICP)测定催化剂中Pt的实际含量。
催化剂对于甲醇氧化反应催化活性的测试在CHI-750A型电化学工作站上进行:取一定量的催化剂样品加入分散溶液中,超声分散得催化剂悬浊液。用微型注射器吸取一定量的悬浊液均匀涂覆在直径为4 mm的玻炭电极表面,充分干燥后作为工作电极,并以饱和甘汞电极为参比电极,Pt丝为对电极组成三电极体系。电解液为0.5 mol/L H2SO4溶液和0.5 mol/L H2SO4+2.0 mol/L CH3OH的混合溶液。测试前一般都在电位区间内以100 mV/s的速度扫10个循环清洗催化剂表面,然后在同样范围内以50 mV/s的速度再扫2个循环。
2 结果与讨论
2.1 不同还原剂制备的的炭气凝胶负载Pt催化剂的Pt粒径大小
为了考察用不同RC比的炭气凝胶负载Pt所制备的Pt/CA 电催化剂上Pt颗粒尺寸,对所制得的 Pt/CA 电催化剂进行了XRD测试,得到的XRD曲线如图1所示。
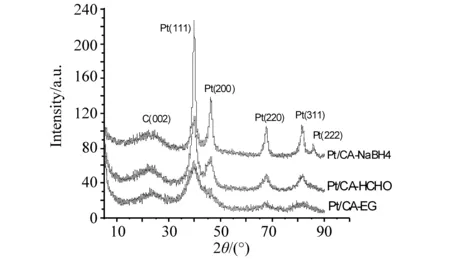
图1 不同还原剂所制备催化剂的XRD衍射图
从图1的图谱上可以看出3个催化剂均在2θ=24.6°处出现衍射峰,可归属为碳黑中的石墨(002)晶面。催化剂在衍射角2θ为39.9°,46.1°,67.2°和81.4°出现了明显的金属Pt X射线特征衍射峰,各衍射峰分别归属为Pt(111),Pt(200),Pt(220)和Pt(311)晶面,4个催化剂都表现为Pt的面心立方结构。这些证实了Pt以单质形式负载在炭气凝胶上。但由于金属粒子太小,衍射峰宽化。采用Sherrer公式[8]计算这4种催化剂的粒径大小时,选择不受载体干扰的Pt(220)晶面衍射峰。4种催化剂样品中,Pt/CA-EG,Pt/CA-HCHO和Pt/CA-NaBH4催化剂上Pt粒子平均粒径分别为2.2,3.1和6.7 nm,也就是说Pt/CA-EG催化剂上Pt的粒径最小,这说明Pt在该催化剂上的分散度最高,Pt/CA-HCHO次之,Pt/CA-NaBH4催化剂上Pt粒径最大,达到6.7 nm,其分散度最差。这可能是因为NaBH4是较强的还原剂,在催化剂制备过程中金属的还原速度较快, 从而使载上去的Pt颗粒增长很快,从而尺寸很大。上述结果也说明,在 Pt/CA-EG催化剂上Pt粒子的聚集程度最小,这是因为乙二醇是一种弱还原剂,它可以同时起到分散和还原的作用,所以使载上去的Pt尺寸很小,根据“粒径效应”[9-10],催化剂中 Pt 晶粒的粒径大小决定了其表面积大小和晶相结构,从而对氧化还原反应表现出不同的催化活性。在一定的粒径范围内,Pt 粒径减小,催化剂比表面积增大,有利于在 DMFC 的气体扩散电极(氢电极和氧电极)中形成较大的传递和反应界面,从而提高电极的性能。
2.2 不同还原剂制备的炭气凝胶负载Pt催化剂的电化学性能研究
图2是不同还原剂制备的炭气凝胶负载Pt催化剂的循环伏安曲线对比图,图中电流密度是电极的几何面积。从图2可以看出,3种催化剂的循环伏安曲线形状相同,但氢的吸脱附峰大小相差很大。其中Pt/CA-EG催化剂的氢吸脱附峰最大,说明其电催化性能最好。氢的吸脱附峰面积可以用来计算催化剂的电化学活性面积(ECA)。根据公式(1)可以算出 Pt/CA-EG, Pt/CA-HCHO和Pt/CA-NaBH4催化剂的电化学活性面积分别为74.1,34.9和26.8 m2/g[11]。
ECA=QH/(LPt*QH-ref)
(1)
式中:ECA为H吸脱附法测得的电化学表面积的数值,m2/g;QH是H吸/脱附电量,μC;QH-ref是多晶铂电极表面氢吸脱附电量常数,为210 μC/cm2[12-13]。
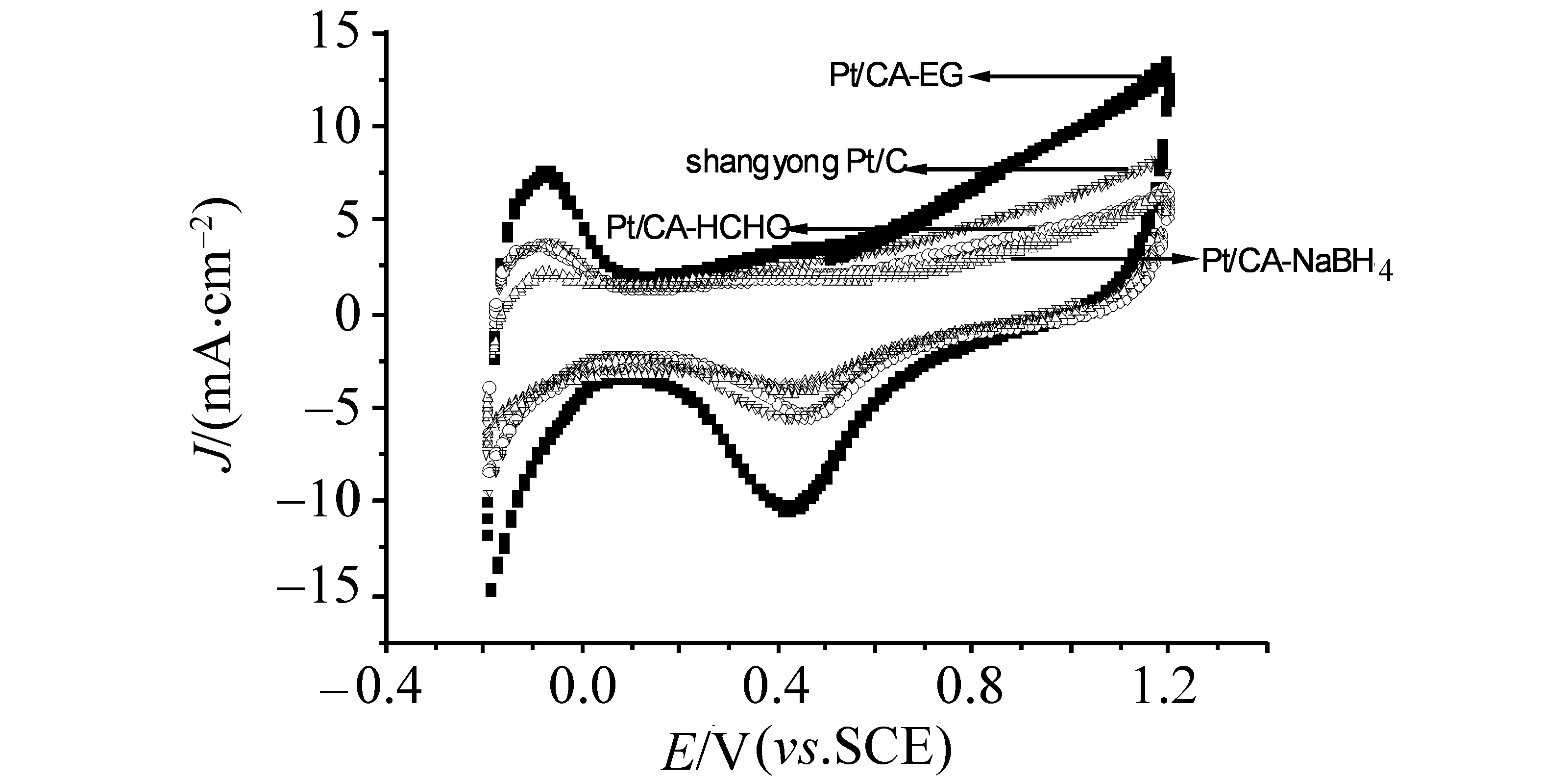
图2 不同还原剂制备的炭气凝胶负载Pt催化剂的循环伏安曲线比较(N2饱和的0.5 mol/L H2SO4)
同时为了评价不同还原剂制备的炭气凝胶负载Pt催化剂的比质量活性,进行了其对甲醇氧化性能的比较。图3为不同还原剂制备的炭气凝胶负载Pt催化剂的甲醇氧化性能比较图,图中电流密度是电极的几何面积。从图3中可知,甲醇在Pt/CA-EG上的氧化峰电流密度(59.4 mA·cm-2)最高,在Pt/CA-HCHO催化剂上的氧化峰电流(38.2 mA·cm-2)次之,在Pt/CA-NaBH4上的氧化峰电流(24.9 mA·cm-2)最低。而商用催化剂的峰电流密度略高于Pt/CA-NaBH4,大约在28.3 mA·cm-2。 这表明催化剂对甲醇催化还原的活性按照相同的顺序降低。我们通常采用正向扫描时氧化峰电流的大小衡量催化剂催化氧化活性的高低,并根据公式(2)计算出催化剂的比质量活性。
MA=Jp/md
(2)
式中:Jp是甲醇氧化的峰电流密度,mA·cm-2;md为单位面积电极上Pt的质量,mg·cm-2。
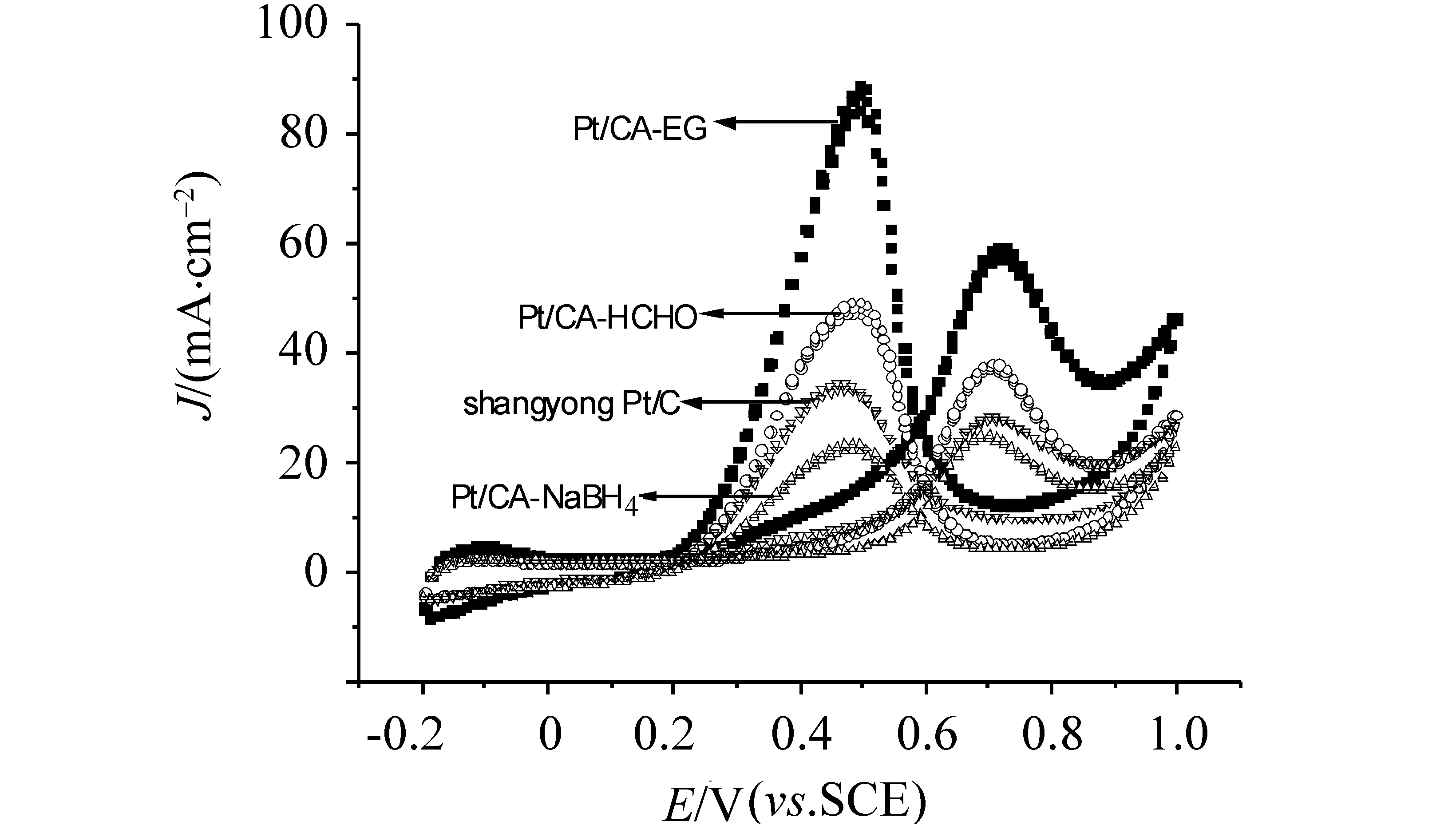
图3 不同还原剂制备的Pt/CA催化剂的甲醇氧化性能比较(N2饱和的0.5过mol/L H2SO4 + 2mol/L CH3OH)
从表1可以看出, Pt/CA-EG,Pt/CA-HCHO和Pt/CA-NaBH4的比质量活性依次为248.8,160.1和104.8 A·g-1,其结果与电化学活性比表面积的结果相符,也是Pt/CA-EG的电催化性能最好。
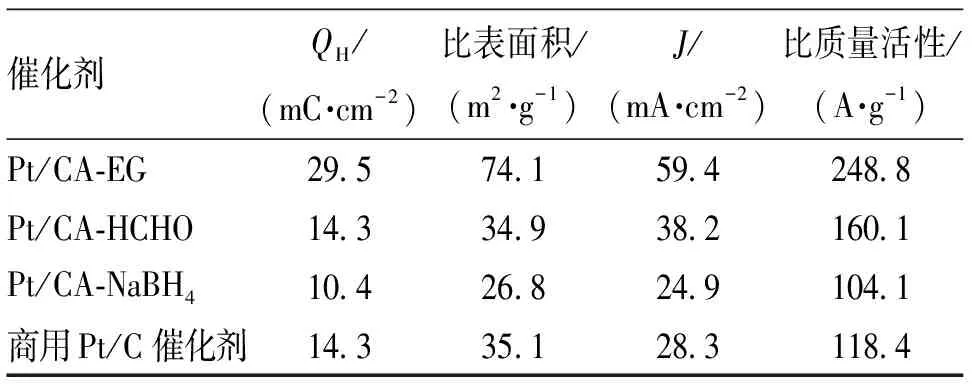
表1 不同还原剂制备的炭气凝胶负载Pt催化剂的电化学活性比表面积和比质量活性
氢气吸附测试以及甲醇氧化性能测试结果均表明,Pt/CA-EG对甲醇的催化氧化性能明显好于Pt/CA-HCHO和Pt/CA-NaBH4催化剂,并且要远远好于商用催化剂。对甲醇电氧化机理的研究表明,甲醇先在Pt催化剂上发生脱氢反应,由于C-O键在低温下难以断裂,导致脱氢后的CO成为毒物强吸附在Pt的活性位上,使反应不能继续进行。甲醇在电化学氧化反应过程中,会产生类似的毒物使Pt催化剂中毒。
2.3 乙二醇液相还原法制备炭气凝胶负载铂催化剂机理的初步探讨
讨论了不同还原剂对制备的Pt/CA催化剂性能的影响,发现用乙二醇做还原剂所制备的催化剂性能最好。这是因为乙二醇在催化剂的制备过程中起着重要作用。根据文献[14-17]报道,乙二醇在反应过程中可能有三方面的作用:其一,乙二醇的黏度较高,高黏度的溶剂阻碍了金属粒子的扩散迁移,使金属粒子长大的过程成为扩散控制的过程;其二,乙二醇的沸点较高,可通过升高到较高的温度使金属盐发生强制性的水解,形成氢氧化物的胶体,再进一步还原为零价的金属;其三,乙二醇是一种典型能形成分子间氢键的有机溶剂,分子间氢键的形成使乙二醇形成一个类环状物,它能与氢氧化物进一步形成氢键,起到了与高分子化合物类似的保护作用。下面我们对炭气凝胶负载金属Pt催化剂的制备过程进行简要的描述。

第二步,金属Pt粒子的制备。由于乙二醇沸点较高,温度升高到一定程度可使金属盐发生强制性的水解,形成氢氧化物的胶体,再进一步还原为零价的金属Pt。
第三步,金属Pt粒子的沉积。通过调节pH值使被还原的金属Pt粒子沉积到炭气凝胶表面,并吸附在炭气凝胶的孔中。
通过以上步骤的分析,认为乙二醇是氯铂酸的还原剂,使其还原成零价的金属铂;同时它还起到分散剂和保护剂的作用,从而使金属铂均匀地分散到炭气凝胶上。
3 结 论
采用浸渍液相还原法分别使用甲醛、硼氢化钠和乙二醇作为还原剂制备了w=20%负载量的 Pt/CA 催化剂。发现3种催化剂的活性大小顺序为Pt/C(EG)>Pt/C(HCHO)>Pt/C(NaBH4)。采用乙二醇还原法制备的Pt/C催化剂Pt聚集程度最小,其粒径最小,Pt的电化学表面积最大。在3种还原方法中乙二醇还原法是制备高载量高分散的 Pt/C 催化剂最适合的方法,并且其电化学性能远远好于商用催化剂。而乙二醇液相还原法制备炭气凝胶负载铂催化剂的过程主要包括炭浆的制备,金属铂粒子的制备和金属铂粒子的沉积。
参考文献:
[1] PRATER K B. Polymer electrolyte fuel cells: a review of recent developments [J]. J Power Sources,1994,51:129-144.
[2] SRINIVASAN S, MANKO D J, KOCK H, et al. Recent advance solid in polymer electrolyte fuel cell technology with low platinum loading electrodes[J]. J Power Source,1990, 29:367-387.
[3] THOMPSON S D, JORDAN L R, FORSYTH M. Platinum electro-deposition for polymer electrolyte membrane fuel cells [J]. Electrochimica Acta, 2001,46:1657-1663.
[4] 都君华,李伟善,陈红雨,等.质子交换膜燃料电池催化剂的研究进展[J]. 电池工业, 2002,7(2):78-80.
[5] BESSEL C A, LAUBERNDS K, RODRIGUEZ N M, et al. Graphite nanofibers as an electrode for fuel cell applications[J]. J Phys Chem B, 2001, 105(6): 1115.
[6] PRATER K B.Polymer electrolyte fuel cells a review of recent development[J]. J Power Source, 1994,51:129.
[7] GIODANO N, PASSALACQUA E, PINO L.Analysis of platinum particle size and oxygen reduction in phosphoric acid[J].Electrochimica Acta, 1991, 36:1979.
[8] WHITE J H, SAMMELLS A F, PEROVSKITE. Anode electrocatalysis for direct methanol fuel cells[J]. J Electrochem Soc, 1993, 140(8):2167-2176.
[9] WATANABE M, SAEGUSA S. High platinum electrocatalsyt utilizations for direct methanol oxidation[J].J Electroanal Chem,1989,271:213-220.
[10] FRELINK T, VISSCHER W, VEEN J A R van. Particle size effect of carbon-supported platinum catalysts for the elcetrooxidation of methanol[J]. J Electroanal Chem, 1995,382:65-72.
[11] ANTOLINI E, GIORGI L, P0OAIO A, et al. Influence of nafion loading in the catalyst layer of gas-diffusion electrodes for PEFC[J]. J Power Sources, 1999,77 (2): 136-142.
[12] FOURNIER J, FAUBERT G, TILQUIN J Y, et al. High-performance, low Pt content catalysts for the electroreduction of oxygen in polymer-electrolyte fuel cells[J]. J Electrochem Soc, 1997, 144(1):145-154.
[13] PARK K W, CHOI J H, AHN K S, et al. PtRu alloy and PtRu-W03nanocomposite electrodes for methanol electrooxidation fabricated by a sputtering deposition method[J]. J Phys Chem B,2004,108 (19):5989-5994.
[14] 周振华.直接甲醇燃料电池:高分散高负载铂基电催化剂的制备规律研究[D].大连:中国科学院大连化学物理研究所,2003.
[15] 姜鲁华,臧海霞,孙公权,等. 制备方法对直接乙醇燃料电池阳极PtSn/C催化剂性能的影响[J]. 催化学报,2006, 27(1):15-19.
[16] WANG H J, YU H, PENG F, et al. Methanol electrocatalytic oxidation on highly dispersed Pt/sulfonated-carbon nanotubes catalysts[J]. J Electrochemistry Communications, 2006(8): 499-504.
[17] DU H D,LI B H, KANG F Y,et al. Carbon aerogel supported Pt-Ru catalysts for using as the anode of direct methanol fuel cells[J]. Carbon,2007,45:429-435.
