50℃时(NH4)2SO4-NH4NO3-H2O三元体系相图研究
2010-06-04,,,
,, ,
(武汉科技大学化学工程与技术学院,湖北 武汉 430081)
水盐体系是无机化工生产(肥料、无机盐、盐湖)常见的反应体系[1~3]。在水盐体系发生溶解、结晶、蒸发、冷却、分离等相变过程中,首先需要了解盐类的溶解度规律。水盐体系的相图不仅能给出盐类溶解或结晶顺序、名称和组成,还能进行物料的计算;并为化工工艺过程及反应器的设计提供依据[4]。
燃煤排放的SO2一般用石灰石钙法脱除,但钙法存在产物石膏销路不畅、投资多、占地面积大、产生二次污染等问题,氨法烟气脱硫技术近年来备受社会关注。氨法脱硫工艺在脱硫的同时又可脱氮,可产生一定的经济效益,是一项适应长远发展要求、极具推广价值的环保的脱硫技术[5,6]。氨法脱硫产生的脱硫液含有硫酸铵、碳酸铵、硝酸铵等盐,作者通过研究(NH4)2SO4-NH4NO3-H2O三元体系的相平衡数据,拟为脱硫液回收提供依据。
1 实验
1.1 试剂与仪器
NH4NO3、(NH4)2SO4、NaNO3、Na2SO4,均为分析纯。实验用水为去离子水(pH≈6.6)。
AL204型电子天平(±0.0001 g);ICS-90型离子色谱仪,美国戴安公司;BHW-100型恒温水浴锅(温度波动在±0.1℃)。
1.2 装置
在恒温水浴锅中加入电动搅拌器,相平衡装置采用直塑料管,装样后固定在转动盘上,置于恒温水浴锅中。实验装置如图1所示。
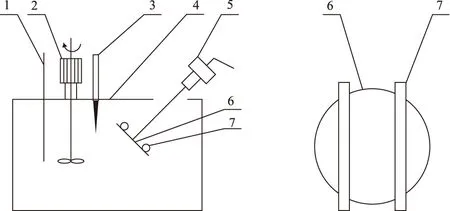
1.精密温度计 2.电动搅拌器 3.温度调节器 4.恒温水浴5.电动机 6.转动盘 7.平衡管
1.3 方法
1.4 分析测试
2 结果与讨论
2.1 (NH4)2SO4-NH4NO3-H2O三元体系的固液平衡数据
利用等温溶解平衡法测定50℃时(NH4)2SO4-NH4NO3-H2O三元水盐体系的溶解度,应用湿渣法确定固相的组成,结果见表1。

表1 50℃(NH4)2SO4-NH4NO3-H2O体系的 固液平衡数据/%
2.2 (NH4)2SO4-NH4NO3-H2O三元水盐体系相图
根据固液平衡数据,利用直角等腰三角形表示法,绘制50℃时(NH4)2SO4-NH4NO3-H2O三元水盐体系相图,见图2。

图2 50℃时(NH4)2SO4-NH4NO3-H2O三元水盐体系相图
由图2可知,50℃时(NH4)2SO4-NH4NO3-H2O体系属于复杂体系,存在纯(NH4)2SO4和纯NH4NO3的结晶,又存在以(NH4)2SO4为主的固溶体和以NH4NO3为主的固溶体的结晶。 AM和BF为纯NH4NO3和纯(NH4)2SO4的溶解度曲线。以(NH4)2SO4为主的固溶体,其组成从纯(NH4)2SO4的D点连续地变化到G点,溶解度曲线为EF;以NH4NO3为主的固溶体,其组成从纯NH4NO3的C点连续地变化到N点,溶解度曲线为EM。根据相律,4条溶解度曲线为单变量曲线,确定其中一种盐的含量,另外一种盐的含量一定。
(NH4)2SO4-NH4NO3-H2O体系的相图中,E点为三元体系的共饱和点,由相律可知,自由度为零,其组成为(NH4)2SO4的质量分数6.85%、NH4NO3的质量分数57.84%。NH4NO3对(NH4)2SO4具有强烈的盐析作用,(NH4)2SO4-H2O二元体系溶解度为46.43%(B点),共饱和点E处则降为6.85%,(NH4)2SO4对NH4NO3也具有较强的盐析作用,NH4NO3-H2O二元体系溶解度为77.12%(A点),E点则降为57.84%。
相图分为6个区域,BDF为纯(NH4)2SO4的结晶区,ACM为纯NH4NO3的结晶区,EFDG为以(NH4)2SO4为主的固溶体结晶区,EGN为以(NH4)2SO4为主的固溶体和以NH4NO3为主的固溶体共同结晶区,ENCM为以NH4NO3为主的固溶体结晶区,以及AEB与坐标轴围成的不饱和区。
2.3 讨论
(1)形成固溶体需要具备下列条件[7]:①晶格的类型相同;②晶格参数大小相近;③原子结构相似;④熔点接近。可能由于(NH4)2SO4和NH4NO3属于同一晶系,都为斜方晶体,具备了形成固溶体的主要条件。
(2)由于NH4NO3的加入对(NH4)2SO4的同离子效应,使(NH4)2SO4的溶解度下降。而(NH4)2SO4的加入同样对NH4NO3具有同离子效应,也使得NH4NO3的溶解度下降。
(3)(NH4)2SO4的结晶区明显大于NH4NO3的结晶区,这是因为50℃时NH4NO3的溶解度为77.12%,(NH4)2SO4的溶解度为46.43%,溶解度小的盐容易析出,对应较大的结晶区。只要控制NH4NO3质量分数≤50.17%就能析出(NH4)2SO4晶体,而只有控制(NH4)2SO4质量分数≤2.23%时才能析出NH4NO3晶体,这对分离(NH4)2SO4和NH4NO3有利。
3 结论
(1)利用等温溶解平衡法测定了50℃时(NH4)2SO4-NH4NO3-H2O的溶解度数据,应用湿渣法确定固相的组成,此三元体系属于复杂体系,有固溶体生成。
(2)根据溶解度数据绘制了相图,相图分为6个区域,包括纯(NH4)2SO4的结晶区、纯NH4NO3的结晶区、以(NH4)2SO4为主的固溶体结晶区、以NH4NO3为主的固溶体结晶区、以(NH4)2SO4为主的固溶体和以NH4NO3为主的固溶体共同结晶区及不饱和区。
参考文献:
[1] 樊彩梅.氯化钾与硫酸铵制备硫酸钾的基础研究[J].太原理工大学学报,1998,29(1):88-90.
[2] Goundali B E L,Kaddami M.The ternary system H2O-Fe(NO3)3-Co(NO3)2isotherms 0 and 15℃[J]. Fluid Phase Equilibria, 2007, 260(2): 295-299.
[3] 桑世华,唐明林,殷辉安,等.Na2CO3-Na2B4O7-H2O三元体系288K相平衡研究[J].矿物岩石,2002,22(2):94-96.
[4] 王卫东,汪春华.25℃时NaCl-NH4Cl-H2O三元水盐体系相平衡的研究[J].盐湖研究,2007,15(2):42-44.
[5] 包振蕴.论述氨法烟气脱硫技术[J].科技信息,2007,(34):56-57.
[6] 闫晓光,熊理想,马宏金,等.FCL氨法烟气脱硫技术特点及应用[J].电力环境保护,2008,24(2):11-12.
[7] 牛自得,程芳琴.水盐体系相图及其应用[M].天津:天津大学出版社,2002:47.
