衍生化分光光度法快速测定卡托普利片中主药的含量Δ
2010-05-22熊正平黄开顺朱链链陈志琼
熊正平,黄开顺,朱链链,陈志琼
(重庆医科大学药物分析教研室,重庆市 400016)
卡托普利(Captopril,Cap),化学名为 1-((2S)-2-甲基-3-巯基-1-氧代丙基)-L-脯氨酸,是第1代血管紧张素转化酶(ACE)抑制剂药物,对各种类型高血压均有明显的降压作用,特别是对其它降压药物治疗无效的严重高血压有很好的疗效,是临床上广泛应用的高血压药物,因此建立其制剂中主药含量的简便快速的测定方法具有重要的意义。但是卡托普利中含有不稳定的巯基,所以对其测定有一定难度。现阶段的测定方法研究很多都集中在将巯基衍生化后再进行卡托普利的含量测定,如采用对溴苯甲酰甲基溴(p-BPB)[1,2]、5,5′-二硫-2-硝基苯甲酸(DTNB)[3]、2,2′-二硫二吡啶(2-PDS)[4]等衍生化试剂,但它们的衍生化产物都不太稳定,给测定带来不便。本文在比较多种衍生化试剂后,采用2,4-二硝基氟苯(DNFB)[5]作为衍生化试剂,结果其与卡托普利反应后形成的产物很稳定,再采用简便的分光光度法即可对其含量进行准确测定,结果可靠。
1 仪器与试药
UV-2102PCS型紫外可见分光光度计(尤尼柯上海仪器公司);HS-2D超声波清洗器(上海新芝生物技术研究所);旋涡混合器(海门市其林贝尔仪器制造有限公司);Elgastat UHO超纯水器(英国Elga公司)。
卡托普利对照品(重庆医科大学药物化学教研室提供,批号:20080104,纯度:99.9%);卡托普利片(湖北华中药业有限公司,批号:20080504、20080703、20080903,规格:每片25 mg);DNFB、二甲基亚砜(DMSO)均为化学纯,乙腈为特级纯,氢氧化钠、甲醇、乙酸乙酯及其它试剂均为国产分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 卡托普利贮备液。精密称取卡托普利对照品25 mg,置于25 mL容量瓶中,用水溶解并稀释至刻度,使制备成浓度为1 g·L-1的贮备液。
2.1.2 衍生化试剂。DNFB经减压蒸馏后用乙腈配成0.05%的溶液,避光保存。
2.1.3 NaOH溶液的制备。称取NaOH 1 g置于250 mL的容量瓶中,用水溶解并稀释至刻度,使成0.1 mol·L-1的贮备液,然后再稀释成0.01 mol·L-1的溶液。
2.1.4 供试品溶液的制备。取卡托普利片20片,精密称定,研细。精取适量(约相当于卡托普利25 mg)置于25 mL容量瓶中,加水超声使其溶解,用水稀释至刻度,摇匀,过滤,得续滤液。精密量取续滤液50 μL和DNFB 90 μL置于10 mL的试管中,再加入25 μL NaOH溶液和5 μL DMSO,旋涡1 min后放入40℃水浴,暗处反应45 min后用水稀释到5 mL刻度处,摇匀,即得。
2.2 吸收光谱的制备
量取1 g·L-1的卡托普利对照品50 μL和DNFB 90 μL置于10 mL的试管中,再加入25 μL NaOH溶液和5 μL DMSO,然后将其旋涡1 min后放入40℃水浴中暗处反应45 min,再用水稀释到5 mL刻度处,摇匀。以空白试剂为参比,在200~500 nm波长范围内扫描,同样扫描得到卡托普利对照品、DNFB、供试品和空白辅料溶液(取不含卡托普利的片剂处方中其它辅料,按“2.1”项下“供试品溶液的制备”方法制备)的吸收光谱见图1。

图1 紫外吸收光谱1.DNFB;2.卡托普利对照品;3.衍生反应产物;4.空白辅料Fig 1 UV absorption spectrum1.2,4-dinitrofluorobenzene;2.captopril control;3.product of derivatization reaction;4.blank excipients
从图1可知,卡托普利对照品在202 nm波长处有最大紫外吸收(曲线2),但是在紫外末端,不宜用于主药的含量测定;而用DNFB(曲线1)衍生后使其吸收峰波长增至(342±1)nm(曲线3),且衍生产物稳定,有利于测定卡托普利片的主药含量。同法处理卡托普利片供试品溶液和辅料,结果表明片剂中卡托普利的衍生化产物与对照品产物的吸收光谱一致;片剂辅料不与DNFB发生反应,且在(342±1)nm波长处无吸收(曲线4),将不会干扰卡托普利的测定。因此,本研究以342 nm为测定波长。
2.3 试验条件的考察
2.3.1 反应温度对衍生化反应的影响考察。精密量取1 g·L-1的卡托普利对照品50 μL和DNFB 50 μL置于10 mL的试管中,再加入25 μL NaOH溶液和5 μL DMSO,然后将其旋涡1 min后分别在室温、40℃、60℃和80℃水浴暗处反应45 min后,用水稀释至5 mL刻度处,摇匀,以空白试剂为参比,在342 nm波长处测定吸光度,结果分别是0.211、0.330、0.328、0.339,可见温度会对衍生化反应产生影响,较低的温度不利于反应的发生,升温可以提高反应产率,但是温度超过40℃后反应产率变化不大,所以选择40℃水浴为反应温度。
2.3.2 反应时间的考察。反应其他条件同“2.3.1”,旋涡1 min后放入40℃水浴暗处反应,反应时间分别是15、30、45、60、90、150 min,在342 nm波长处测定的吸光度分别是0.299、0.329、0.332、0.334、0.326、0.326,即反应进行45 min基本达到平衡,故本试验选取45 min为反应时间。
2.3.3 DNFB的用量考察。反应其他条件同“2.3.1”,改变衍生化试剂DNFB溶液的用量,分别加入DNFB 0、50、65、75、85、90、95、100、110 μL,在40 ℃水浴暗处反应45 min后在342 nm波长处测定其吸光度,分别为 0、0.325、0.397、0.412、0.420、0.424、0.416、0.410、0.415。结果表明,卡托普利与DNFB的反应是一个可逆反应,稍过量的DNFB有利于衍生化产物的形成,但是过量太多反而会使衍生产物量减少,所以DNFB选取量为90 μL。
2.3.4 NaOH溶液的用量考察。反应其他条件同“2.3.1”,改变NaOH溶液用量,分别加入NaOH溶液0、10、20、25、30、35、40 μL,在40℃水浴暗处反应45 min后在342 nm波长处测定其吸光度,结果如图2所示。

图2 NaOH溶液的用量对反应的影响Fig 2 Effect of the amount of NaOH solution on derivatization reaction
由图2可以看出,当NaOH溶液加到20 μL后吸光度变化不大,所以本试验NaOH溶液选用25 μL。
2.3.5 衍生物的稳定性考察。反应其他条件同“2.3.1”,在40℃水浴暗处反应45 min后用水稀释至5 mL时及室温放置20、40、60、90、150 min、24 h后测定吸光度。其结果分别为0.421、0.421、0.420、0.420、0.420、0.420、0.420。可见吸光度在24 h内没有明显变化,所以在室温状况下,衍生化反应产物在24 h内都可以稳定存在,使测定更为方便。
2.4 标准曲线的制备
取7支试管,分别精密量取1 g·L-1的卡托普利对照品0、5、20、30、40、50、70 μL和DNFB 90 μL,其他操作照“2.1.4”项下“于10 mL的试管中”起,同法操作,以空白试剂为参比,在342 nm波长处测定吸光度,以吸光度(A)对卡托普利的质量浓度(ρ)进行回归分析,得回归方程ρ=25.153A-0.0916(r=0.9999),结果表明卡托普利检测浓度在1.0~14.0 μg·mL-1的范围内有良好的线性关系。
2.5 方法的重复性
取同一样品5份,按“2.1.4”项下供试品溶液的方法操作,间隔不同时间测定吸光度,考察日内精密度,结果RSD=0.24%(n=5);取同一样品于1周内不同日测定吸光度考察日间精密度,结果RSD=1.37%(n=5),表明方法的重复性很好。
2.6 回收率试验
分别精密称取卡托普利对照品适量置于25 mL容量瓶中,分别加入处方量的各种辅料,按“2.1.4”项下供试品溶液的方法操作,低、中、高3个浓度(每个浓度平行测定3份)下回收率计算结果如表1。
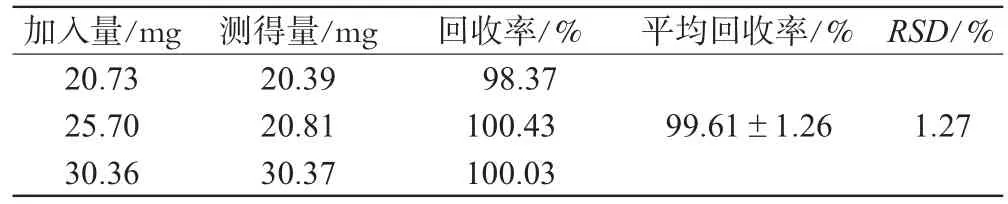
表1 回收率的测定结果Tab 1 Results of recovery tests
2.7 卡托普利片中主药含量测定
选取3个批次的市售卡托普利片,照“2.1.4”项下供试品溶液的方法操作,每个批次平行测定3次,计算其主药标示含量,并与《中国药典》的碘酸钾法[6]进行比较,结果如表2。
3 讨论

表2 卡托普利片中主药含量测定结果Tab 2 Content determination of the main component of Captopril tablets
《中国药典》中[6]采用碘酸钾法测定卡托普利片剂主药含量时,由于其辅料大部分都是淀粉,过滤时不能全部过滤干净或淀粉部分溶于水中使滴定终点提前到达,因此使测定结果很不准确。经验证,采用DNFB作为衍生化试剂与卡托普利反应,使吸收峰波长增至342 nm,且形成的衍生产物很稳定,能更方便地测定卡托普利片剂中主药的含量。本试验结果表明,本方法稳定、可靠,且操作简便、快速,适用于卡托普利片剂中主药的含量测定。
[1]张群艳,李章万,洪 诤,等.衍生化HPLC柱切换法测定人血浆中卡托普利浓度的方法研究[J].药物分析杂志,2001,21(4):273.
[2]Huang TM,He Z,Yang B,et al.Simultaneous determination of captopril and hydrochlorothiazide in human plasma by reverse-phase HPLC from linear gradient elution[J].Journal of Pharmaceutical and Biomedical Analysis,2006,41(2):644.
[3]刘 魁,戎欣玉.衍生化分光光度法测定卡托普利片的含量[J].华西药学杂志,2004,19(1):64.
[4]万绍晖,郝海欧,万绍宇.卡托普利缓释片衍生化紫外分光光度法[J].河南大学学报(医学科学版),2001,20(3):15.
[5]Archontaki HA,Koupparis MA,Efstathiou CE.Semi-automated kinetic determination of phenolic compounds using a fluoride-selective electrode and based on their micellar-catalysed with 1-fluoro-2,4-dinitrobenzene[J].Analyst,1989,114:591.
[6]国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:105.
