15N标记S-苄基-L-半胱氨酸含量及其同位素丰度检测
2010-05-16宋明鸣杜晓宁
宋明鸣,杜晓宁
(上海化工研究院,上海 200062)
S-苄基-L-半胱氨酸(SBC)是巯基保护的氨基酸,是肽类药物谷胱甘肽合成中重要的前体[1]。SBC可通过进一步酯化、Grignard反应制得手性β-氨基醇,用作对潜手性酮进行不对称还原反应的手性配体[2]。15N是氮元素的稳定同位素,作为示踪剂广泛应用于生物化学、医学、药物学、农业科学等领域。15N标记氨基酸和多肽是研究医学和生命科学的重要工具,在蛋白质的人工合成、判定生物活性物质(多肽、蛋白质)的化学结构及药用机理等领域都发挥着独特的示踪作用[3]。天然丰度半胱氨酸类化合物的分析检测主要是采用高效液相色谱法(HPLC),其基本原理是利用该类化合物中的氨基与一系列衍生试剂反应,通过色谱柱分离后进行测定[4]。但该方法分析检测时间过长,不利于对SBC样品合成过程进行实时快速检测。本研究拟对HPLC方法进行改进,建立一种新的简便快捷的检测方法。
1 主要仪器与试剂
2487型高效液相色谱仪:美国Waters公司产品,配备1525型两元梯度泵,2487型紫外可见双波长检测器,Breeze色谱数据工作站;756MC紫外可见分光光度计:上海分析仪器二厂产品;MAT-271气体同位素质谱计:美国Finnigan质谱公司;高温电阻炉(又称马弗炉):上海实验仪器厂;真空转化系统:系统真空度高于10-2Pa,本实验室自制[5]。
SBC标准品:纯度99%,ACROS公司产品;乙腈:色谱纯,上海强顺化学试剂有限公司产品;N,N-二甲基甲酰胺:分析纯,上海凌峰化学试剂有限公司产品;2,4-二硝基氟苯(DNFB)、碳酸氢钠:分析纯,中国医药上海化学试剂有限公司产品;氧化铜、氧化钙、5A分子筛、铜丝均为国产试剂。
2 实验方法
2.1 SBC含量的测定
2.1.1 标准品的配制、衍生及含量测定
准确称取100 mg SBC标准品于100 mL容量瓶中,再加入5 mL 6 mol/L盐酸溶液,用水稀释至刻度,作为储备标准品溶液备用。
移取1 mL配制好的储备标准品溶液至10 mL容量瓶中,再加入2 mL 0.2 mol/L碳酸氢钠溶液和1 mL 1%DNFB乙腈溶液,在60℃水浴中避光反应1 h,冷却至室温,用0.2 mol/L p H 7.0磷酸盐缓冲溶液稀释至刻度,摇匀。以4 000 r/min离心10 min,再用0.45μm滤膜过滤,得到标准品衍生溶液。用HPLC对标准品衍生溶液进行分析。分析条件:色谱柱为Cosmosil C18柱(5μm,150 mm×4.6 mm);流动相A为0.05 mol/L乙酸钠缓冲溶液(pH=6.5,含10 mL/L N,N-二甲基甲酰胺);流动相B为V(乙腈)∶V(水)=3∶1。流动相B的梯度洗脱程序如下:0 min,75%;10 min,40%;13 min,5%;17 min,75%;流动相流速为1.0 mL/min;检测波长为350 nm;柱温为 30℃;进样量为5μL。
2.1.2 样品的衍生及含量测定
移取适量15N标记SBC的发酵液至10 mL容量瓶中,再加入2 mL 0.2 mol/L碳酸氢钠溶液和1 mL 1%DNFB乙腈溶液,60℃水浴中避光反应1 h,冷却至室温,用0.2 mol/L磷酸盐缓冲溶液稀释至刻度,摇匀。以4 000 r/min离心10 min,再用0.45μm滤膜过滤,得到待测样品的衍生溶液。对样品衍生溶液进行HPLC分析。分析条件与2.1.1节相同。
2.2 同位素15N丰度的测定
2.2.1 样品处理
采用微量高温燃烧法[6]转化SBC样品:称取适量SBC标准品,与还原剂氧化铜、吸附剂氧化钙、5A分子筛和铜丝一同加入样品转化管中[7],接入真空转化系统,在真空度高于0.05 Pa时将转化管熔封,放入马弗炉中,高温下反应数小时后取出,自然冷却备用。
2.2.2 样品的测定
用气体同位素MAT-271质谱计测定处理后的样品中15N的丰度。
3 结果与讨论
3.1 SBC含量的测定
3.1.1 分离条件的选择
(1)检测波长。对SBC标准品溶液进行波长全扫描,发现在检测波长为200~400 nm区间内有最大吸收。分别将波长设定为200、250、300、350、400 nm 对样品溶液进行测定,从所得谱图上看,λ=350 nm时,SBC峰强度最大,且其余杂质峰相对较小,对计算结果的干扰最小,故选择350 nm作为检测波长。
(2)流动相 p H。分别配制 p H=6.0、6.2、6.4、6.6、6.8、7.0的流动相进行样品溶液的测定,从谱图上看,p H<6.4时,SBC与其它杂质峰会产生部分重叠,无法实现有效分离,且所有峰的保留时间都较大。pH>6.4时,所有峰的拖尾现象都很严重,不利于组分的定量计算。通过实验,流动相 pH为6.4时,分离效果最佳。pH=6.4时样品的HPLC谱图示于图1。

图1 SBC样品HPLC谱图(p H=6.4)
(3)柱温。分别将柱温设定为 20、25、30、35、40℃,对样品溶液进行 HPLC分析。从HPLC谱图上看,柱温对于SBC峰强度的影响不大;但随着温度的升高,SBC与其他杂质峰的分离度越来越小,不利于分析结果的计算。同时,柱温越低,SBC及其他杂质峰的保留时间越长,分析时间将大幅延长。综合考虑,取柱温为30℃。
3.1.2 标准曲线及检出限
分别配制 0.2、0.4、0.6、0.8、1.0 g/L 的SBC标准工作溶液,按2.1.1节的方法进行HPLC分析,结果示于图2。由图2可以看出,在10 min以内即可检测到SBC的色谱峰,大幅节约了分析时间,有利于实现对反应过程中SBC浓度的实时监控。
以图2中SBC峰的面积(y)对SBC溶液的浓度(x)作图,得到SBC的标准曲线,结果示于图3。对图3进行线性回归分析,其回归方程为y=3×106x-4.16×104,R2=0.998 6。此结果表明,SBC的浓度c在0.2~1.0 g/L范围内与其色谱峰面积A呈良好的线性关系。
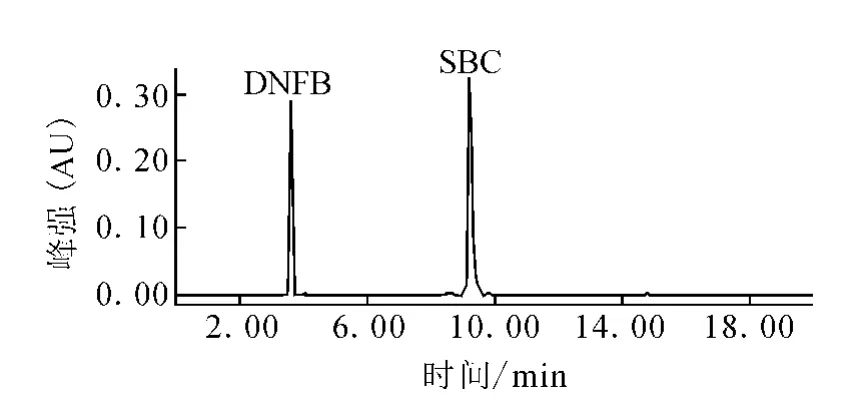
图2 SBC标准品HPLC谱图
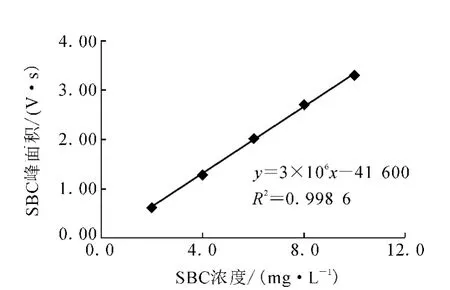
图3 SBC标准曲线
检出限的确定:取SBC标准品溶液适量,采用逐级稀释法,按进样后所得谱图中SBC峰信噪比约为3倍计算,得出该方法对于SBC溶液的检测限为3.95×10-4g/L。
3.1.3 精密度实验
取5μL SBC标准品溶液进行HPLC分析。重复进样6次,所得HPLC谱图中SBC峰面积列于表1。由表1可以看出,测定值的相对标准偏差为0.45%。
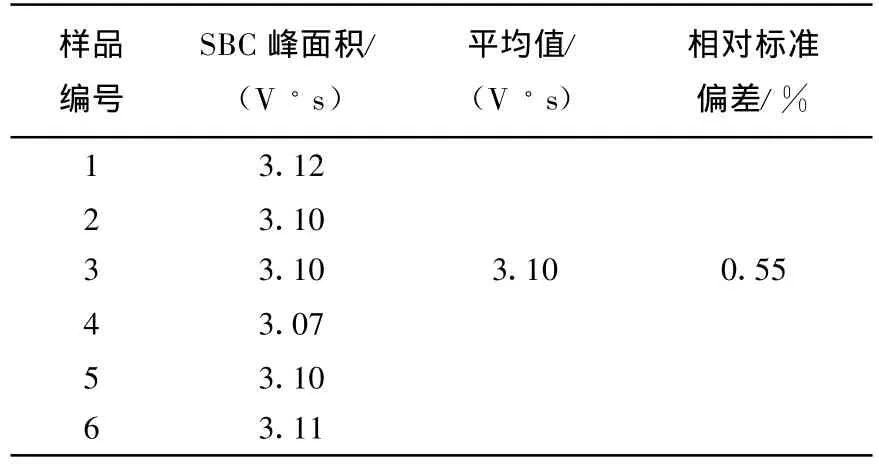
表1 SBC精密度实验结果
3.1.4 加标回收实验
在5批SBC含量为0.141 g/L的发酵液中分别加入等量的约1.0 g/L SBC标准品溶液,按前述方法衍生后进行HPLC分析。加标后SBC理论含量为0.570 g/L,实测含量分别为0.556、0.555、0.553、0.555 、0.554 g/L 。据此计算得加标回收率分别为 97.5%、97.4%、97.0%、97.4%、97.2%,平均回收率为97.3%。
3.1.5 样品中SBC含量测定
按照本实验方法对不同反应时间得到的发酵液中SBC含量进行测定,结果示于图4。从图4可以看出,采用该发酵工艺合成SBC,反应在很短的时间内即可完成。随着反应时间的延长,SBC将继续反应生成其他产物,反而会降低其在发酵液中的含量。因此,采用该路线合成SBC时,建议反应1 h后即可进行目标产物的分离提取。
对于该发酵工艺合成SBC中的其他影响因素(反应温度、投料配比等),采用本实验方法也进行了进一步考察,均取得了满意的结果。说明利用本研究建立的检测方法,可为该发酵工艺合成SBC提供很好的指导作用。
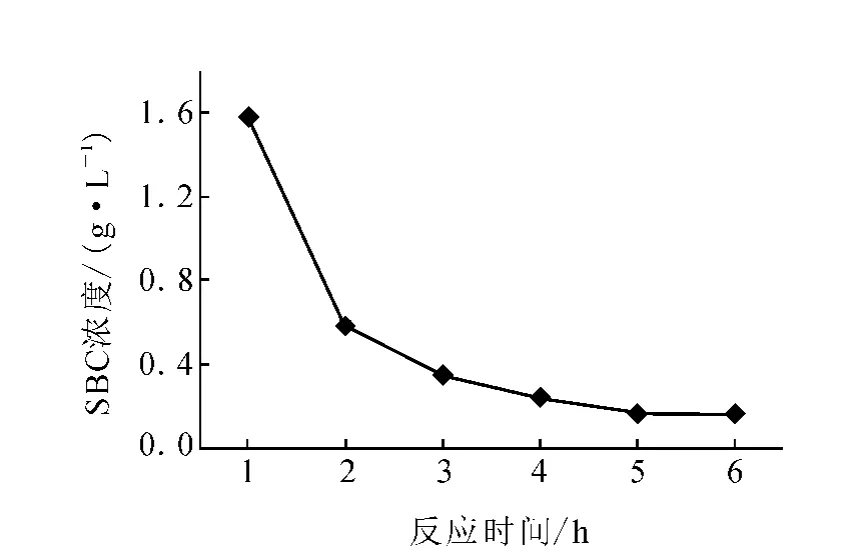
图4 反应时间对SBC含量的影响
3.2 同位素15N丰度的测定
3.2.1 样品的转化处理条件
用高温燃烧法[6,8]处理SBC样品,针对反应温度、反应时间、样品量等做了相关实验,结果显示,SBC样品的转化温度为530℃,反应时间为3 h,称样量2 mg可以满足质谱检测要求。
3.2.2 样品管中杂质气体的影响
SBC属巯基保护的氨基酸,分子中所含的硫在高温燃烧过程中会生成少量的SO2、H2S等杂质气体,这些杂质气体是否会对样品转化产生影响未见相关报道,本实验利用普通SBC试剂对这一因素进行了考察,结果列于表2。由表2可以看出,样品中硫的存在对样品转化和15N丰度测定的精确度不会产生影响。采用微量高温燃烧法转化SBC样品可以满足气体同位素质谱测定15N同位素丰度的要求。
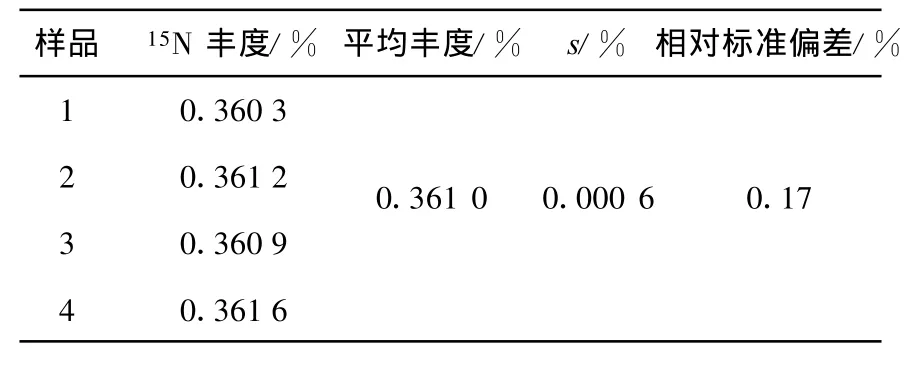
表2 杂质气体对15 N丰度的影响
4 结 论
1)采用本工作建立的HPLC法测定发酵液中SBC的含量,操作简便快捷,准确度及精度高,数据重现性好。
2)采用本测定方法分析发酵液中SBC含量时,检测波长、流动相的pH、柱温等因素均对测定结果的准确性有影响。最佳分析条件为:检测波长350 nm,流动相p H 6.4,柱温 30℃。
3)采用微量高温燃烧法进行样品转化,气体同位素质谱计分析15N标记SBC中15N的同位素。该方法具有测定消耗样品量少,精确度高的优点,对于制备15N标记SBC产品工艺优化具有很好的指导作用。
[1] 孟献梁,荀志金,贺忠,等.硫代苄基半胱氨酸结晶介稳区的测定及分析[J].南京工业大学学报,2003,25(6):66-69.
[2] 陈维一,陆军,蒋虹,等.含硫手性β-氨基醇的合成及其在对映选择还原反应中的应用[J].有机化学,2003,23(12):1 393-1 395.
[3] 柯昌武,罗勇,潘洁,等.酶法拆分氮-15标记S-苄基-半胱氨酸的研究[J].上海化工,2009,34(10):7-11.
[4] 蔡东联,陈小莉.高效液相测定同型半胱氨酸方法的建立[J].氨基酸和生物资源,2001,23(1):48-51.
[5] Smith CS,Chalk PM.Nitrogen gas preparative system for isotope-ratio analysis by mass spectrometry[J].Anal Chem Acta,1979,104:245-252.
[6] 杜晓宁,宋明鸣,赵诚.质谱检测用同位素15N标记样品的处理方法[J].原子能科学技术,2009,43(增刊):59-63.
[7] 杜晓宁,李良君,李虎林,等.HG/T 3789—2005稳定性同位素氖气[S].北京:化学工业出版社,2005.
[8] 杜晓宁,宋明鸣,赵诚,等.13C-尿素同位素丰度的检测方法[J].同位素,2010,23(1):39-43.
