两种皂荚多糖胶流变性质的表征
2010-03-23菅红磊朱莉伟张卫明蒋建新
菅红磊,朱莉伟,张卫明,蒋建新,*
(1.北京林业大学材料科学与技术学院,北京 100083;2.南京野生植物综合利用研究院,江苏 南京 210042)
两种皂荚多糖胶流变性质的表征
菅红磊1,朱莉伟1,张卫明2,蒋建新1,*
(1.北京林业大学材料科学与技术学院,北京 100083;2.南京野生植物综合利用研究院,江苏 南京 210042)
采用Brookfield流变仪研究在不同加热时间、温度、pH值以及盐和糖质量浓度等条件下两种不同形状皂荚豆中多糖胶的流变性质。结果表明:皂荚豆胶是一种假塑性流体,测得的剪切速率和相应的剪切应力的关系符合Power-law模型,圆皂荚豆胶具有较高的黏度,且假塑性明显高于扁皂荚豆胶。在80℃条件下加热1h可使皂荚豆胶完全水合,胶液黏度随温度的上升而下降。在pH2~11范围内,皂荚豆胶比较稳定,但过酸或过碱会导致黏度的下降。皂荚豆胶的黏度随NaCl质量浓度的上升而下降,随白砂糖质量浓度的上升而略微升高。与扁皂荚豆胶相比,NaCl对圆皂荚豆胶的降黏作用较为明显。
皂荚豆胶;黏度;流变性;假塑性
皂荚(Gleditsia sinensis Lam.)为豆科苏木亚科的多年生木本植物,落叶乔木,高可达30m,胸径达1.2m;树皮暗灰或灰黑色,粗糙;刺常分枝,基部粗圆。种子多为长圆形,荚果扁平,长约12~30cm,宽约2~4cm,荚果微厚,高棕色且表面被白色粉霜[1]。皂荚花期4~5月,果期10月[2]。木材黄褐色,有光泽,可供室内装修、细木工、旋制品及工艺品等用材;荚果煎汁可以代替肥皂;荚瓣、种子入药,祛痰通窍;枝刺可作药用,能消肿排脓、杀虫、治癣。皂荚树的分布地域跨温带与亚热带,平原、丘陵和山区都能生长,具有复杂的多种多样的生态属性,遗传多样性程度高[3],在我国河北、山东、山西、江苏、浙江、江西、福建、广东、四川、贵州、云南等地均有分布。皂荚树根系发达,具有耐旱、节水、耐寒、固氮和抗病虫害等优点,是营造水土保持林和防风固沙林的优良生态树种之一。皂荚豆胶(Gleditsia sinensis gum),又名皂荚糖胶、皂角子胶,是从豆科(Leguminosae)多年生植物皂荚种子胚乳中分离提取得到的多糖胶,其主要成分为半乳甘露聚糖[4]。半乳甘露聚糖是以β-D-(1→4)苷键连接的D-甘露聚糖为主链,在某些D-甘露糖基的O-6位上连接有单个的α-D-半乳糖[5-7]。皂荚豆胶具有与瓜尔胶、胡芦巴胶等植物多糖胶相似的性质,可
作为增稠剂、黏合剂、稳定剂等应用于食品、石油、造纸、印染和选矿等多种工业中。
根据种子形状,皂荚豆可以普遍分为圆形和扁形两种。对于不同形状的皂荚豆中多糖胶流变性质的研究,未曾见有相关报道。虽然目前国内已有一些皂荚豆胶流变性质的研究[8-10],但是所用黏度计大多为NDJ-1型旋转黏度计,需要手动采集数据,人为误差大,数据的重现性不理想。美国Brookfield公司的旋转黏度计和流变仪是黏度测定的世界标准,因此应用Brookfield流变仪对皂荚豆胶的流变性质进行综合表征与其他多糖胶,如已经充分研究的瓜尔胶和刺槐豆胶,具有更好的可比性。
1 材料与方法
1.1 材料与仪器
皂荚荚果,河北涉县供销社提供,自然晾干,经手工剥离获得皂荚种子。种子按照外形分为扁皂荚种子和圆皂荚种子。
79-2磁力加热搅拌器、国华2004-211(601)超级恒温水浴 常州国华电器有限公司;FA1004分析天平、雷磁PHS-25数显pH计 上海精密科学仪器有限公司;LVDV-Ⅲ Ultra型流变仪(配有小量样品适配器,SC4-31号转子) 美国Brookfield公司。
1.2 物理参数的测定与胶粉的制备
采用4分法选取30个皂荚荚果,测定其外形参数、荚果籽粒数和荚果质量。采用4分法选取30粒种子,测定其外形参数和千粒质量。
种子采用烘炒法[11]去壳后,分离得到胚乳片,粉碎过120目筛分别获得扁皂荚豆胶粉和圆皂荚豆胶粉。皂荚胶粉在空气中经水分平衡后,在105℃条件下测定胶粉的水分含量。
1.3 流变性质的测定
所有胶液的配制均是以干质量为基准称取胶粉,用2%(占胶液的体积分数)的无水乙醇打湿胶粉,加入去离子水。在磁力搅拌器上搅拌15min,于80℃条件下加热1h使胶液达到充分水合,自然冷却至室温后,在25℃测定加热时间、温度和pH值等对皂荚豆胶溶液流变性质的影响。
1.3.1 恒温加热时间对皂荚豆胶溶液黏度的影响
配制0.05g/L皂荚豆胶溶液,分别在80℃条件下加热0.5、1、1.5、2、2.5h,自然冷却至室温后,在25℃条件下测定黏度随加热时间的变化。
1.3.2 温度对皂荚豆胶溶液黏度的影响
配制0.05g/L的皂荚豆胶溶液,经充分水合后,在25~85℃范围内,以1℃/min的升温速率进行温度与黏度的关联性测定。
1.3.3 pH值对皂荚豆胶溶液黏度的影响
配制0.05g/L的皂荚豆胶溶液,经充分水合后,分别用稀酸(HCl溶液)和稀碱(NaOH溶液)调节其pH值,在25℃条件下测定pH值变化对黏度的影响。
1.3.4 剪切速率对皂荚豆胶溶液黏度的影响
取0.05g/L皂荚豆胶溶液分别在25℃和80℃条件下水合1h后,自然冷却至室温后,25℃时Rheocalc V3.2软件控制剪切速率由0s-1升至85s-1,测得黏度和剪切应力随剪切速率的变化曲线。
1.3.5 盐和糖对皂荚豆胶溶液黏度的影响
配制两份0.05g/L的皂荚豆胶溶液,经充分水合后,1份加入NaCl,充分搅拌混匀,于25℃测定含0.1、0.5、1g/L NaCl的胶液黏度的变化;另外1份加入白砂糖,充分搅拌混匀,25℃条件下测定含0.1、0.5、1g/L白砂糖的胶液黏度的变化。
2 结果与分析
2.1 物理参数

表1 皂荚荚果与种子的物理参数Table 1 Physical parameters of Gleditsia sinensis pods and seeds
从表1可以看出,扁皂荚荚果的宽度比较大,而长度较小,具有较高的荚果单质量。扁皂荚种子的得率较低,仅为17%,而圆皂荚种子得率为24%。两类种子的千粒质量相接近。扁皂荚豆胶和圆皂荚豆胶的水分含量分别为8.2%和8.0%。
2.2 皂荚豆胶的流变性质
2.2.1 恒温加热时间对皂荚豆胶溶液表观黏度的影响

图1 80℃加热时间对皂荚豆胶溶液表观黏度的影响Fig.1 Effect of heating time at 80 ℃ on the viscosity of Gleditsia sinensis gum solutions
由图1可知,在80℃恒温加热条件下,随着加热时间的延长,皂荚豆胶的表观黏度逐渐上升,加热1h可使表观黏度达到最大值,但是当加热时间大于1h后,表观黏度则出现下降。这是由于加热可以提高皂荚豆胶的水合速率,使表观黏度迅速升高。但是,长时间的高温加热会使溶液中的半乳甘露聚糖分子发生少量降解,多糖分子链变短,导致溶液的表观黏度降低。
2.2.2 温度对皂荚豆胶溶液表观黏度的影响
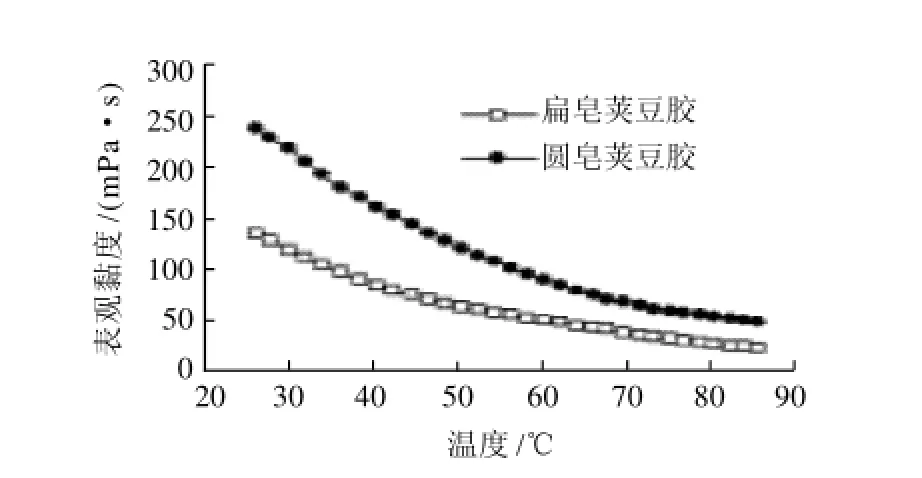
图2 温度对皂荚豆胶溶液表观黏度的影响Fig.2 Effect of temperature on the viscosity of Gleditsia sinensis gum solutions
由图2可知,充分水合的皂荚豆胶的表观黏度随温度的升高而呈下降趋势。在温度由25℃升至85℃的过程中,扁皂荚豆胶和圆皂荚豆胶的表观黏度分别下降了83%和79%。溶液温度升高导致分子热运动加剧,从而削弱了胶体大分子间的缠结,另外,加热可导致分子链间和链内氢键的断裂,使表观黏度下降[12]。
2.2.3 pH值对皂荚豆胶溶液表观黏度的影响
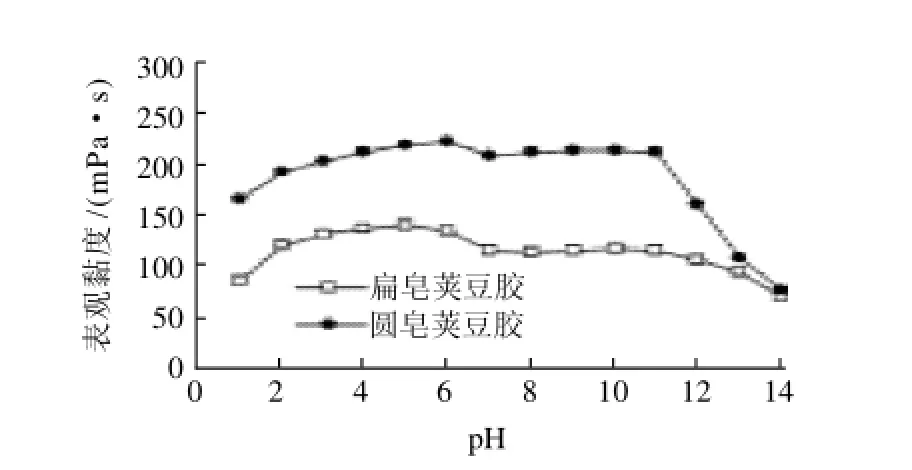
图3 pH值对皂荚豆胶溶液表观黏度的影响Fig.3 Effect of pH value on the viscosity of Gleditsia sinensis gum solutions
由图3可知,在pH1~14范围内,圆皂荚豆胶的表观黏度明显高于扁皂荚豆胶,两种豆胶的表观黏度随pH值的变化趋势基本一致。在酸性溶液中,溶液表观黏度随pH值上升而逐渐升高,表观黏度达到最大值后出现下降。扁皂荚豆胶的最大表观黏度值(140mPa·s)出现在pH5时,而圆皂荚豆胶的最大表观黏度值(223mPa·s)出现在pH6处。在碱性溶液中,pH7~11范围内扁皂荚豆胶和圆皂荚豆胶的表观黏度值基本恒定,当pH>11时两种胶的表观黏度值均出现剧烈下降,圆皂荚豆胶表观黏度的下降程度明显大于扁皂荚豆胶。总的来说,在pH2~11范围内,表观黏度的变化不大,即皂荚豆胶在酸性溶液和碱性溶液中比较稳定。
随着溶液pH值减小,即酸性增大时,溶液表观黏度变小。这是由于在溶液中,半乳甘露聚糖大分子呈无规线团状,彼此交叠、缠结在一起,过量的酸根离子起到了静电屏蔽作用而使单个高分子无规线团紧缩[13],结果减弱了缠结程度,表观黏度因而变小。碱性条件下,随着溶液pH值增加Na+浓度逐渐上升,可以推测Na+的加入与多糖分子上的羟基反应生成钠盐,可能会阻碍分子间缔合氢键的形成,造成表观黏度的下降[14]。此外,半乳甘露聚糖大分子链上的苷键在过酸和过碱条件下会发生水解反应而使大分子降解,使表观黏度下降[15-16]。
2.2.4 剪切速率对皂荚豆胶溶液表观黏度的影响

图4 剪切速率对不同水合温度的皂荚豆胶溶液剪切应力(a)和表观黏度(b)的影响Fig.4 Effect of shear rate on the shear stress (a) and viscosity (b) of Gleditsia sinensis gum solutions at different hydration temperatures
图4 为分别在25℃和80℃条件下水合1h后的皂荚豆胶溶液的流动曲线。Ostwald和de Waele提出的Powerlaw模型[17-19]为:

式中:τ为剪切应力/Pa;D为剪切速率/s-1;k为稠度指数/(Pa·sn);n为流动指数,无量纲。稠度系数k为流体在1s-1流速梯度下的表观黏度。k值越大,表观黏度越大。流动指数n表示流体在一定流速范围内的非牛顿性程度。n=1时,牛顿性流体,溶液的表观
黏度不依赖于剪切速率的变化;n<1时,假塑性流体,随剪切速率增加而变稀(剪切稀释特性);n>1时,膨胀性流体,随剪切速率增加而变稠。

表2 皂荚豆胶的流变参数Table 2 Rheological parameters of Gleditsia sinensis gum solutions
应用Power-law模型计算得到的参数k和n以及在5s-1和85s-1剪切速率下的表观黏度列于表2中。由图4和表2可知,扁皂荚豆胶和圆皂荚豆胶溶液均为假塑性流体,即溶液表观黏度随剪切速率的增加而降低(剪切稀释)。这一现象主要是由于当剪切速率增加时,溶液中的半乳甘露聚糖大分子容易在剪切作用下定向并使缠结减弱,导致表观黏度的降低[20]。速度梯度越大,定向作用越强,定向使分子与流动方向趋于一致,使大分子间的缠结减弱[13],因此,溶液的表观黏度随着剪切速率的增加而下降。水合温度为80℃的皂荚豆胶溶液的假塑性明显高于25℃的,这说明加热可以在很大程度上促进水合速率的提高。
低剪切速率下的表观黏度值可用于反映产品在口中的质感,而高剪切速率下的表观黏度值则反映产品在加工过程中的性能[21]。80℃水合的扁皂荚豆胶和圆皂荚豆胶在5s-1条件下的表观黏度分别为118mPa·s和240mPa·s,而在85s-1条件下的表观黏度分别为69mPa·s和121mPa·s。
2.2.5 盐和糖对皂荚豆胶溶液表观黏度的影响
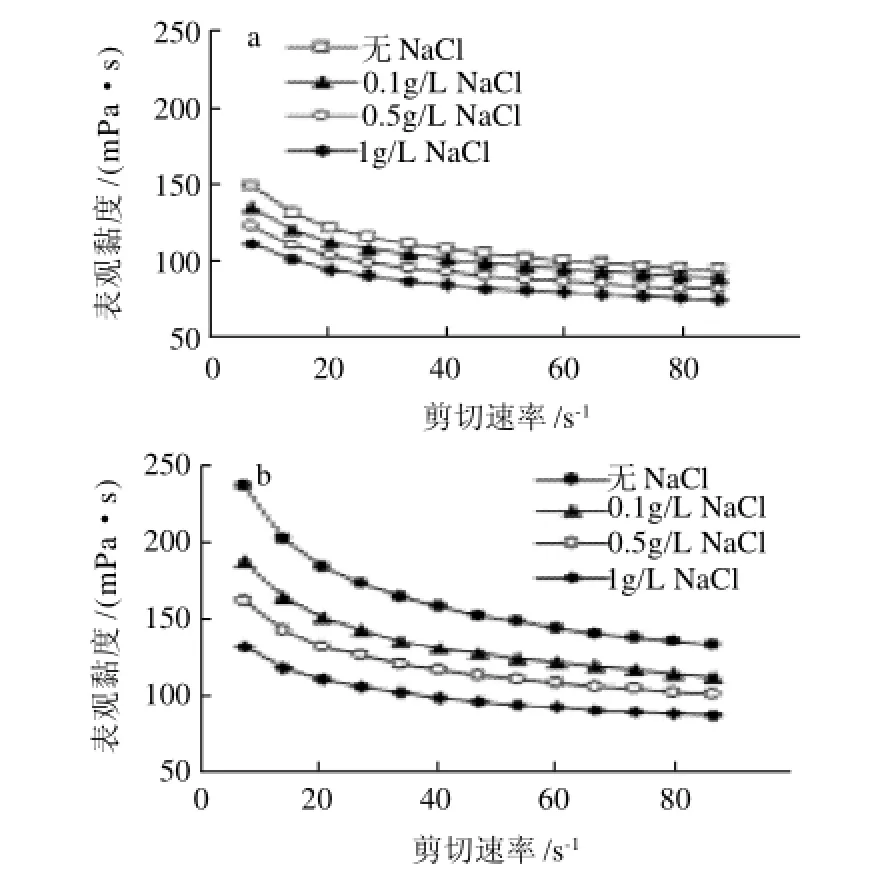
图5 NaCl对扁皂荚豆胶(a)和圆皂荚豆胶(b)溶液表观黏度的影响Fig.5 Effect of NaCl on the viscosity of Gleditsia sinensis gum solutions
由图5可知,随NaCl质量浓度的上升,溶液表观黏度逐渐下降,并且NaCl对圆皂荚豆胶溶液表观黏度的影响程度要明显大于扁皂荚豆胶。圆皂荚豆胶溶液的假塑性随NaCl质量浓度的上升而逐渐降低。当NaCl质量浓度为1g/L时,圆皂荚豆胶溶液的流动指数为0.84,稠度指数为0.18Pa·sn。可以推测Na+的加入与多糖分子上的羟基反应生成钠盐,可能会阻碍分子间缔合氢键的形成,造成表观黏度的下降[14]。
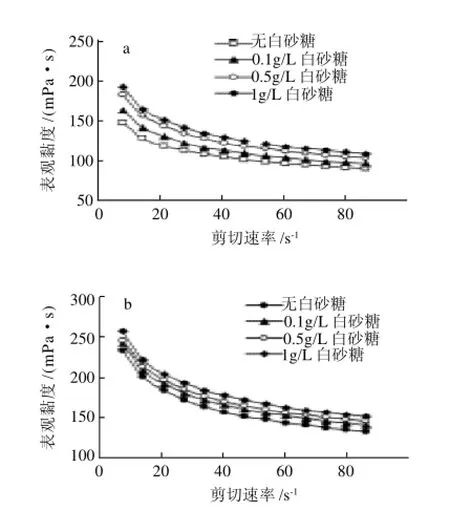
图6 白砂糖对扁皂荚豆胶(a)和圆皂荚豆胶(b)溶液表观黏度的影响Fig.6 Effect of white sugar on the viscosity of Gleditsia sinensis gum solutions
由图6可以看出,扁皂荚豆胶和圆皂荚豆胶溶液的表观黏度随白砂糖质量浓度的增加而上升,但是白砂糖的增黏效果都不明显。白砂糖的增黏作用可能是因为糖是强亲水性物质,糖的加入可以增强半乳甘露聚糖大分子间的相互作用(氢键),使表观黏度增加。
3 结 论
扁皂荚豆胶和圆皂荚豆胶溶液,随着剪切速率的增大,表观黏度减小。两种流体均表现为假塑性,其流变特性可用Power-law模型表示。在相同条件下,圆皂荚豆胶溶液的假塑性明显高于扁皂荚豆胶溶液。圆皂荚豆胶的表观黏度明显高于扁皂荚豆胶。两种皂荚豆胶溶液经充分水合后,表观黏度随温度的升高而下降。总体而言,pH值对皂荚豆胶溶液的表观黏度影响很小,但是过酸或过碱条件会破坏多糖的糖苷键连接导致溶液表观黏度急剧下降。由于Na+会阻碍分子键氢键的形成,NaCl对皂荚豆胶溶液有降黏作用,且对圆皂荚豆胶溶液的影响较为明显。而白砂糖有利于半乳甘露聚糖
大分子间形成氢键,因此对皂荚豆胶溶液有低幅度的增黏作用。
[1] 胡国华. 功能性食品胶[M]. 北京: 化学工业出版社, 2003: 74-77.
[2] 中国科学院植物研究所. 中国高等植物图鉴赏: 第二册[M]. 北京: 科学出版社, 1980: 7.
[3] 邵金良, 袁唯, 董文明, 等. 皂荚的功能成分及其综合利用[J]. 中国食物与营养, 2005(4): 23-25.
[4] 张广伦, 肖正春. 半乳甘露聚糖胶的研究、生产和应用[J]. 中国野生植物资源, 1990(2): 1-5.
[5] 蒋建新, 朱莉伟, 安鑫南, 等. NMR法研究我国主要植物胶资源的多糖化学结构[J]. 林产化学与工业, 2006, 26(1): 41-44.
[6] SINGH V, SETHI R, TIWARI A. Structure elucidation and properties of a non-ionic galactomannan derived from the Cassia pleurocarpa seeds[J]. International Journal of Biological Macromolecules, 2009, 44(1): 9-13.
[7] TAMAKI Y, TETUYA T, TAKO M. The chemical structure of galactomannan isolated from seeds of Delonix regia[J]. Bioscience Biotechnology and Biochemistry, 2010, 74(5): 1110-1112.
[8] 杨永利, 张继, 姚健, 等. 皂荚豆胶冷水溶部分和热水溶部分的流变性研究[J]. 食品科学, 2002, 23(8): 56-59.
[9] 蒋建新, 安鑫南, 朱莉伟, 等. 皂荚豆组成及皂荚胶的流变性质[J].南京林业大学学报: 自然科学版, 2003, 27(1): 11-15.
[10] 蒋建新, 朱莉伟, 安鑫南, 等. 植物多糖胶流变性质的研究[J]. 中国野生植物资源, 2003, 22(5): 29-33.
[11] 蒋建新, 张卫明, 朱莉伟, 等. 烘炒法分离提取半乳甘露聚糖型种子胶[J]. 中国野生植物资源, 2003, 22(5): 34-36.
[12] RINAUDO M, MORONI A. Rheological behavior of binary and ternary mixtures of polysaccharides in aqueous medium[J]. Food Hydrocolloids, 2009, 23(7): 1720-1728.
[13] 王伟, 徐德时, 李素清, 等. 聚电解质: 壳聚糖浓溶液流变学性质研究: 浓度、温度、溶剂pH值和外加盐对黏度及流动性的影响[J].高分子学报, 1994(3): 328-333.
[14] 李少霞, 赵谋明, 徐建祥, 等. 常用食品胶耐盐性的研究[J]. 食品科学, 1999, 20(3): 11-15.
[15] 汤凤霞, 王忠敏. 葫芦巴胶溶液流变特性研究[J]. 食品科学, 2004, 25(5): 46-52.
[16] KOK M S. Rheological study of galactomannan depolymerisation at elevated temperatures: Effect of varying pH and addition of antioxidants [J]. Carbohydrate Polymers, 2010, 81(3): 567-571.
[17] OSTWALD W. About the rate function of the viscosity of dispersed systems[J]. KOLLOID-Z, 1925, 36: 99-117.
[18] ANDERTOVA J, RIEGAR F. Rheometry of concentrated ceramic suspensions-steps from measured to relevant data. Part 3: rotational viscometer with parallel plates, power-law model[J]. Ceramics-Silikaty, 2009, 53(4): 283-286.
[19] BANDULASENA H C H, ZIMMERMAN W B, REES J M. An inverse methodology for the rheology of a power-law non-Newtonian fluid[J]. Journal of Mechanical Engineering Science, 2008, 222(5): 761-768.
[20] YOO D, KIM C, YOO B. Steady and dynamic shear rheology of rice starch-galactomannan mixtures[J]. Starch-Starke, 2005, 57(7): 310-318.
[21] SMITH C H, LOGEMANN J A, BURGHARDT W R, et al. Oral and oropharyngeal perceptions of fluid viscosity across the age span[J]. Dysphagia, 2006, 21(4): 209-217.
Rheological Characteristics of Gums from Gleditsia sinensis Lam. Seeds with different Shapes
JIAN Hong-lei1,ZHU Li-wei1,ZHANG Wei-ming2,JIANG Jian-xin1,*
(1. College of Materials Science and Technology, Beijing Forestry University, Beijing 100083, China;2. Nanjing Institute for Comprehensive Utilization of Wild Plants, Nanjing 210042, China)
The rheological properties of gums from Gleditsia sinensis Lam. seeds with different shapes were studied with Brookfield rheometer, at different levels of heating time, temperature, pH and salt (NaCl) and white sugar concentrations. The results showed that both the Gleditsia sinensis gums were a type of pseudoplastic fluid and the relationship between the detected shear rate and shear stress accorded with the Power-law model. The gum from round seeds was more viscous than that from flat seeds. It was found that the two gums achieved complete hydration by heating at 80 ℃ for 1 h. The viscosity of the fully hydrated gum solution decreased with increasing temperature. The Gleditsia sinensis gum solution was stable with pH values varying from 2 to 11. The viscosity of the gum solution decreased with increasing salt concentration, while slightly increased with increasing white sugar concentration. Salt had more obvious effect on the viscosity of round seed gum than that of flat seed gum.
Gleditsia sinensis gum;viscosity;rheological properties;pseudoplastic
TS201.7
A
1002-6630(2010)17-0068-05
2010-04-28
国家自然科学基金项目(30771685);“十一五”国家科技支撑计划项目(2006BAD06B05)
菅红磊(1985—),女,硕士研究生,研究方向为植物多糖。E-mail:jianhonglei@163.com
*通信作者:蒋建新(1969—),男,教授,博士,研究方向为林产化工及生物质能源。E-mail:jiangjx@bjfu.edu.cn
