沉淀法检测水泥三氧化硫
2010-02-23刘吉贵深圳市建筑科学研究院广东深圳518049
刘吉贵(深圳市建筑科学研究院,广东 深圳518049)
1 前言
水泥中的三氧化硫(硫酸盐)含量是评定水泥品质的重要指标和产品检测的必要项目。水泥中的三氧化硫主要是水泥生产中为了调节其凝结时间而掺加石膏带入的,或者是煅烧熟料时掺加矿化物或由原燃材料带入的。适量的硫酸盐能改善水泥性能,如提高水泥强度,降低收缩性,改善抗冻、抗渗和耐腐蚀性等;还对改善易烧性、促进硅酸三钙矿物的形成及提高水泥强度等有显著作用。但如果水泥中的硫酸盐含量过高,易在水泥硬化后继续与水和铝酸三钙反应形成钙矾石,产生体积膨胀。所以,在水泥生产过程中要严格控制三氧化硫的含量。
2 检测方法
2.1 方法提要
在酸性溶液中,用氯化钡溶液沉淀硫酸盐,经过滤灼烧后以硫酸钡形式称量。测定结果以三氧化硫计。
2.2 主要试剂
盐酸溶液:1:1(体积比)
氯化钡溶液:100g/L
硝酸银溶液:5g/L
2.3 分析步骤
称取约0.5g试样m1,精确到0.0001g,置于200ml烧杯中,加入约40ml水,搅拌使试样完全分散,在搅拌下加入10mL盐酸(1+1),用平头玻璃棒压碎块状物,加热煮沸并保持微沸(5±0.5)min。用中速滤纸过滤,用热水洗涤10~12次,滤液及洗液收集于400mL烧杯中。加水稀释至约250mL,玻璃棒底部压一小片定量滤纸,盖上表面皿,加热煮沸,在微沸下从杯口缓慢滴加10mL热的氯化钡溶液,继续微沸3min以上使沉淀良好的形成,然后在常温下静止12~24h或温热处静置至少4h,此时溶液体积应保持在约200mL。用慢速定量滤纸过滤,以温水洗涤,直至检验无氯离子为止。
将沉淀及滤纸一并移入已灼烧恒量的瓷坩埚中,灰化完全后,放入800℃~900℃的高温炉内灼烧30min,取出坩埚,置于干燥器中冷却至室温,称量沉淀质量m2。反复灼烧,直至恒量。
2.4 结果结算
试样中三氧化硫的质量分数
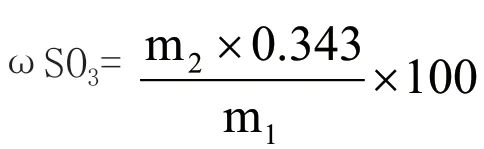
式中:
ωSO3—三氧化硫的质量分数,%;
m1—试料的质量,单位g;
m2—灼烧后沉淀的质量,单位g;
0.343—硫酸钡对三氧化硫的换算系数。[1]
3 试验步骤解析及注意事项
3.1 称样
称取水泥试样前应将试样搅拌,采用四分法或缩分器将试样缩分至100g,经80μm方孔筛,充分混匀,装入试样瓶中,密封保存,使得所取试样有代表性。[1]
3.2 样品分散及酸溶解
称取样品应置于干燥烧杯中,加入40ml水后要充分搅拌,使样品充分分散,避免样品结块,影响下一步的样品溶解,注意加入盐酸要边加入边搅拌,用玻璃棒压碎块状物,煮沸5min使其充分溶解。此处加入的盐酸一部分起到溶解样品的作用,过量的酸在下一步的沉淀过程中会使溶液产生稀酸的环境,稀酸的环境能提高硫酸钡沉淀的溶解度,有利于得到较大晶粒的沉淀。
3.3 第一次过滤
选用中速滤纸进行过滤,漏斗应选用直径60~70mm、径长150mm左右、角度为60°容易做成水柱和流速较快的长颈漏斗。折叠滤纸及过滤过程要注意不要将滤纸弄破,以免发生漏滤现象,滤纸和漏斗壁之间尽量不要有气泡存在,使滤纸紧贴漏斗壁上,如果有气泡存在可用手指轻轻排除,将水加到漏斗中,漏斗径内应全部充满水而形成水柱,以加快过滤速度,过滤时玻璃棒应轻触滤纸的三层处,洗涤时要用热水洗涤多次,使有效成分充分过滤。
3.4 试样沉淀及陈化
沉淀法检测方法本身的特点要求生成的沉淀物晶粒要足够大,以保证能在过滤的时候尽可能多的留在滤纸上,硫酸钡属于晶型沉淀,为了得到相对大的晶粒,必须减小沉淀开始时溶液中硫酸钡的相对过饱和度,使沉淀剂与溶液中SO42-相遇的瞬间,生成较少的晶核,然后渐渐增大成为较大的晶粒。如果相对过饱,瞬间生成很多晶核,在此后加入沉淀剂时,各晶粒竞相生长,必然得到极多的极细小的晶粒,甚至成为无定形沉淀,将很难过滤和洗涤,检验结果会有很大误差。要取得理想的晶形沉淀,必须满足以下沉淀条件:
在稀溶液中进行沉淀。试验溶液及沉淀剂溶液均应为适当的稀溶液,以减小沉淀反应开始时溶液中硫酸钡的相对过饱和度。生成较大的晶粒,易滤易洗,同时可以减少共沉淀,有利于得到纯净的沉淀。本试验中0.5g 试样最后制成约200ml溶液,沉淀剂为10% 氯化钡溶液。但溶液也不能过稀,以免BaSO4沉淀溶解损失增大,实验证明溶液体积为200~250ml时沉淀比较理想。
在热溶液中进行沉淀。试验溶液应在微沸条件下用氯化钡溶液进行沉淀。因为热溶液中沉淀的溶解度增大,可使溶液的过饱和度降低,从而使晶核生成较少,同时,高温可以增加离子的扩散速度,加快沉淀晶粒的生长,有利于获得较大晶粒的沉淀。另外在较高的温度下,沉淀吸附杂质的量也较少,有利于晶粒的净化。
在不断搅拌下慢慢滴加沉淀剂。可用滴管吸取后慢慢加入热溶液中,切不可将10mlBaCL2溶液一次性全倒入试验溶液中。不断搅拌下慢慢滴加沉淀剂可避免溶液局部形成过饱和溶液,瞬间生成过多的晶核。
沉淀生成以后,将沉淀连同溶液一起在温热处放置4h 以上或过夜,即所谓陈化过程,陈化可使小晶粒沉淀逐渐溶解,大晶粒不断长大。因为小晶粒的溶解度比大晶粒大,在同一溶液中,对大晶粒为饱和溶液时,对小晶粒则为未饱和溶液。因此,小晶粒就要溶解,溶解到一定程度时,溶液对小晶粒为饱和溶液,对大晶粒则为过饱和溶液,沉淀就在大晶粒上析出,直至饱和为止。此时溶液对小晶粒又不饱和了,于是小晶粒继续溶解。如此反复进行,小晶粒逐渐消失,大晶粒不断长大。大晶粒长大的同时,沉淀总表面积变小,吸附杂质的量就变小,因而还能提高沉淀的纯度。温热的条件可加速陈化作用,缩短陈化时间[2] [3]。
3.5 第二次过滤及沉淀洗涤
硫酸钡沉淀属于细晶型沉淀,过滤时应采用慢速滤纸,为防止沉淀漏滤,最好采用双层慢速滤纸过滤,但因GB/T 176中规定采用单层滤纸,因此为了保证检测结果的可比性,正常的检测活动中还应采用单层滤纸过滤。
从烧杯往滤纸上转移沉淀时一定要转移干净,若有沉淀吸附在烧杯上不易转移,可用带乳胶头的玻璃棒擦洗烧杯后再转移。
用温水洗涤沉淀时,应坚持“少量多次”的原则,既不能洗涤次数不够,又不能过量洗涤。若洗涤次数过少,则会因沉淀洗不干净而使分析结果偏高;反之,若过量洗涤,则有部分BaSO4沉淀溶解致使分析结果偏低。一般洗涤7 ~8 次即可,每次洗涤量以10 ml左右为宜。通过用硝酸银溶液检验滤液中有无氯离子判定沉淀是否洗涤干净。
3.6 沉淀灰化及灼烧
将沉淀连同滤纸转入已恒重的坩埚内,斜盖上坩埚盖,置于电炉上,先在低温下烘干水分,待滤纸干燥后再提高温度灰化,使滤纸灰化完全。灰化时特别注意不要使滤纸着火,否则会因气流的强烈流动使沉淀飞失。如已着火,应立即切断电炉电源,并将坩埚盖盖上,让其自行熄灭后再继续灰化,切忌用嘴吹灭火焰,以防沉淀飞失。另外,灰化温度不可过高,如果灰化温度过高,部分BaSO4沉淀有可能会被碳化的滤纸还原成BaS,而使分析结果偏低。反应式如下[2][3]:
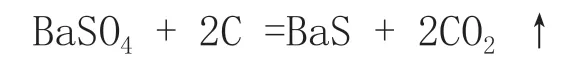
沉淀灰化后应放入800~900℃高温炉内进行灼烧。沉淀灼烧好后,将坩埚取出放在石棉板或耐火瓷板上,在空气中稍冷后再放入干燥器中,此时坩埚还有一定的温度,为避免干燥器中的空气从高温降到室温后压力大大降低,盖子很难打开,因此先盖上盖子,再慢慢推开盖子,放出热空气。这样重复数次,直到听不到“嘣”“嘣”的声音后,把盖子盖紧并移至天平室,冷却至室温后称量。恒量空坩埚和恒量沉淀时,灼烧温度、放置时间等条件应保持一致,在保证试样已冷却到室温前提下,放置时间应尽可能短[4]。
[1]王瑞海等.GB/T.176-2008.水泥化学分析方法【S】21-22
[2]丁美荣等.水泥质量及化验技术【M】.北京.中国建材工业出版社,1992.
[3]刘珍等.化验员读本上册化学分析(第二版)【M】.北京.化学工业出版社,1994:
[4]刘吉贵.影响水泥烧失量检测结果的因素分析【J】.科技创新导报2009,(29):169-170.
