γ-Al2O3表面吸附SO2、NOx的机理分析
2010-01-29郭大为
郭大为
(中国石化石油化工科学研究院,北京100083)
SO2、NOx(NO2及 NO)是催化裂化再生烟气中大气污染源的主要组分。目前,控制催化裂化工艺中SO2和NOx排放的途径有3类:原料油加氢脱硫脱氮;使用硫/氮转移剂;烟气脱硫脱氮。前两类或者受到氢源和投资费用的限制,或者由于脱除率的限制而影响了使用;第3类方法则具有脱除效率高、适用范围广等优点,越来越得到重视。
在烟气脱硫脱氮方法中,对比单独脱除过程,联合脱硫脱氮工艺成为目前的发展方向。在联合脱硫脱氮过程中,与湿法和半湿法相比,干法过程因其过程简单、操作便捷而越来越受到欢迎。目前已经在催化裂化再生烟气处理中使用的干法联合脱硫脱氮工艺是基于移动床的以活性炭为吸附剂的Mitsui-BF(Berbau-Forschung)工艺[1]。但该过程使用氨为还原剂,容易出现二次污染物。本着环境友好、不引入二次污染物的理念,丹麦的科学家开发了 SNAP(SO2-NOxadsorption process)技术[2-3]。此技术以经过碱金属改性的γ-Al2O3为吸附剂,采用稀相流化床吸附-再生工艺。他们与比利时的研究者合作,在微反试验装置及中型试验装置上确定了较为系统的吸附反应动力学模型[3-4]。李平等[5-7]采用原位分析手段对γ-Al2O3吸附NO和SO2的机理进行了分析。
另一方面,Al2O3由于其良好的机械性能和热稳定性,尤其是卓越的酸-碱特性,在炼油工业中被广泛用作催化剂或催化剂载体,因而越来越得到研究者们的注意。在实验方面,人们从具有类尖晶石结构的γ-Al2O3的晶体结构出发,提出了其(100)面和(110)面为活性晶面的假设,并利用探针分子,如H2O、H2、O2、CO、CO2和 H2S等,考察了γ-Al2O3晶体表面的反应性能。在理论计算方面,人们采用分子动力学(MD)方法、周期边界性的从头算及平面波密度泛函等量子化学方法研究了γ-Al2O3的表面和本体,以及 γ-Al2O3与诸如 H2O、H2S、CH3OH、MoS2、(Re)2(CO)10等小分子的反应性能[8]。
笔者利用密度泛函方法着重考察γ-Al2O3的(100)面中的酸性八面体Al位相对SO2、NOx(NO2及NO)的吸附趋势,结合实验分析γ-Al2O3对 SO2和NOx的吸附机理。
1 计算方法与实验方法
1.1 模型与计算方法
含Al、Mg、O的尖晶石晶体,其空间群为立方晶系的 Fd-3m,晶胞参数为 a=b=c=0.8144 nm[9]。以此为出发点,将晶体中的Mg置换为Al。理想的尖晶石晶胞含56个原子(32个 O和24 Al,其中16个Al处于八面体位,8个 Al处于四面体位)。为满足γ-Al2O3的化学计量数,调整部分 Al原子位的占有率,使得晶体中的氧为32个,铝为,阳离子空位为。以此为输入构象,采用 GULP程序包[10]进行构象优化。GULP所用的经验力场是由Bush等导出的壳层模型力场[11]。优化后的结果是 a=b=c=0.8042 nm,与初始构象相比晶胞有所收缩,偏差为5.17%。考虑到晶体中Mg、Al间的替代以及阳离子空位的存在,晶胞收缩现象是合理的。所得晶体模型如图1所示。

图1 采用 GULP构象优化得到的γ-Al2O3的晶体结构模型Fig.1 Crystal structure model ofγ-Al2O3optimized by GULP

图2 γ-Al2O3晶体的(100)和(110)晶面模型Fig.2 Surface(100)and(110)models ofγ-Al2O3crystal(a)Periodic slab of(100);(b)Cluster of(100); (c)Periodic slab of(110);(d)Cluster of(110)Dark ball and light ball represent O and Al,respectively,in (a)and(c);grey ball and red ball represent Al and O, respectively,in(b)and(d)
从优化后的γ-Al2O3晶体切割出(100)面,做成5层簇模型,其中含20个重原子(12个 O,8个Al);切割出(110)面,做成4层簇模型,其中含36个重原子(20个O,16个Al),如图2所示。其中,(100)面的尺寸分别为 a=b=0.5687 nm,c= 0.4170 nm(厚);(110)面的尺寸为 a=0.4267 nm (厚),b=0.6107 nm,c=0.5687 nm。考察的着眼点是(100)面和(110)面的八面体位上的6配位Al。
在进行构象优化时,使用 H质子饱和表面的悬挂键,出于计算条件的考虑将其余部分的 O和 Al冻结。采用B3L YP方法[12],使用6-31G基组,计算工具为 Gauusian03程序包[13]。
吸附质与γ-Al2O3簇之间的吸附能 Eb-c按式(1)计算。
Eb-c= Eb+c- Ec- Eb(1)
式(1)中,Ec和 Eb分别为原子簇和吸附质分子无限远离时的能量,Eb+c是原子簇与吸附质稳定吸附时的总能量,kJ/mol。
1.2 实验方法
采用小型连续固定流化床式实验装置。该装置包括吸附配气系统、吸附系统、分析系统和处理放空系统,其核心部位为吸附器。吸附器材质为不锈钢,上段尺寸为 φ48 mm×4 mm×200 mm;下段为φ14 mm×2 mm×600 mm。吸附气为配制烟气,含有SO2、NOx(NO和NO2)、CO2、O2和N2。采用D07-18A/ZM型质量流量控制计和D08-8C/ZM流量积算仪(北京七星华创电子股份有限公司产品)分6路计量气体。NO、NO2和 SO2原始样品为北京氦谱北分气体工业有限公司产品,其中 NO、NO2和 SO2的体积分数分别为1.0%、0.18%和2.0%,底气为 N2。配制烟气的组成见表1。采用KM9106型综合烟气分析仪在线分析(10 s记录1次)吸附过程的原料和尾气。

表1 配制烟气的体积组成Table 1 Volume composition of flue gas %
进行吸附剂的性能评价时,先测定吸附器中无吸附剂时 SO2、NOx的流出曲线,称为空白吸附。然后测定在吸附剂存在下 SO2、NOx的流出曲线,通过比较对应时刻下空白和吸附后被考察物种的体积分数变化,得到相应的脱除率,按式(2)计算。

式(2)中,xi为i时段的脱除率,%;ci和c0分别为i时段吸附和空白吸附时的吸附质浓度。
2 结果与讨论
2.1 理论计算
在B3lyp/6-31G水平下优化得到了SO2、NO2、NO的结构参数,结果列于表2。表2中3种分子的结构数据与X-ray衍射实验数据存在一定偏差,但这不影响将其作为基准来考察它们与晶体表面铝的作用情况。

表2 B3lyp/6-31G水平下的SO2、NO和 NO2的结构参数Table 2 G eometric parameters of SO2,NO and NO2 optimized with B3lyp/6-31G
由不同的吸附质分子与晶面的初始吸附模型出发,可以得到相应的势能极小值点,比较后得到其中的最小值,进而获得优化后的结构参数和势能。以SO2为例,经优化后其在γ-Al2O3的(100)面和(110)面上的吸附构象示意图见图3。

图3 SO2在γ-Al2O3晶体的(100)面和(110)面上的吸附构象Fig.3 Conformations of SO2over(100)and(110) ofγ-Al2O3crystal(a)(100);(b)(110) Grey ball,red ball and yellow ball represent Al,O and S,respectively.
由图3可知,SO2之所以能吸附在(100)面或(110)面,是表面模型中用于中和悬挂键的质子H脱掉,使得6配位 Al空出1个配位来接受来自SO2的1个O原子的孤对电子,最终将SO2键接在表面。以SO2分子中与6配位 Al接触的 O记为O1,另1个记为O2,吸附在2个晶面上的SO2的结构数据分别为:(100)面上,dO1—Al=0.2017 nm, dS—O1=0.1878 nm,dS—O2=0.1750 nm,AO1—S—O2= 102.1°;(110)面上,dO1—Al=0.1959 nm,dS—O1= 0.1827 nm,dS—O2=0.1756 nm,AO1—S—O2=98.5°。
与表2中 SO2分子的基准数据相比,吸附在(100)表面后,由于晶面上 Al的作用,SO2的2个S—O键均变长,说明具有空轨道的 Al的吸电子作用,使得SO2中的电子转向Al,S与O1和O2的作用削弱;但 2个键变长的幅度不同,dS—O1> dS—O2,这是由于O1距Al更近一些,O1的电子密度转向Al的份额也多一些,O1与S的结合作用比O2与 S来得弱一些。此外与晶格中Al—O的键长0.1934 nm 比起来,O1与 6配位 Al的距离0.2017 nm要大一些,说明 SO2与(100)面中的6配位Al的结合强度弱于晶格中的O1—Al,遇有外力作用后,O1—Al间形成的键更容易断裂,从而使SO2的脱附变为可能。(110)面的情形与此类似。
根据式(1)处理后,得到 SO2在(100)面上的吸附能为-648.3 kJ/mol,在(110)面上的吸附能为-594.8 kJ/mol,说明 SO2在(100)面上的吸附占有热力学上的优势。
类似可以得到NO2和NO在2个面上的吸附结果。由于(110)面上的6配位Al无悬挂 H保护时呈4配位状态,有2个配位可以利用,SO2和NO2的2个O可以共同与这个 Al键合,形成环状结构,如图4所示。
SO2、NO2、NO分别吸附在γ-Al2O3的(100)面和(110)面上的构象数据见表3。
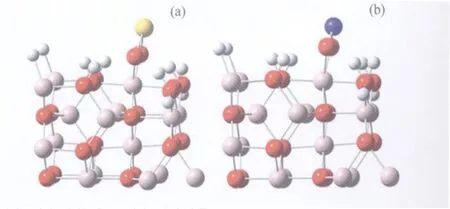
图4 SO2和 NO2在(110)面上的环状吸附构象Fig.4 Cycle conformations of SO2and NO2 over(110)ofγ-Al2O3(a)Conformation of SO2over(110); (b)Conformation of NO2over(110)Grey ball represents Al,red ball O,yellow ball S,blue ball N
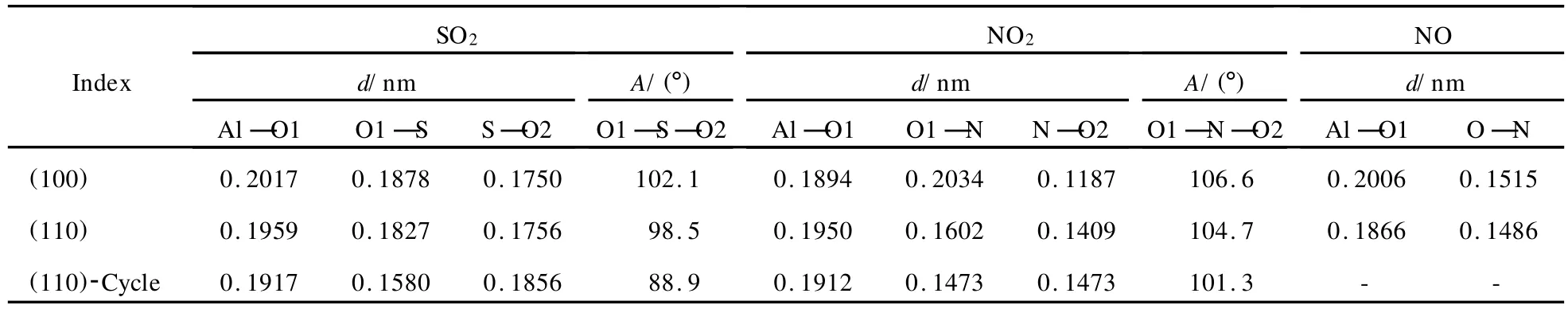
表3 SO2、NO2、NO分别吸附在γ-Al2O3的(100)面和(110)面上的吸附构象数据Table 3 G eometric data of SO2,NO2,NO adsorptions over surfaces ofγ-Al2O3
由表3可见,NO2和 NO在γ-Al2O3的(100)面和(110)面上吸附后构象的变化情况与 SO2类似,引起变化的原因也类似。在(110)面与 SO2、NO2的环状构象中,dAl—O1=dAl—O2,说明此种情形下O1、O2所处的环境是充分相近的;但从其数值上看,键长0.1917 nm和0.1912 nm均小于晶格中dAl—O的0.1934 nm,预示着此种情况下实现 SO2、NO2的脱附有难度。
虽然在初始吸附模型设计中有3种吸附质分子中的S或N与Al位作用的构象,但优化后均未得到收敛的结果,说明3种吸附质中的O与表面 Al的键接方式占优。
对应 SO2、NO2、NO分别吸附在γ-Al2O3的(100)面和(110)面上的吸附构象,得到相应的吸附能数据,见表4。
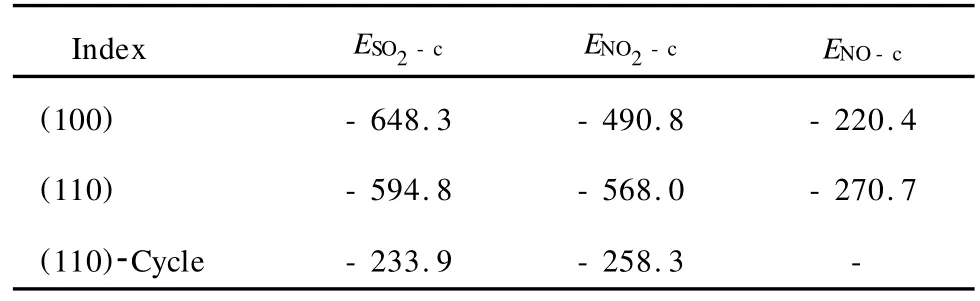
表4 SO2、NO2、NO分别吸附在γ-Al2O3的(100)面和(110)面上的吸附能Table 4 Adsorption energies of SO2,NO2,NO over surfaces ofγ-Al2O3 kJ/mol
由表4可见,SO2在2个面上的吸附能有53.5 kJ/mol的差值,SO2被(100)面吸附的趋势强于(110)面;类似的原因,NO2和NO被(110)面吸附的趋势强于(100)面。不论(100)面还是(110)面上的6配位 Al,对 SO2的吸附能力均明显强于对NO2和NO的吸附。在环状吸附的(110)面上,表面对NO2和 SO2吸附能的差值是24.4 kJ/mol,对NO2的吸附能力略强于 SO2。即使2类表面对3种气体的吸附能力不同,但总的说来还是具有同时脱硫脱氮的能力。
在γ-Al2O3晶体中,(100)面和(110)面是最容易存在的晶面,也是进行吸附操作的工作面。因此这2个面的吸附能力可以代表整个晶体的总体吸附能力。同样,这2个面上6配位Al的吸附能力可以代表γ-Al2O3晶体中6配位Al的能力。但6配位Al对总吸附能力的贡献比例,还有待商榷。
陈英等[7]认为,在含有SO2、NO和O2的气氛中γ-Al2O3对SO2的吸附作用源于其表面O位、表面O空穴与气态O的传递、NO的协同作用等。如果SO2和NO吸附在与表面Al相邻的O位,经过相应的原子迁移活动使吸附在 O位的 SO2得到来自NO的1个O,与邻近金属形成硫酸盐得以固定在表面,而丢失1个O的NO则将1个表面O攫取形成1个新的NO,留下1个表面O空位后自己返回到气流中去,表面O空位则靠气相 O的迁移再形成表面O;如果SO2和NO被吸附在与表面Al相间或者更远的O位,NO的O传递不到 SO2那里去,那么 NO就会拔走吸附它的表面 O生成NO2,留下表面O空位后进入气流主体。按照这种说法,吸附SO2和NO的表面O的位置若是隔Al位相邻,NO不能留在表面;若是隔 Al位相间, NO仍不会留在表面但会转变成 NO2;2种情况下表面Al位均不直接参与吸附过程。
2.2 实验结果
吸附剂为γ-Al2O3(山东铝业集团生产),装剂量2.5 g,进料标准状态体积流率1800 mL/min,吸附温度200℃,吸附时间10 min。吸附剂脱除SO2、NOx的性能如图5所示。定义 SO2脱除率达到90%时的吸附时间为穿透时间,记为 ts,吸附容量为每克吸附剂吸附溶质的毫克数。根据全程运转时间和 ts将操作按2个时间段考虑,经计算得到针对3种吸附质的吸附容量和平均脱除率,见表5。

图5 SO2、NO和 NO2在γ-Al2O3的脱除率(x)随流出时间的变化Fig.5 Removal rate(x)of SO2,NO and O2over γ-Al2O3vs effluent time(1)NO;(2)NO2;(3)SO2
表5 γ-Al2O3对SO2、NO和 NO2的吸附容量(Cad)和平均脱附率()Table 5 Adsorption capacity(Cad)and average removal rate()of SO2,NO and NO2overγ-Al2O3

表5 γ-Al2O3对SO2、NO和 NO2的吸附容量(Cad)和平均脱附率()Table 5 Adsorption capacity(Cad)and average removal rate()of SO2,NO and NO2overγ-Al2O3
Sample Cad/(mg·g-1)X i/% 600 s ts 600 s ts SO2 29.70 20.00 88 99 NO 3.83 2.88 56 73 NO2 0.14 0.72 15 75 NOx 3.97 3.60 51 73
由图5可见,当吸附时间在600 s内,吸附前期SO2的脱除率维持在接近100%的水平,至吸附时间为330 s时,脱除率才降为90%,330 s即此次操作的 ts;在 ts后SO2的脱除率平缓下降,至吸附操作结束时仍保持55%的SO2脱除率。NO的脱除率整体上由高到低,但是在吸附时间前330 s的时段内有个小波动,出现1个小波谷,之后平稳下降,结束时的脱除率为 20%左右;NO2的脱除率在330 s后急剧下降,至吸附操作结束时脱除率为-180%左右,说明此时吸附剂向物流中释放了NO2。由表5可见,对 SO2而言,对应全程操作的约30 mg/g的吸附容量,ts之前的吸附容量为20 mg/g,占了2/3的比例,而且 ts之前的平均脱除率达99%;对于NO,ts之前的吸附容量占全程容量的75%;而对于NO2,ts之前的吸附容量是全程容量的500%还多。综合来讲,γ-Al2O3对 SO2的吸附能力远远大于对NOx的能力,对3种吸附质吸附容量由大到小的顺序为:SO2、NO、NO2。
由于吸附实验在200℃下进行,虽然没有实验精确验证γ-Al2O3属于哪种工作表面,但可以推断:可能存在于γ-Al2O3表面的 H2O和 OH会脱除,表面的O位和Al就会以缺陷点的形式暴露,形成吸附的活性中心。
从NO2在γ-Al2O3上的吸附行为看,在 SO2的 ts之前的脱除率高达75%,说明表面的6配位Al发挥了作用;而 ts之后的脱除率急剧下降乃至出现负值,但与此同时依然维持相当数量的NO的脱除率,验证了表面O位发挥作用生成 NO2的说法。
从NO在γ-Al2O3上的吸附行为看,在SO2的ts之前的脱除率为73%,但吸附曲线中存在小波谷,说明表面6配位 Al发挥了主要作用,另一方面NO和 SO2隔Al相邻吸附在O位,固定了SO2、覆盖了Al活性位又释放出了NO;而 ts之后NO仍维持一定的脱除率、与此同时NO2的脱除率出现负值,证实了O位与NO结合生成NO2的解释。
NOx的吸附行为证实了表面上6配位Al和表面O的存在和发挥的作用,那么对 SO2吸附同样是这2类活性中心共同作用的结果。ts之前,主要是表面Al发挥作用;ts之后,表面O位发挥主要作用。
SO2本身的活泼性、原料气中相对高的体积分数、NOx分子的协同作用、大量存在的表面活性位,使得SO2在γ-Al2O3上的吸附始终占优,这与前面的理论预测相符。
理论计算表明,γ-Al2O3的(100)面和(110)面上的Al位对 NO2的吸附作用均强于对NO的作用,这与实验结果有偏差,究其原因在于,实验物流中φ(NO)/φ(NO2)≈7,即便有少量的NO与表面O位作用生成NO2,也会显著干扰对NO2的相应计算。另外,计算精度受计算资源和能力的限制、理论计算局限于0 K状态下势能的计算,属于热力学范畴,尚未考虑热力学因素以及宏观的扩散等因素,都是产生偏差的原因。但随着计算能力的进一步提高,理论计算将在性能预测和微观机理探索方面发挥越来越大的作用。
3 结 论
(1)利用分子力学计算确定了γ-Al2O3的晶体结构及其(100)面和(110)面的结构数据;建立了(100)面和(110)面的物理模型,采用B3lyp/6-31G密度泛函方法考察了2个晶面中的6配位八面体Al位对SO2、NOx(NO2及 NO)吸附的构象特征,综合得到2个表面对吸附质的吸附能的强弱顺序是: SO2、NO2、NO。其中 SO2在(100)面上的吸附能力强于其在(110)面上的能力;NO2和NO在2个面上吸附能力顺序与 SO2相反;在与(110)面形成环式构象的吸附中,NO2的吸附能力大于SO2。
(2)吸附实验结果与理论预测基本吻合,借助实验结果可以推断:γ-Al2O3表面存在6配位Al位和O位2类缺陷活性点,在SO2穿透时间前Al位对SO2、NOx吸附起主要作用;在 SO2穿透时间后O位发挥主要作用。
致谢:感谢中国石化石油化工科学研究院16室周涵、代振宇、赵毅博士及陈远明、阎杰高级工程师在模型讨论及远程技术方面给予的帮助,感谢2室于敬川、陈西岩在实验方面给予的协助;感谢中科院化学所杨小震教授和荷兰 Wageningen大学 Han Zuilhof教授在程序使用方面提供的支持。
[1]SHIRAISHI I,NINAGAWA Y,TSUJ IK,et al. Production process of formed activated coke for SOxand NOxremoval having high NOx-removing ability:US, 5270279[P].1993.
[2]FELSVANG K,BOSCAK V,IVERSEN S B,et al. Update on SNAP technology for simultaneous SOxand NOxremoval[C]//EPRIDOE-EPA Combined Utility Air Pollutant Control Symposium,The Mega Symposium, Atlanta,GA,1999.
[3]DAS A K,WILDE J D,HEYNDERICKX G J,et al. Simultaneous adsorption of SO2-NOxfrom flue gases in a riser configuration[J].AIChE Journal,2001,47(12): 2831-2844.
[4]WILDE J D,DAS A K,HEYNDERICKX G J,et al. Deveplopment ofatransientkenetic model forthe simultaneous adsorption of SO2-NOxover Na/γ-Al2O3sorbent[J].Int Eng Chem Res,2001,40(1):119-130.
[5]李平,赵越,卢冠忠,等.SO2对 NO催化氧化过程的影响 Ⅰ载体的作用[J].华东理工大学学报,2002,28 (4):397-440.(LI Ping,ZHAO Yue,LU Guanzhong, et al.Effect of SO2on NO catalytic oxidationⅠRole of supports[J].Journal of East China University of Science and Technology,2002,28(4):397-440.)
[6]李平,赵越,卢冠忠,等.SO2对NO催化氧化过程的影响 Ⅱ载体γ-Al2O3与SO2的相互作用[J].高等学校化学学报,2001,22(12):2072-2076.(LI Ping, ZHAO Yue,LU Guanzhong,et al.Effect of SO2on NO catalytic oxidation Ⅱ Interaction betweenγ-Al2O3support and SO2[J].Chemical Research in Chinese Universities,2001,22(12):2072-2076.)
[7]陈英,李雪辉,徐建昌,等.催化剂载体γ-Al2O3上NO对 SO2的氧化吸附[J].华南理工大学学报(自然科学版),2004,32(11):1-5.(CHEN Ying,LI Xuehui, XU Jianchang,et al.Effect of NO on SO2oxidation adsorption over catalyst supportγ-Al2O3[J].Journal of South China University of Technology (Natural Science),2004,32(11):1-5.)
[8]IONESCU A,ALLOUCHE A,AYCARD J P,et al. Study ofγ-alumina surface reactivity:Adsorption of water and hydrogen sulfide on octahedral aluminum sites [J].J Phys Chem B,2002,106(36):9359-9366.
[9]YAMANAKA T,TAKEUCHI Y,TOKONAMI M. Anharmonic thermal vibrations of atoms in MgAl2O4spinel attemperatures up to 1933 K[J]. Acta Crystallographica B,1984,40(2):96-102.
[10]GAL E J D. GULP-acomputerprogram forthe symmetry adapted simulation of solids[J].JCS Faraday Trans,1997,93(4):629-637.
[11]BUSH T S,GALE J D,CATLOW C R A,et al.Selfconsistent interatomic potentials for the simulation of binary and ternary oxides[J].J Mater Chem,1994,4: 831-837.
[12]BECK A D.Density-functional thermochemistry III The role of exact exchange[J].J Chem Phys,1993,98: 5648-5652.
[13]FRISCH M J,TRUCKS G W,POPLE J A,et al. Gaussian 03,Reversion B 03[CP/CD].Pittsburg PA: Gaussian Inc,2003.
