闭塞性外周动脉粥样硬化症
2009-09-16005沈阳军区空军司令部门诊部李冬梅张汉道
005 沈阳军区空军司令部门诊部 李冬梅 张汉道
125105 沈阳军区兴城疗养院 张 雷2
闭塞性外周动脉粥样硬化症
110015 沈阳军区空军司令部门诊部 李冬梅1张汉道3
125105 沈阳军区兴城疗养院 张 雷2
闭塞性外周动脉粥样硬化 (peripheral arteriosclerosis obliterations,PASO)是指除冠状动脉之外的动脉血管由于粥样硬化引起血管的狭窄、闭塞或瘤样扩张性疾病[1],1891年由Von Mantanfel首次报道。近年来,该疾病的诊断及治疗有了很多新的进展,现将其综述如下。
1 病因和发病机制
闭塞性外周动脉粥样硬化是一种全身性疾病,其病理变化如同冠状动脉粥样硬化一样,以内膜受损为启动机制,某些区域血管血流的应力、张力和压力的变化,如血管分枝或分叉的对角处所产生的湍流和涡流的持续性压力,可造成血管内膜损伤,在此基础上脂质沉着,形成动脉粥样硬化斑块。由于粥样硬化斑块逐渐增长,导致管腔进行性狭窄,当管腔狭窄达到50%~60%,出现远端缺血症状[2]。由于斑块内出血或斑块破裂,导致继发性血栓形成,引起远端严重缺血以至于坏死。病变血管可见于心脏及脑以外的全身动脉,包括下肢、肾、肠系膜及腹主动脉等,以腹主动脉下端、髂动脉、股动脉和动脉最为常见,上肢动脉较少累及。
2 临床表现
本病好发于50岁以上男性,男女发病率之比为10∶1。病程进展隐匿,缺乏典型的临床症状,病变最常见部位是下肢动脉[3]。但大部分患者并没有可以被识别的肢体缺血症状。下肢血管病变最早出现的症状是患肢发凉、麻木和跛行。本病跛行症状由活动诱发,休息可缓解,呈现典型的“行走—疼痛—休息—缓解”的规律,需与其他原因引起的假性跛行相鉴别。随着病情的加重,行走距离会逐渐缩短。行走距离和疼痛部位可提示血管病变的范围和程度。小腿疼痛提示浅表股动脉阻塞;大腿和小腿均痛提示髂股动脉阻塞;髋部和臀部疼痛提示主髂动脉阻塞。男性有阳痿等性功能障碍伴股动脉搏动消失提示下腹部主动脉阻塞。病变位于上肢的血管时,在上肢活动后也可表现出类似的“间歇性跛行”症状;当供应脑部的血管阻塞时出现耳鸣、眩晕、构语障碍、复视、双侧视力模糊、单侧或双侧感觉缺失,甚至昏厥,称“脑窃血综合征”。随着缺血的加重,下肢疼痛由活动后转为休息时,常发生于夜间入睡后数小时,病人常因下肢严重的烧灼样疼痛而觉醒,肢体下垂疼痛减轻,称为“静息痛”。静息痛的出现预示着患肢即将丧失运动功能。如果缺血进一步加重,患肢下垂疼痛也不能缓解。此外,由于缺血和营养的匮乏,患肢出现皮肤变薄、颜色苍白、温度下降、感觉减退、汗毛脱落、患肢肌肉萎缩、趾甲增厚变形、骨质稀疏,当损伤或感染后出现溃疡和坏疽,局部甚至发生蜂窝组织炎、骨髓炎或败血症,如缺乏有效治疗,可能导致截肢甚至危及生命。
此外,由于血管的阻塞或狭窄,患肢可出现动脉搏动减弱或消失,病变侧肢体血压测量数值降低或测不出。狭窄的血管周围可闻及收缩期或连续性血管杂音,尤以运动后显著。少数可扪及扩张的动脉瘤,多见于窝或腹股沟韧带以下的股动脉部。
3 危险因素
该病的发生同年龄、吸烟、糖尿病、高脂血症、高血压、高同型半胱氨酸血症及肥胖等因素有关。下肢动脉疾病的高危人群包括:①年龄<50岁,有糖尿病和1项其他动脉粥样硬化的危险因素或糖尿病病史≥10年。②年龄在50~69岁之间,有吸烟或糖尿病史。③年龄≥70岁。④劳累相关的腿部不适或缺血性静息痛。⑤下肢脉搏检查异常。⑥确诊的粥样硬性冠状动脉、脑血管或肾动脉疾病患者。对于高危人群应进行详细的体格检查和必要的相关检查。
4 相关检查
由于外周动脉疾病患者的症状隐匿,仅10%~30%有间歇跛行的表现,大部分患者没有可以被识别的肢体缺血症状,因此只有通过较为敏感的检查方法才能够作出诊断。
4.1 踝肱指数(ABI) 通过血压计和多普勒探头,分别测量踝动脉、肱动脉血流恢复时的收缩压值,两者之比称为ABI。如果两侧肱动脉收缩压有区别,取其高值作为肱动脉收缩压,两侧踝动脉收缩压则选低值作为踝动脉收缩压。正常值在0.90~1.30之间。ABI<0.90诊断下肢动脉硬化性疾病与血管造影比较敏感性为95%,特异性为99%,ABI是诊断下肢动脉硬化性疾病可靠的无创指标[4]。其中ABI在0.41~0.90之间表明血流轻到中度减少,ABI值≤0.40,表明重度血流减少。
4.2 趾臂指数测定 许多长期糖尿病、老年以及终末期肾病需要透析的患者因为血管中层的钙化,导致踝动脉僵硬,影响ABI或节段压力测定的准确性。当ABI>1.3或测得的下肢收缩压异常增高,超过生理情况下从心脏到下肢动脉节段收缩压的增加时 (通常大于2.7 kPa或高于上臂收缩压的20%),考虑可能存在动脉僵硬的情况。趾动脉通常不涉及弹性动脉的钙质沉着,因此可以通过测定趾动脉收缩压来代替踝动脉收缩压,比值称为趾臂指数,趾臂指数<0.7即可诊断下肢动脉硬化性疾病。
4.3 脉搏容积记录 动脉血流入下肢是搏动性的,因此在每个心动周期中随着血液的灌注,肢体容积发生变化。测定下肢容积变化可作为评价肢体灌注的定性或定量资料,因此可以用于外周动脉疾病的初步诊断。脉搏容积记录能评价病变的位置和严重程度,预测严重肢体缺血和截肢的风险,对在ABI和节段压力假性增高的血管僵硬患者有重要诊断价值。此外,还可以用于下肢血管重建术后患者肢体灌注的评价。
4.4 运动试验与运动后ABI 运动试验可测定患者出现症状的行走距离(初始跛行距离)及从出现症状到因症状而停止运动的距离(绝对跛行距离),用于病情的分级及疗效的评价。此外,通过运动前的静息ABI和运动后的ABI比较,可以鉴别由下肢外周动脉疾病引起的“跛行”和其他原因引起的“假性跛行”。
4.5 双功能超声(duplex ultrasound) 用于诊断四肢血管病变的位置和狭窄程度;介入病例的选择;旁路移植术病人和手术吻合部位的选择,以及血管重建术后的随访。在评价动脉瘤、动脉夹层、动脉筋膜室综合征、囊状淋巴管瘤和探查血管性疾病患者的软组织肿块方面有广泛的临床用途。诊断髂动脉到动脉的≥50%腔径狭窄的敏感性和特异性可达到90%~95%。
4.6 计算机断层扫描血管造影(CTA) 计算机断层扫描血管造影检查可用于血管病变的解剖学定位和管腔狭窄程度的判断。可作为对磁共振血管成像(CE-MRA)有禁忌患者的替代检查,与血管造影相比,CTA可以通过三维成像在空间自由旋转,有助于评价偏心狭窄。但空间清晰度相对较低,两侧下肢造影不对称导致漏掉一些血管的动脉相,以及三维成像处理复杂等是其不足。
4.7 CE-MRA CE-MRA可用于病变的解剖定位、狭窄程度的判定以及介入病例的筛选,还可用于旁路移植手术和手术吻合部位的选择以及血管重建术后的监测。
4.8 血管造影 目前为止,血管造影仍被认为是确定正常血管解剖和血管病理的“金标准”,是唯一被普遍接受的用于指导经皮外周介入操作的方法。可提供有关动脉解剖的详细信息,适用于计划行血管重建的下肢动脉疾病患者的诊断及术前检查。其中数字减影血管造影成像的能力较非减影造影强。
5 诊断
有外周动脉硬化性疾病危险因素的患者,如果出现典型的间歇性跛行、静息痛及坏疽症状,可以据此作出临床诊断。所有可疑病人均应进行ABI检查,有劳累性下肢症状、伤口不愈合、年龄≥70岁或年龄≥50岁但有吸烟或糖尿病史的患者,静息ABI≤0.90即可成立诊断。ABI范围在0.90~1.30的患者,如果无典型间歇性跛行症状及其他动脉粥样硬化临床表现,但有下肢动脉疾病危险因素的人群应该进行运动ABI检查。运动ABI下降超过20%可以诊断。如运动ABI无异常,患者跛行可能是由非血管性因素所引起的假性跛行。对于ABI≥1.30的人群,可能存在踝动脉的僵硬,应进一步进行脉搏容积描记、足趾压力测定、双功能超声、CTA或CE-MRA等检查。下肢外周动脉硬化性疾病诊断流程(图1)。
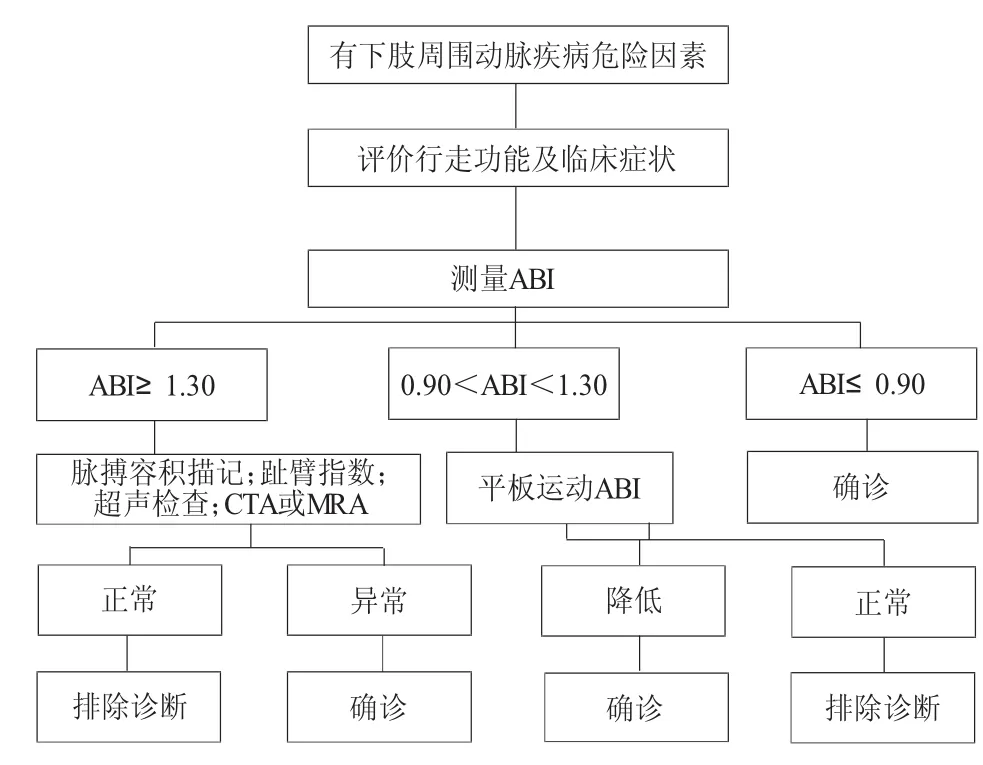
图1 诊断流程
6 治疗
对于无症状的外周动脉硬化性疾病患者应积极改善生活方式,控制危险因素,对有临床症状的患者应该进行相应的针对性治疗包括改善跛行,减轻静息痛,改善肢体循环,促进溃疡愈合,对症状明显或药物治疗不理想者可以考虑血管重建,有些患者甚至需要截肢手术。
6.1 危险因素的控制 外周动脉硬化性疾病患者应重视生活方式的改变,如:戒烟、合理饮食、控制体重、适当锻炼、足部保健等。对于危险因素应严格控制。外周动脉硬化性疾病被认为是冠心病的等危症,其心、脑血管事件的发病率等同于冠心病。因此,其危险因素应严格按照冠心病的标准进行控制。血压的控制:一般血压应控制在18.7/12.0 kPa以内,心衰和肾功能不全患者应在18.0/11.3 kPa以内,糖尿病患者应在17.3/10.7 kPa以内。降压药物应根据患者的不同情况进行选择,目前认为ACEI类药物较适合外周动脉硬化性疾病患者的降压治疗。血脂的控制:LDL-C应控制在100 mg/dL以内,对于极高危的患者可以将LDL-C控制在70 mg/dL以内。他汀类药物是较理想的调制药物。血糖控制:合并糖尿病的患者应积极控制血糖,空腹血糖应在6.1 mmol/L以内,糖化血红蛋白应控制在7%以内,并注意控制餐后血糖。此外,还应积极进行抗血小板治疗,每日服用75~325 mg阿司匹林可以减少外周动脉硬化性疾病患者的心肌梗死、脑卒中或血管性死亡的风险,对阿司匹林有禁忌者可选择氯吡格雷每日75 mg。
6.2 改善跛行 没有心力衰竭的患者,口服西洛他唑50~100 mg,2次/d可以改善患者的行走距离,提高生活质量。对不能应用西洛他唑者可选用己酮可可碱400 mg, 2~3次/d,能增加最长行走距离。其他药物如: L-精氨酸、丙酰-L-肉毒箭、银杏叶制剂及前列腺素类药物的疗效对改善跛行尚缺乏足够的循证医学的证据支持[4]。
6.3 改善肢体循环 前列腺素类药物如PGE-1或伊洛前列腺素可以部分减轻患者缺血性疼痛,并有助于溃疡的愈合。凝血酶抑制剂阿加曲班可抑制血小板聚集及血管收缩,使患肢组织氧分压及皮肤温度升高,有利于溃疡的愈合及减轻静息痛。链激酶、阿替普酶、瑞替普酶、替奈普酶等溶栓药物通过动脉导管溶栓可改善急性期缺血症状。
6.4 介入及手术治疗 外科手术和介入治疗不适用于仅有肢体血流灌注严重减少(如ABI<0.4)而没有相应临床症状的患者。对于临床症状较重或药物治疗不理想的患者可以考虑介入或手术治疗进行血管重建。下肢负重部分出现明显坏疽的非卧床患者,无法改善的屈曲挛缩患者,有肢体麻痹的患者,难以控制的缺血性静息痛患者,败血症或由于并存疾病影响生存的患者应考虑截肢。
7 预防
外周动脉粥样硬化症的预防关键在于对危险因素的早期干预。目前已知糖尿病是外周动脉硬化症最重要的的危险因素[5]。疾病的发生与糖尿病的病程和严重程度有关,糖尿病患者严重肢体缺血的风险明显高于非糖尿病患者,糖尿病患者的下肢动脉疾病患者接受大截肢几率增加7~15倍。吸烟是下肢动脉疾病的强有力的危险因素,80%的下肢动脉疾病患者有吸烟史,吸烟的量和发生下肢动脉疾病的危险显著正相关。吸烟者下肢动脉硬化性疾病的危险增加2~6倍,间歇性跛行的危险增加3~7倍。其他相关危险因素还包括:高龄、高脂血症、高血压、肥胖及高同型半胱氨酸血症等。培养健康的生活方式,早期干预存在的危险因素可在一定程度上减少外周动脉粥样硬化症的发生。
[1]Aronow WS.Management of peripheral arterial disease[J].Cardiol Rev,2005,13:61-68.
[2]Rancic Z,Radak D,Stojanovic D.Early detection of asymptomatic carotid disease in patients with obliterative arteriosclerosis of the lower extremities[J].Srp Arh Celok Lek,2002, 130:258-264.
[3]Schainfeld RM.Management of peripheral arterial disease and intermittent claudication[J].J Am Board Fam Pract,2001,14: 443-450.
[4]胡大一,杨进刚.下肢动脉疾病诊疗的专家共识[J].中国实用内科杂志,2006,26(11):1678-1683.
[5]杨进刚,胡大一.ACC/AHA新版外周血管疾病诊疗指南解读[J].中国医药导刊,2006,8(2):147-148.
1005-619X(2009)11-1024-03
2009-04-08)
