氨酪酸氯化钠注射液的质量研究
2009-06-03王志远
王志远
[摘要] 目的 为验证新生产的氨酪酸氯化钠注射液符合质量标准,达到销售要求。方法 参照相关文献,对氨酪酸氯化钠注射液的质量进行研究。结果 氨酪酸氯化钠注射液的各项指标达到要求。结论 新生产的氨酪酸氯化钠注射液符合质量标准,允许上市销售。
[关键词] 氨酪酸氯化钠注射液;氨酪酸;氯化钠
[中图分类号] R969;R971[文献标识码] A[文章编号] 1673-9701(2009)12-95-02
氨酪酸是一种氨基酸类抑制性中枢神经递质,临床用于脑卒中后遗症、脑动脉硬化症、头部外伤后遗症以及一氧化碳中毒所致昏迷的辅助治疗,亦可用于各型肝昏迷[1-3]。现将其质量研究报道如下。
1样品来源
氨酪酸氯化钠注射液由吉林省银河制药厂提供。批号:20080110,20080111,20080112;氨酪酸对照品:中国药
品生物制品检定所提供。
2含量限度
本品为含氨酪酸的灭菌水溶液,含氨酪酸和氯化钠均应为标示量的95.0%~105.0%。根据三批样品检测结果均在此限度范围内。
3性状
氨酪酸原料为白色粉末或结晶性粉末,氯化钠原料为无色透明结晶或结晶性粉末,本品为氨酪酸与氯化钠的灭菌水溶液。故将三批样品订为“无色的澄明液体”。

4鉴别[1,2]
(1)取本品5mL,加茚三酮试液数滴,加热煮沸,显蓝紫色。三批样品依法检验,均呈正反应,符合规定。另取0.9%氯化钠溶液5mL,同法试验,结果呈阴性。氯化钠对本鉴别反应无干扰。此反应为氨基酸类药物的共性反应,氨酪酸为氨基酸类药物,故具此反应。
(2)取本品,作为供试品溶液;另取氨酪酸参比试剂适量,加水稀释成相同浓度的溶液作为参比溶液,照薄层色谱法,吸取上述溶液各5μL,点于同一硅胶G薄层板上,以正丁醇-水-冰醋酸(5∶2∶1)为展开剂,展开后,晾干,喷以茚三酮的丙酮溶液(1→50),在90℃干燥10min,立即检视。供试品溶液所显主斑点的颜色与位置应与参比溶液相同。
(3)本品钠盐与氯化物的鉴别反应。钠盐:取铂丝,蘸取本品,在无色火焰中燃烧,火焰即显鲜黄色;取本品,加醋酸氧铀锌试液,即生成黄色沉淀。氯化物:取本品,加硝酸银试液,即生成白色凝乳状沉淀;分离,沉淀加氨试液即溶解,再加硝酸,沉淀复生成。三批样品依法检验,均呈正反应,符合规定。另取0.4%氨酪酸溶液,同法试验,结果均呈阴性,氨酪酸对本反应无干扰。
5检查
5.1pH值
取本品,依法测定,三批样品的pH值均接近7.0。国家标准氨酪酸注射液pH值为6.0~8.0,氯化钠注射液pH值为4.5~7.0。将本品pH值规定为6.0~8.0。结果见表1。
5.2有关物质的测定
γ-氨酪酸仅有紫外末端吸收,难以用HPLC法检查有关物质。若采用氨基酸类药物含量测定用的衍生法,由于衍生试剂及其分解产物等杂质的影响,对本品有关物质的测定带来干扰。所以参照中国药典2005年版[4],氨基酸类药物有关物质的检查方法,采用薄层色谱法对其有关物质进行监控,试验方法及结果如下。
5.2.1最低检出限与定量限取氨酪酸原料药0.2016g加水至100mL,每1毫升中含0.01mg、0.02mg的溶液,分别点于同一硅胶G薄层板上,照鉴别(2)项下的方法操作。结果:在该色谱条件下,最低检出限为0.01mg/mL。
5.2.2破坏性试验供试品溶液制备:取氨酪酸原料4.0g,加水至50mL,溶解后备用。取供试品溶液2mL,分别进行酸、碱、氧化和热破坏后,照鉴别(2)项下的方法检查。结果:在该色谱条件下,上述破坏性试验供试品液的色谱图均未显杂质斑点。说明本品在酸、碱、氧化和热条件下稳定,且该色谱条件能有效地分离检测氨酪酸的降解产物及杂质。
5.2.3有关物质检查供试品溶液配制:取本品作为供试品溶液(4mg/mL);对照品溶液配制:精密量取供试品溶液1mL,置100mL量瓶中,用水稀释至刻度,摇匀(0.04mg/mL),作为对照溶液(1.0%)。精密量取供试品溶液和对照溶液各5μL,点于同一硅胶G薄层板上,以正丁醇-水-冰醋酸(5∶2∶1)为展开剂,展开后,晾干,喷以茚三酮的丙酮溶液(1→50),于90℃干燥10min,立即检视。供试品溶液如显杂质斑点,所显杂质斑点的颜色,与对照溶液主斑点比较,不得更深。结果:三批样品均未检出杂质斑点。
5.3不溶性微粒
取本品,依法检查,应符合规定。三批样品经依法检验,结果均符合规定。
5.4细菌内毒素
取本品,依法检查,应符合规定。三批样品经依法检验,结果均符合规定。
5.5装量
取本品,依法检查,应符合规定。三批样品经依法检验,结果均符合规定。
5.6可见异物
取本品,照《可见异物检查法》[5]的规定检查,应符合规定。三批样品经依法检验,结果均符合规定。
6含量测定
6.1氨酪酸
参照氨酪酸注射液质量标准[6-8]中含量测定项下方法测定,并进行方法学验证。
6.1.1方法精密量取本品25mL(约相当于氨酪酸0.1g),置水浴上蒸至近干,加乙醇1mL,继续蒸干后,置105℃干燥约15min,置干燥器中放至室温,加冰醋酸10mL溶解,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定,至溶液显蓝绿色,并将滴定的结果用空白试验校正,即得。每1毫升高氯酸滴定液(0.1mL/L)相当于10.31mg的氨酪酸。
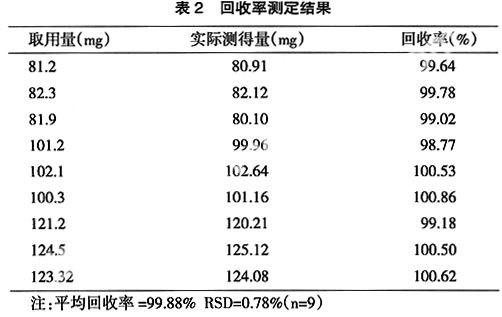
6.1.2回收率试验按供检量的80%、100%、120%,取氨酪酸原料(含量99.2%)约80mg、100mg、120mg,精密称定,各一式三份(共9份),每份分别加0.9%氯化钠溶液25mL,使溶解后(以0.9%氯化钠溶液25mL作空白实验校正)。照上述方法,自“置水浴上蒸至近干” 起,依法测定,计算回收率,结果见表2。
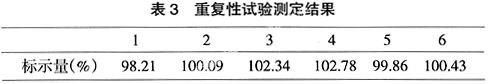
6.1.3重复性试验取本品(批号20080110)25.0mL(六份),照上述方法测定,结果见表3。
以上回收率试验及重复性试验说明,本法测定氨酪酸含量回收率高,重复性好,可收载入本质量标准中,以控制本品的氨酪酸的含量。
6.1.4样品含量测定三批样品照上述方法测定氨酪酸的含量,三批样品的含量测定结果均在标示量的95.0~105.0%范围内,符合规定。结果见表4。

7结论
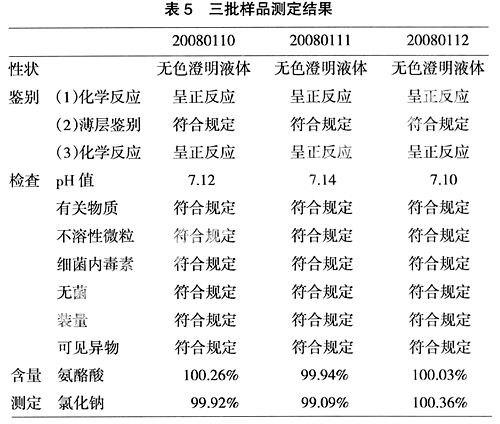
参照相关的规定与方法,对三批样品进行了外观性状、鉴别反应、pH值、不溶性微粒、细菌内毒素、装量、可见异物、有关物质、含量测定等项的质量研究工作,制定了氨酪酸氯化钠注射液质量标准草案。作为对本品初步稳定性考察的检验依据,三批样品按照本法检验,均符合规定。结果见表5。
[参考文献]
[1] 胡波,邱小鹰,梅元武. 氨基丁酸与脑缺血性损害的关系[J]. 国外医学:脑血管疾病分册,1999,7(6):323-326.
[2] 刘松岩,邬英全,赵力,等. 氨基丁酸在大鼠急性脑缺血再灌注损伤中的作用[J]. 脑与神经疾病杂志,1998,6(4):222-223.
[3] 陆勤,朱剑琴. γ-氨基丁酸的神经营养作用[J]. 国外医学:生理、病理科学与临床分册,1995,15(3):187-188.
[4] 国家药典委员会编.国家药品监督管理局化学药品地方标准上升国家标准[M]. 北京:人民卫生出版社,2002:01.
[5] 郑筱萸. 化学药品和治疗用生物制品研究指导原则(试行)[M]. 北京:中国医药科技出版社,2002:05.
[6] 国家药典委员会编. 中国药典2005年版二部[M]. 北京:化学工业出版社,2005:01.
[7] 周寒,李健和,黎银波,等. 氨酪酸氯化钠注射液的研制[J]. 中南药学,2007,5(6):511.
[8] 薛梅妍,王东凯,纪标. 薄层色谱法测定注射用氨酪酸中的有关物质及配伍稳定性[J]. 中国生化药物杂志,2006,27(2):89-91.
(收稿日期:2009-01-10)
