苗药芪胶升白胶囊防治乳腺癌化疗相关白细胞减少症的临床研究
2024-12-13楚立园韩丹阳田劭丹张玲段赟曾清吕丽媛陈信义兰梦好



〔摘要〕 目的 观察芪胶升白胶囊防治乳腺癌化疗相关白细胞减少症的临床疗效。方法 采用多中心随机、阳性药对照的临床试验设计,纳入4个中心119例气血两虚型乳腺癌化疗患者,按2∶1比例随机分为芪胶升白胶囊治疗组(n=79)和安多霖胶囊对照组(n=40),疗程为20 d。比较两组患者治疗前后白细胞和中性粒细胞计数及减少分级、中医证候与症状积分、后续化疗按时进行率和用药安全性。结果 治疗后,两组中医证候与症状积分均较治疗前降低(Plt;0.05),两组患者白细胞、中性粒细胞计数与减少程度分级和后续化疗按时进行率比较,差异无统计学意义(Pgt;0.05)。治疗组有1例患者出现轻度腹泻,但停药后好转。结论 芪胶升白胶囊防治乳腺癌化疗相关白细胞减少症具有一定优势,可有效改善气血两虚证,保障后续化疗按时进行,临床安全性良好。
〔关键词〕 乳腺癌;化疗;芪胶升白胶囊;白细胞减少症;临床研究
〔中图分类号〕R273" " " " "〔文献标志码〕A" " " " " 〔文章编号〕doi:10.3969/j.issn.1674-070X.2024.12.010
Clinical study of Miao medicine Qijiao Shengbai Capsule in the prevention and treatment of chemotherapy-induced leukopenia in breast cancer
CHU Liyuan1, HAN Danyang2, TIAN Shaodan1*, ZHANG Ling3, DUAN Yun4, ZENG Qing5,
LYU Liyuan1, CHEN Xinyi1, LAN Menghao1
1. Department of Hematology and Oncology, Dongzhimen Hospital of Beijing University of Chinese Medicine, Beijing 100700, China; 2. Beijing Gulou Hospital of Chinese Medicine, Beijing 100009, China; 3. Yunnan University of Chinese Medicine, Kunming, Yunnan 650500, China; 4. Gansu Provincial Cancer Hospital, Lanzhou, Gansu 730050, China; 5. The First Affiliated Hospital of Guangxi University of Chinese Medicine, Nanning, Guangxi 530023, China
〔Abstract〕 Objective To observe the clinical efficacy of Qijiao Shengbai Capsule in the prevention and treatment of chemotherapy-induced leukopenia in breast cancer. Methods A multi-center, randomized, and positive drug-controlled clinical trial design was used, enrolling 119 patients with breast cancer undergoing chemotherapy who presented with qi and blood deficiency pattern from four centers. They were randomly assigned to the Qijiao Shengbai Capsule treatment group (n=79) and the Anduolin Capsule control group (n=40) in a ratio of 2∶1. The treatment course lasted for 20 days. White blood cell count (WBC), absolute neutrophil count (ANC), and their respective reduction grades, as well as the Chinese medicine (CM) pattern and symptom scores, were compared between the two groups before and after treatment. Additionally, the rates of timely follow-up chemotherapy and medication safety were compared between the two groups. Results After treatment, the CM pattern and symptom scores in both groups decreased compared to those before treatment (Plt;0.05). There were no statistically significant differences in WBC, ANC, their respective reduction grades, or the rates of timely follow-up chemotherapy between the two groups (Pgt;0.05). One patient in the treatment group experienced mild diarrhea, which improved after discontinuing the medication. Conclusion Qijiao Shengbai Capsule has certain advantages in preventing and treating chemotherapy-induced leukopenia in breast cancer patients. It can effectively alleviate the symptoms of qi and blood deficiency and ensure the timely continuation of chemotherapy, with good clinical safety.
〔Keywords〕 breast cancer; chemotherapy; Qijiao Shengbai Capsule; leukopenia; clinical study
乳腺癌是女性最常见的恶性肿瘤,其发病率在世界范围内逐年递增,在我国位居女性恶性肿瘤发病率首位[1]。化学治疗目前仍是治疗和控制乳腺癌进展最有效的手段之一,白细胞减少症多发生在接受紫杉烷类联合蒽环类药物治疗的乳腺癌患者中,是影响化疗进程和疗效的严重不良反应。白细胞在外周血中存活时间为8~12 h,受化疗影响颇为显著,西医治疗以应用粒细胞集落刺激因子(granulocyte colony stimulating factor,G-CSF)为主要治疗措施,常规的升白药物如鲨肝醇、肌苷、维生素B4等用于治疗乳腺癌化疗相关白细胞减少疗效欠佳[2]。然而,G-CSF主要用于Ⅲ~Ⅳ级白细胞减少的患者,迅速提升外周白细胞计数(white blood cellcount,WBC)计数以便患者按时化疗,但不宜长期使用,且作用时间短、成本昂贵。实践证明,中西医结合防治化疗相关白细胞减少症优势显著,能够提高化疗完成率,改善临床症状,提高患者生活质量,具有增效减毒的效应[3-5]。白细胞减少引起的证候表现属于中医学“虚劳”“虚损”范畴,以脏腑亏损、气血不足为主要病机变化,其病位与脾、肾亏虚密切相关[6]。化疗药物对体内癌毒起到攻伐抗邪作用的同时,对全身的正气、脏腑和气血津液亦有严重的毒害作用,正如《素问·五常政大论篇》所言“大毒治病,十去其六”,“无使过之,伤其正也”。本研究依托国家科技重大新药创制专项《苗药芪胶升白胶囊技术改造及再评价研究》课题,旨在评价芪胶升白胶囊防治乳腺癌化疗所致白细胞减少症的有效性与安全性,为患者提供更多的治疗选择与保障。
1 资料与方法
1.1" 一般资料
选取来自北京中医药大学东直门医院、甘肃省肿瘤医院、广西中医药大学第一附属医院及上海中医药大学附属曙光医院4家三级甲等医疗单位收治的119例乳腺癌化疗后患者(2016年4月至2018年2月),依据随机数字表法,将符合入选标准的患者以2∶1比例随机分为治疗组和对照组,治疗组79例,对照组40例;其中12例患者因失访、拒绝提供可评价疗效的资料及放弃临床试验等原因自然脱落。所有患者均为女性,中位年龄49岁,最小年龄25岁,最大年龄74岁。入组时两组乳腺癌患者的疾病评级、病理类型、临床分期、病灶部位、转移部位、既往疾病、合并疾病、KPS评分等病情基线资料比较,差异均无统计学意义(Pgt;0.05),具有可比性,见表1。本研究经北京中医药大学东直门医院伦理委员会批准(ECPJ-BDY-2015-09)。本研究在中国临床试验注册中心注册,注册号为ChiCTR-IPR-15006759。
1.2" 西医诊断标准
参照《血液病诊断及疗效标准》拟定[7],化疗后成人外周血WBClt;4×109/L。当成人外周血中性粒细胞绝对值(absolute neutrophil count,ANC)lt;2.0×109/L时,为中性粒细胞减少症。
1.3" 中医诊断标准
中医辨证标准参考《中药新药临床研究指导原则》拟定“气血两虚证”辨证标准[8]。主症:神疲乏力,气短懒言;次症:头昏眼花,面色萎黄,自汗,心悸失眠;舌脉象:舌质淡嫩,舌苔薄白,脉象细弱。具备主症2项,次症1项以上,结合舌脉即可诊断“气血两虚证”。
1.4" 纳入标准
(1)经影像学及组织病理学或细胞学确诊为乳腺癌;(2)化疗前白细胞≥3.5×109/L;(3)中医辨证符合气血两虚证;(4)年龄18~75岁,性别不限;(5)KPS评分≥60分;(6)预计生存期至少3个月;(7)拟应用1周期含紫杉烷类药物的双药联合化疗;(8)未合并其他心、肝、肾、血液病等严重疾病病史;(9)自愿参加临床研究,并签署知情同意书。
1.5" 排除标准
符合以下任一条件:(1)年龄lt;18岁或gt;75岁;(2)存在骨髓转移;(3)化疗前已合并严重的心、肝、肾等疾病;(4)妊娠或哺乳期妇女;(5)精神病患者;(6)既往治疗过程中发现用药依从性差。
1.6" 干预方法
1.6.1" 给药方案" 在化疗进行的同时,试验组予芪胶升白胶囊(贵阳德昌祥药业有限公司,国药准字Z20025027,0.5 g×36粒),每日3次,每次4粒;对照组予安多霖胶囊(福州阿多拉制药有限公司,国药准字Z10970016,0.32 g×24粒),每日3次,每次4粒。两组患者均连续治疗20 d。
1.6.2" 合并用药注意事项" 对合并用药规定如下:(1)不使用如利可君、升白胺等升高白细胞的西药;在WBC低于2.0×109/L或ANC低于1.0×109/L时使用G-CSF 2.5 μg/(kg·d),若WBC低于1.0×109/L或ANC低于0.5×109/L时使用G-CSF 5 μg/(kg·d),连续使用3日,如WBC高于4.0×109/L则停用,否则继续应用。(2)原则上不使用其他中成药以及明确标注具有升高白细胞作用的单味中药和注射剂。(3)针对其他疾病治疗的药物,如纠正贫血、血小板减少、抗感染等药物,详细记录药名、用量、使用次数和转归等。
1.7" 观察指标
记录两组患者治疗前(即化疗第1天)及治疗后(化疗第20天)的有效性和安全性评估数据。(1)白细胞与中性粒细胞计数及分级:根据美国国家癌症协会常见毒性标准进行分级,白细胞减少症分级:WBC 3.0~4.0×109/L为Ⅰ级、2.0~3.0×109/L为Ⅱ级、1.0~2.0×109/L为Ⅲ级、lt;1.0×109/L为Ⅳ级;中性粒细胞减少症分级:ANC 1.5~2.0×109/L为Ⅰ级、1.0~1.5×109/L为Ⅱ级、0.5~1.0×109/L为Ⅲ级、lt;0.5×109/L为Ⅳ级[9]。(2)中医证候与症状积分:参考《中药新药临床研究指导原则》[8],记录治疗前、后两组患者中医证候总积分及神疲乏力、气短懒言、头昏眼花、自汗等单项症状积分。将症状分无、轻、中、重4个等级,根据症状分级主症分别记0、2、4、6分,次症分别记0、1、2、3分。(3)后续化疗按时进行率:统计各例患者能否按时进行后续化疗,对后续按时化疗进行率进行对比分析。(4)安全性评价:监测并记录不良事件发生情况,统计血常规、肝功能和肾功能等检验指标变化。
1.8" 统计学分析
采用SPSS 27.0.1统计软件进行分析。计量资料符合正态分布以“x±s”表示,比较采用t检验;偏态分布以中位数[M(P25,P75)]表示,两组比较采用非参数秩和检验。计数资料和等级资料采用例数及百分比描述,计数资料采用卡方或Fisher精确概率法检验,等级指标采用秩和检验。以Plt;0.05表示差异有统计学意义。
2 结果
2.1" 两组患者白细胞及中性粒细胞计数和分级比较
治疗前,两组患者WBC、ANC计数和分级比较,差异无统计学意义(Pgt;0.05),组间具有可比性。治疗后,两组患者WBC、ANC计数和分级比较的差异无统计学意义(Pgt;0.05)。随着化疗方案的实施,WBC和ANC减少程度分级逐渐加重。治疗后两组WBC和ANC减少程度分级较治疗前上升(Plt;0.05),考虑到该情况主要原因为化疗药物导致。详见表2—3。
2.2" 两组患者中医证候与症状积分比较
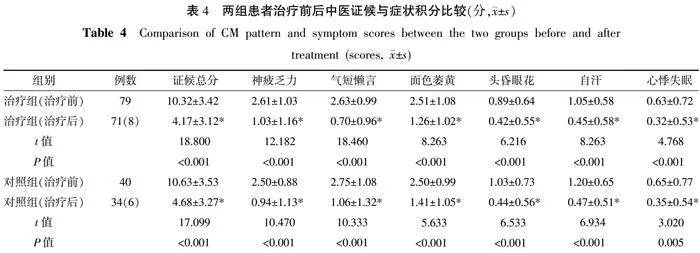
治疗前,两组中医证候与症状积分比较,差异无统计学意义(Pgt;0.05)。治疗后,两组神疲乏力、气短懒言、面色萎黄、头昏眼花、自汗、心悸失眠评分及中医证候总分均较治疗前降低,差异有统计学意义(Plt;0.05),治疗组和对照组组间比较差异无统计学意义(Pgt;0.05)。详见表4。
2.3" 两组患者后续化疗进行率比较
两组患者后续化疗进行率组间比较差异无统计学意义(Pgt;0.05)。详见表5。
2.4" 两组患者安全性指标比较
治疗组有1例患者出现轻度腹泻,停药后好转;对照组未出现不良反应。两组患者治疗前后血常规和肝肾功能未见明显异常,差异无统计学意义(Pgt;0.05)。
3 讨论
紫杉类药物是乳腺癌化疗的基石,而白细胞减少是紫杉类药物最常见的剂量限制性毒性反应,其引起的严重感染等并发症已成为肿瘤患者死亡的主要原因之一[10-11]。乳腺癌患者身患癌毒,正气本虚,复受化疗药毒所戕,损害脏腑,耗伤气血,本病治疗当以益气补血为主要原则。早期及时地干预可以缓解化疗所致骨髓抑制的恶化程度,阻止白细胞下降或舒缓其下降速度,充分发挥中医药“以防为主,防治结合”的治未病优势,提高患者远期生存率。
芪胶升白胶囊为苗药大品种,临床常用于防治因化疗或抗癌药物引起的白细胞减少症[12-14],其临证处方用药具有鲜明浓厚的民族特色。方中血人参为少数民族特色苗药,《贵州民间方药集》曰其“滋阴补肾,补气摄血”“补虚弱开力”,在当地具有广泛的药用价值。药理研究表明,血人参具有抗肿瘤、辅助癌症放化疗、抗氧化和保肝等作用[15]。阿胶滋阴补血、黄芪益气固表,为臣药,具有抗肿瘤、保护骨髓功能和提高免疫力的作用[16-17];当归补血活血、大枣健脾养血、苦参清热燥湿,三药合用为佐药,具有调节免疫、抗炎、保肝等作用[18-19];淫羊藿补肾强筋骨为使药,有类雄激素样作用,可提高机体耐缺氧能力等[20]。全方组方精练,用药讲究,共奏补血益气之功。阳性对照药物安多霖胶囊为国家保密品种,由抗辐射植物提取物、黄芪、鸡血藤等组成,具有益气补血、扶正解毒的功效,适用于放化疗引起的白细胞下降、食欲不振、神疲乏力、头晕气短等症,缓解肿瘤放化疗导致的骨髓抑制疗效确切[21-23]。
本研究采用了多中心、随机、阳性药物对照的临床试验方法,结果显示芪胶升白胶囊和安多霖胶囊防治乳腺癌化疗相关白细胞减少症,在改善WBC和ANC与减少程度分级方面,差异无统计学意义(Pgt;0.05)。芪胶升白胶囊组WBC和ANC下降发生率为28.17%和15.49%,安多霖胶囊组WBC和ANC下降发生率为26.47%和17.65%;循证医学研究显示,接受标准紫杉醇或多西他赛化疗的乳腺癌患者,中性粒细胞减少症的发生率高达83.3%~93.8%,4级ANC减少发生率可达22%[24-27],经与文献对照分析,提示芪胶升白胶囊和安多霖胶囊在促进白细胞及中性粒细胞复常、防治乳腺癌化疗相关白细胞减少方面均具有优势。
化学治疗药物引起的长期毒性严重影响大多数乳腺癌幸存者的生活质量,而肿瘤的治疗目标不仅是可以清除病灶,更应关注患者的全程康复管理,有效控制相关症状和提高患者生活质量,中医药在改善肿瘤相关病症方面具有明显的优势和特色[28]。本研究结果显示,芪胶升白胶囊和安多霖胶囊均能改善乳腺癌患者气血两虚证,防止药毒进一步耗伤气血,尤其能够减轻神疲乏力、气短懒言、面色萎黄、头昏眼花、自汗、心悸失眠的症状,减轻患者痛苦。文献报道,乳腺癌化疗每延期4周或1个月,患者总生存期下降15%,死亡风险增加1.3倍[29-30],这一影响在分期较晚或复发风险高的人群中更为显著。本研究结果显示,芪胶升白胶囊和安多霖胶囊能够保障患者后续化疗的按时进行,避免了治疗延期造成的负面影响。合并用药情况显示,治疗组22例患者使用了G-CSF,对照组11例患者使用了G-CSF,对比既往临床试验,二者均能降低G-CSF的使用率[31-32]。临床试验过程中,芪胶升白胶囊和安多霖胶囊对安全性指标均无致异常影响。
综上所述,芪胶升白胶囊防治乳腺癌化疗相关白细胞减少症具有一定优势,可有效改善气血两虚证,保障后续化疗按时进行,临床安全性良好。
参考文献
[1] HAN B F, ZHENG R S, ZENG H M, et al. Cancer incidence and mortality in China, 2022[J]. Journal of the National Cancer Center, 2024, 4(1): 47-53.
[2] 陶" 娟, 胡" 军, 梁运升, 等. 乳腺癌化疗相关骨髓抑制的中西医防治研究进展[J]. 光明中医, 2023, 38(18): 3670-3673.
[3] 中国中西医结合学会血液病专业委员会. 肿瘤放化疗后白细胞减少症中西医结合治疗专家共识(2022年版)[J]. 中华肿瘤防治杂志, 2022, 29(23): 1641-1646, 1652.
[4] XU X Q, LI H M, HU X W, et al. The efficacy and safety of diyushengbai tablet on preventing and treating leukopenia caused by radiotherapy and chemotherapy against tumor: A systematic review and meta-analysis[J]. Frontiers in Pharmacology, 2022, 13: 827710.
[5] WANG K H, SHEN H S, CHU S C, et al. Effectiveness of Chinese herbal medicine as a complementary treatment for neutropenia prevention and immunity modulation during chemotherapy in patients with breast cancer: Protocol for a real-world pragmatic clinical trial[J]. JMIR Research Protocols, 2024, 13: e55662.
[6] 田劭丹, 董" 青, 祁" 烁, 等. 化疗后白细胞减少症中医药防治与评估专家共识[J]. 现代中医临床, 2018, 25(3): 1-6.
[7] 张之南, 沈" 悌. 血液病诊断及疗效标准[M]. 3版. 北京: 科学出版社, 2007: 99-100.
[8] 郑筱萸. 中药新药临床研究指导原则: 试行[M]. 北京: 中国医药科技出版社, 2002: 177-180.
[9] US Department of Health and Human Services, National Institutes of Health, National Cancer Institute. Common Terminology Criteria for Adverse Events (CTCAE) Version 5.0[EB/OL]. 2017. https://academy.myeloma.org.uk/wp-content/uploads/2015/04/CTCAE v5. pdf.
[10] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)肿瘤放化疗相关中性粒细胞减少症规范化管理指南(2021)[J]. 临床肿瘤学杂志, 2021, 26(7): 638-648.
[11] BLAYNEY D W, SCHWARTZBERG L. Chemotherapy-induced neutropenia and emerging agents for prevention and treatment: A review[J]. Cancer Treatment Reviews, 2022, 109: 102427.
[12] 张" 玲, 叶宝东, 曾" 清, 等. 芪胶升白胶囊治疗气血两虚型白细胞与中性粒细胞减少症: 多中心随机对照试验[J]. 中国中西医结合杂志, 2021, 41(11): 1330-1335.
[13] 李" 燕, 陈" 蓉, 徐新倩. 芪胶升白胶囊治疗消化道恶性肿瘤化疗后骨髓抑制临床效果与安全性观察[J]. 中华中医药学刊, 2023, 41(7): 235-238.
[14] 陈" 剑, 王" 宙, 吕丽媛, 等. 芪胶升白胶囊预防结直肠癌术后化疗骨髓抑制临床研究[J]. 北京中医药, 2021, 40(7): 747-750.
[15] 廖泽宇, 傅" 建, 付慧晓, 等. 苗药血人参化学成分和药理作用研究进展及Q-marker的预测分析[J]. 中国民族民间医药, 2023, 32(12): 37-47.
[16] 虞跃跃, 俞瑶帅, 汪铱宇, 等. 黄芪多糖免疫调节和抗肿瘤作用机制研究新进展[J]. 世界中医药, 2023, 18(20): 2998-3003.
[17] 杨" 帅, 鲁婷婷, 周祖英, 等. 阿胶化学成分和药理作用及质量控制研究进展[J]. 中国新药杂志, 2023, 32(8): 806-816.
[18] 华" 龙, 王晨宇, 姚坤厚, 等. 基于Keap1/ARE通路探究氧化苦参碱对肝癌大鼠肝损伤的改善作用[J]. 中西医结合肝病杂志, 2022, 32(8): 710-713.
[19] 徐志伟, 李季文, 马新换, 等. 当归不同药用部位的化学成分及药理作用研究进展[J]. 中华中医药学刊, 2024, 42(4): 74-77.
[20] DONGYE Z C, WU X P, WEN Y X, et al. Icaritin and intratumoral injection of CpG treatment synergistically promote T cell infiltration and antitumor immune response in mice[J]. International Immunopharmacology, 2022, 111: 109093.
[21] 路鹏霏, 贾春丽, 吴" 戈, 等. 安多霖对食管鳞癌放疗期间骨髓抑制程度影响的研究[J]. 中华养生保健, 2023, 41(12): 1-4.
[22] 廖湘晖, 官成浓. 安多霖对进展期胃肠道肿瘤患者化疗前后免疫功能的影响[J]. 中医药临床杂志, 2015, 27(9): 1263-1265.
[23] 赵同德, 田劭丹, 侯" 丽, 等. 苗药芪胶升白胶囊防治化疗相关白细胞减少的临床研究[J]. 世界中西医结合杂志, 2020, 15(8): 1547-1552.
[24] JONES S E, ERBAN J, OVERMOYER B, et al. Randomized phaseⅢstudy of docetaxel compared with paclitaxel in metastatic breast cancer[J]. Journal of Clinical Oncology, 2005, 23(24): 5542-5551.
[25] 师文聪, 邓智平. 白蛋白结合型紫杉醇联合表柔比星及环磷酰胺在乳腺癌新辅助化疗中的效果及安全性[J]. 肿瘤研究与临床, 2021, 33(3): 200-203.
[26] GRADISHAR W J, TJULANDIN S, DAVIDSON N, et al. PhaseⅢtrial of nanoparticle albumin-bound paclitaxel compared with polyethylated castor oil-based paclitaxel in women with breast cancer[J]. Journal of Clinical Oncology, 2005, 23(31): 7794-7803.
[27] JEON Y W, KIM T H, YOUN H J, et al. A multicenter phase"Ⅱtrial of neoadjuvant chemotherapy with docetaxel and gemcitabine in locally advanced breast cancer[J]. Journal of Breast Cancer, 2017, 20(4): 340-346.
[28] 陈信义. 中医药提升肿瘤患者生活质量研究述评[J]. 北京中医药大学学报, 2022, 45(11): 1081-1088.
[29] YU K D, HUANG S, ZHANG J X, et al. Association between delayed initiation of adjuvant CMF or anthracycline-based chemotherapy and survival in breast cancer: A systematic review and meta-analysis[J]. BMC Cancer, 2013, 13: 240.
[30] TRUFELLI D C, MATOS L L, SANTI P X, et al. Adjuvant treatment delay in breast cancer patients[J]. Revista Da Associacao Medica Brasileira, 2015, 61(5): 411-416.
[31] VAN BELLE H, HURVITZ S A, GILBAR P J, et al. Systematic review and meta-analysis of febrile neutropenia risk with TCH(P) in HER2-positive breast cancer[J]. Breast Cancer Research and Treatment, 2021, 190(3): 357-372.
[32] DO T, MEDHEKAR R, BHAT R, et al. The risk of febrile neutropenia and need for G-CSF primary prophylaxis with the docetaxel and cyclophosphamide regimen in early-stage breast cancer patients: A meta-analysis[J]. Breast Cancer Research and Treatment, 2015, 153(3): 591-597.
〔基金项目〕北京中医药大学揭榜挂帅重点项目(2024-JYB-JBZD-007);国家科技重大专项项目-重大新药创制专项(2014ZX09301308007);国家中医药管理局高水平中医药重点学科建设项目中医血液病学(zyyzdxk-2023268);北京中医药大学东直门医院(国家中医药管理局下拨)-临床研究和成果转化能力提升试点项目(DZMG-ZJXY-23014)。
〔通信作者〕*田劭丹,女,博士,主任医师,E-mail:oliviatsd@126.com。
