2023年普通高中学业水平等级性考试(北京卷)化学试题及考查目标解读
2024-05-29黄晓斌郭宇凯
黄晓斌 郭宇凯

【试题部分】
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32
第一部分
本部分共14小题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是( )。
A.三种物质中均有碳碳原子间的σ键
B.三种物质中的碳原子都是sp3 杂化
C.三种物质的晶体类型相同
D.三种物质均能导电
2.下列化学用语或图示表达正确的是( )。
3.下列过程与水解反应无关的是( )。
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下轉化为氨基酸
D.向沸水中滴入饱和FeCl3 溶液制备Fe(OH)3 胶体
4.下列事实能用平衡移动原理解释的是( )。
A.H2O2 溶液中加入少量MnO2 固体,促进H2O2 分解
B.密闭烧瓶内的NO2 和N2O4 的混合气体,受热后颜色加深
C.铁钉放入浓硝酸中,待不再变化后,加热能产生大量红棕色气体
D.锌片与稀硫酸反应过程中,加入少量CuSO4 固体,促进H2 的产生
5.回收利用工业废气中的CO2 和SO2,实验原理如图1所示。
下列说法不正确的是( )。
A.废气中SO2 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是HCO- 3的水解程度大于HCO- 3 的电离程度
C.装置a中溶液的作用是吸收废气中的CO2 和SO2
D.装置b中的总反应为SO23- +CO2+H2O=HCOOH+SO24-
6.下列离子方程式与所给事实不相符的是( )。
A.Cl2 制备84 消毒液(主要成分是NaClO):C12 + 2OH- =Cl- +C1O- +H2O
B.食醋去除水垢中的CaCO3:CaCO3+2H+ =Ca2+ +H2O+CO2↑
C.利用覆铜板制作印刷电路板:2Fe3+ +Cu=2Fe2+ +Cu2+
D.Na2S 去除废水中的Hg2+ :Hg2+ +S2- =HgS↓
7.蔗糖与浓硫酸发生作用的过程如图2所示。
下列关于该过程的分析不正确的是( )。
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
8.完成下述实验,装置或试剂不正确的是( )。
9.一种聚合物PHA 的结构简式如下,下列说法不正确的是( )。
A.PHA 的重复单元中有两种官能团
C.PHA 在碱性条件下可发生降解
D.PHA 中存在手性碳原子
10.下列事实不能通过比较氟元素和氯元素的电负性进行解释的是( )。
A.F—F键的键能小于Cl—Cl键的键能
B.三氟乙酸的Ka 大于三氯乙酸的Ka
C.氟化氢分子的极性强于氯化氢分子的极性
D.气态氟化氢中存在(HF)2,而气态氯化氢中是HCl分子
11.化合物K 与L反应可合成药物中间体M,转化关系如下。
已知L能发生银镜反应,下列说法正确的是( )。
A.K 的核磁共振氢谱有两组峰
B.L是乙醛
C.M 完全水解可得到K 和L
D.反应物K 与L的化学计量比是1∶1
12.离子化合物Na2O2 和CaH2 与水的反应分别为①2Na2O2+2H2O =4NaOH+O2 ↑,② CaH2 +2H2O = Ca(OH)2 +2H2↑。下列说法正确的是( )。
A.Na2O2、CaH2 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C.Na2O2 中阴、阳离子个数比为1∶2,CaH2 中阴、阳离子个数比为2∶1
D.当反应① 和② 中转移的电子数相同时,产生的O2 和H2 的物质的量相同
13.一种分解氯化铵实现产物分离的物质转化关系如下,其中b、d 代表MgO 或Mg(OH)Cl中的一种。下列说法正确的是( )。
A.a、c分别是HCl、NH3
B.d既可以是MgO,也可以是Mg(OH)Cl
C.已知MgCl2 为副产物,则通入水蒸气可减少MgCl2 的产生
D.等压条件下,反应①、② 的反应热之和,小于氯化铵直接分解的反应热
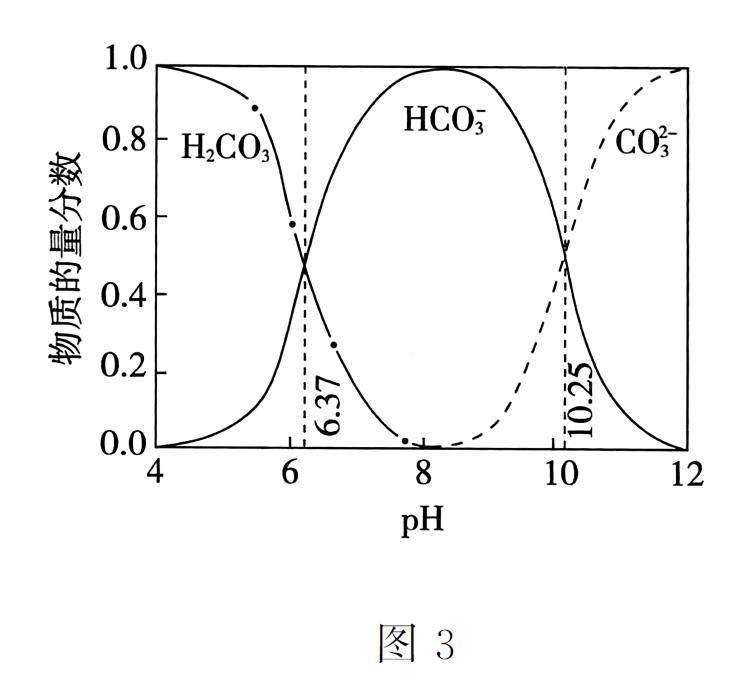
14.利用平衡移动原理,分析一定温度下Mg2+ 在不同pH 的Na2CO3 体系中的可能产物。
已知:①图3 中曲线表示Na2CO3 体系中各含碳粒子的物质的量分数与pH 的关系。
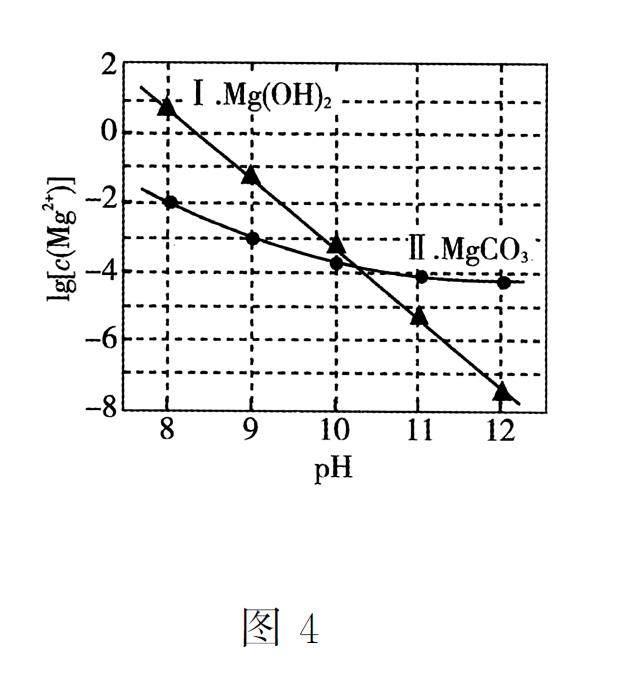
② 图4 中曲线Ⅰ 的离子浓度关系符合c(Mg2+ )·c2(OH- )=Ksp[Mg(OH)2];曲线Ⅱ 的离子浓度关系符合c (Mg2+ )·c2(CO23-)= Ksp (MgCO3 ) [注: 起始c(Na2CO3)= 0.1 mol·L-1,不同pH 下c(CO23-)由图3得到]。
下列说法不正确的是( )。
A.由圖3,pH =10.25,c(HCO- 3 )=c(CO23-)
B.由图4,初始状态pH = 11,lg[c(Mg2+ )] =-6,无沉淀生成
C.由图4,初始状态pH = 9,lg[c(Mg2+ )]= -2,平衡后溶液中存在c(H2CO3)+c (HCO3- )+c (CO23- )=0.1 mol·L-1
D.由图3 和图4,初始状态pH =8,lg[c(Mg2+ )]= - 1,发生反应:Mg2+ +2HCO- 3 =MgCO3↓+CO2↑+H2O
第二部分
本部分共5小题,共58分。
15.硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根(S2O23-)可看作是SO24- 中的 一个 O 原 子被 S 原 子取代 的产物。
(1)基态S原子价层电子排布式是_____。
(2)比较S原子和O 原子的第一电离能大小,从原子结构的角度说明理由:_____。
(3)S2O23- 的空间结构是_____。
(5)MgS2O3·6H2O 的晶胞形状为长方体,边长分别为a nm、b nm、c nm,结构如图5所示。
晶胞中的[Mg(H2O)6]2+ 个数为_____。已知MgS2O3·6H2O的摩尔质量是M g·mol-1,阿伏加德罗常数为N A,该晶体的密度为_____g·cm-3。(1 nm=10-7cm)
(6)浸金时,S2O23- 作为配体可提供孤电子对与Au+ 形成[Au(S2O3)2]3- 。分别判断S2O23- 中的中心S原子和端基S原子能否做配位原子并说明理由:_____。
16.尿素[CO(NH2)2]合成的发展体现了化学科学与技术的不断进步。
(1)十九世纪初,用氰酸银(AgOCN)与NH4Cl在一定条件下反应制得CO(NH2)2,实现了由无机物到有机物的合成。该反应的化学方程式是_____。
(2)二十世纪初,工业上以CO2 和NH3为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ.CO2 和NH3 生成NH2COONH4;
ⅱ.NH2COONH4 分解生成尿素。
结合反应过程中能量变化示意图(如图6),下列说法正确的是_____(填序号)。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.CO2(l)+2NH3(l)=CO(NH2)2(l)+H2O(l) ΔH =E1-E4
(3)近年研究发现,电催化CO2 和含氮物质(NO- 3 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3 溶液通CO2 至饱和,在电极上反应生成CO(NH2)2,电解原理如图7所示。
①电极b是电解池的_____极。
②电解过程中生成尿素的电极反应式是_____。
(4)尿素样品含氮量的测定方法如下。
已知:溶 液 中c(NH4+ )不 能 直 接 用NaOH 溶液准确滴定。
①消化液中的含氮粒子是_____。
②步骤ⅳ中标准NaOH 溶液的浓度和消耗的体积分别为c 和V,计算样品含氮量还需要的实验数据有_____。
17.化合物P 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
(1)将等体积的KI溶液加入到m mol铜粉和n mol I2(n>m)的固体混合物中,振荡。实验记录如表1所示。
①初始阶段,Cu被氧化的反应速率:实验Ⅰ_____ (填“>”“<”或“=”)实验Ⅱ。
②实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有[Cu(H2O)4]2+ (蓝色)或[CuI2]- (无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入CCl4,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是_____。
ⅱ.查阅资料,2Cu2+ +4I-=2CuI↓+I2,[Cu(NH3)2]+ (无色)容易被空气氧化。用离子方程式解释步骤b的溶液中发生的变化:_____。
③结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是CuI,实验Ⅰ中铜被氧化的化学方程式是_____。分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓KI溶液,_____(填实验现象),观察到少量红色的铜。分析铜未完全反应的原因是_____。
(2)上述实验结果,I2 仅将Cu氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了I2 能将Cu氧化为Cu2+ 。装置如图9所示,a、b分别是_____。
(3)运用氧化还原反应规律,分析在上述实验中Cu被I2 氧化的产物中价态不同的原因:_____。
【试卷整体评价】
2023年北京高考化学卷采用15+4形式(15道单选,4道大题),难度梯度设计合理,有较好的选拔功能,通过巧设情境,对考生的必备知识和关键能力进行考查,同时渗透化学学科价值。要求考生在掌握必备知识的同时,要学会知识的迁移应用,面对不同情境下的化学问题时要学会掌握一定的关键能力,应用化学学科知识解决问题,深刻感受和理解化学与社会之间的关系,感受化学学科价值。
【参考答案与解析部分】
1.A
考查目标及解析:
本题以我国科研成果单晶石墨炔为情境,考查金刚石、石墨和石墨炔等物质结构。
A 项正确,原子间优先形成σ键,三种物质中均存在σ键。
B项错误,根据成键方式,金刚石中所有碳原子均采用sp3 杂化,石墨中所有碳原子均采用sp2 杂化,石墨炔中苯环上的碳原子采用sp2 杂化,碳碳三键上的碳原子采用sp杂化。
C项错误,金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体。
D项错误,金刚石中没有自由移动电子,不能导电。
2.C
考查目标及解析:
本题以化学用语为主题考查物质结构,体现符号表征是化学基本表现方式。
3.B
考查目标及解析:
