2024年高考化学模拟试题A卷
2024-05-29高小艳冯存良
高小艳 冯存良


一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1.化学与生产、生活、科技及环境等密切相关。下列说法正确的是( )。
A.“天和”核心舱用到的镁合金涂层中的自愈缓蚀剂2-巯基苯并噻唑(C7H5NS2),属于有机高分子化合物
B.植物可以吸收利用空气中的NOx 作为肥料,实现氮的固定
C.葡萄酒中通常添加有微量SO2,既可以杀菌,又可以防止营养成分被氧化
D.我国新一代长征七号运载火箭使用的是液氧煤油发动机,煤油主要由煤的干馏制得
2.聚醋酸乙烯酯难溶于水,可用作白乳胶、塑料薄膜和涂料等,用它可得到聚乙烯醇,聚乙烯醇水溶液可用作医用滴眼液。合成路线如下。
下列说法不正确的是( )。
A.试剂a是乙酸
B.通过增加甲醇用量可提高聚乙烯醇的产率
C.由M 转化为聚醋酸乙烯酯的过程中发生了缩聚反应
D.由聚醋酸乙烯酯转化为聚乙烯醇过程中还会生成乙酸甲酯
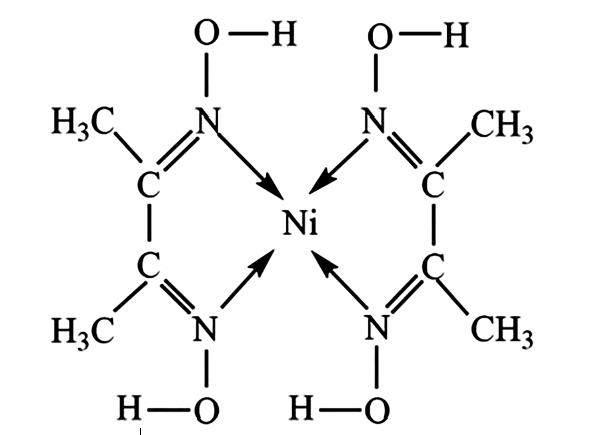
3.丁二酮肟常用于检验Ni2+ ,在稀氨水介质中,丁二酮肟与Ni2+ 反应可生成鲜红色沉淀,其结构如下所示。下列说法不正确的是( )。
A.元素H、C、N、O、Ni电负性由大到小的顺序为O>N>C>H>Ni
B.1 mol该沉淀含有σ键与π键的个数比为17∶2
C.基态Ni2+ 的价电子排布式为3d64s2
D.该沉淀中C的杂化方式为sp2、sp3
4.科学家近年发明了一种新型光电催化装置,它能将葡萄糖和CO2 转化为甲酸盐,如图1所示。光照时,光催化电极a产生电子(e- )和空穴(h+ ),图中的双极膜中间层中的H2O 会解离产生H+ 和OH- 。
下列说法错误的是( )。
①“沉渣”的主要成分除MnO2 外,还有_____。
②若加入过量的Na2S2O8,钴元素会被氧化进入“沉渣”中,则溶液中残留Co3+ 的浓度为_____mol·L-1。
(2)“沉锌”时,在近中性条件下加入Na2CO3,可得碱式碳酸锌[ZnCO3 ·2Zn(OH)2·H2O]固体,同时产生大量的气体,试分析产生大量气体的原因:_____。
(3)由碱式碳酸锌生成氧化锌的化学方程式为_____。
(4)沉锌后的滤液经过一系列操作后得到的副产品为_____(填化学式)。
(5)ZnO 的晶胞结构如图4,则锌的配位数为_____;已知晶胞参数为a cm,该晶体的密度为_____g·cm-3(写出计算式,阿伏加德罗常数的值为NA)。
9.(15分)科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究,回答下列问题:
Ⅰ.制备FeCl2。装置如图5所示(夹持装置省略),已知FeCl3 极易水解。
(1)仪器a的名称是_____。
(2)装置Ⅱ中制备FeCl2 的化学方程式为_____。
(3)该装置存在的缺陷是:①_____;②缺少氢气的尾气处理装置。
Ⅱ.利用惰性电极电解0.1 mol·L-1 FeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
(4)实验数据如表2所示。
①由实验1、2现象可以得出结论:在溶液pH 相同时,增大电压,_____优先于_____放电。
②由实验1、4现象可以得出结论:_____。
Ⅲ.为了探究外界条件对氯化銨水解平衡的影响,某兴趣小组设计了如表3所示实验方案。
(5)该实验限选药品和仪器:恒温水浴、pH 传感器、烧杯、0.1 mol.L-1 硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量”是_____。
②实验目的A 是_____。
③上述表格中,b_____d(填“>”“<”或“=”)。
10.(14分)将CO2 转化为更有价值的化工原料,正成为科学家们研究的一个重要领域。回答下列问题:
(1)已知:①2H2 (g)+ O2 (g)=2H2O(g) ΔH =- 484 kJ·mol-1
②2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1 353 kJ·mol-1
