高考工艺流程题中反应条件的控制
2024-05-26杨涛
杨涛


高考工艺流程题常以工业生产、社会热点、科技前沿为命题情景,体现无情景不命题的思想。试题主要考查学生元素化合物、化学反应原理相关知识,应用理论知识解决实际生产问题的核心素养,旨在培养学生的安全意识和严谨求实的科学态度。试题中反应条件的选择主要从以下5个方面考查。
一、温度的控制
化工生产工艺中温度控制的作用及温度选择见表1。
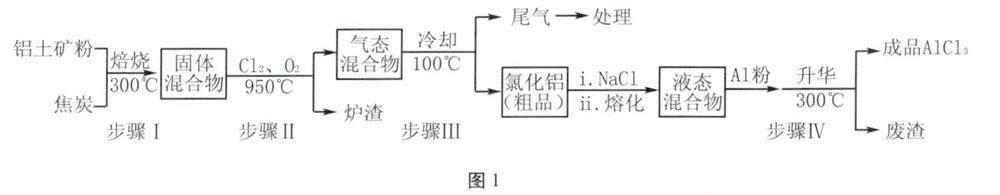
例题1 (2015年福建卷节选)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的工艺流程示意图如图1所示,部分物质沸点见表2。
(4)步骤Ⅲ的尾气经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为____。
解析 温度:该流程图中出现了4次具体的温度,问题(4)设置上也与温度有关。
步骤Ⅰ中焙烧300℃目的是:使固体水分挥发,防止步骤Ⅱ生成的AlCl3水解;焦炭气孔数日增多,目的是增大接触面积,加快反应速率;
步骤Ⅱ中焙烧950℃目的是分离出SiCl4、AlCl3、FeCl3气体。
步骤Ⅲ冷却到100℃目的是分离出SiCl4气体得到AlCl3、FeCl固体。
步骤Ⅳ300℃目的是将产品升华得到AlCl3
(4)中出现的温度:室温。步骤Ⅲ的气态混合物冷却至100℃时AlCl3、FeCl3液化;尾气冷却到室温后,SiCl4成为液体。此时的气体中能与氢氧化钠反应的是Cl2和CO2,分析写出产物。
答案:NaCl、NaClO和Na2CO3
二、pH的控制
生产过程中,控制溶液pH的作用见表3。
例题2 (2020年新课标Ⅰ节选)黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用图2所示工艺流程可由黏土钒矿制备NH4VO3。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH见表4。
解析 “酸浸氧化”中,VO+和VO2+被氧化成VO2+;“中和沉淀”中,钒水解并沉淀为V2O5·xH2O;“沉淀转溶”中,V2O5·xH2O转化为钒酸盐溶解。
题干pH调控过程是:钒矿粉先酸浸,再加碱由小到大调pH,再加酸凋pH由大到小。
“酸浸氧化”中,硫酸溶解Fe3O4,生成的产物Fe2与MnO,反应生成Fe3+和Mn2+,VO+和VO2+被MnO2氧化成VO2+,同时除去SiO2。
pH由小升高:滤液①用NaOH调pH为3.0 -3.1时,沉淀了大部分的Fe3+和小部分的铝离子,得到V2O5· xH2O
pH继续升高:滤饼②中含氢氧化铁、氢氧化铝和V2O5·xH2O,滤饼②在pH>13的NaOH环境中发生沉淀转溶,溶解了全部的氢氧化铝,同时有V2O5·xH2O转化为钒酸盐溶解的过程,氧氧化铁作为滤渣③被过滤除去。
pH由大往小调:滤液③加HCl调pH为8.5,将NaAlO2转化为Al(OH)3沉淀过滤除去。该流程的特殊性,Al3+和Fe3+不是一步被除净的。
解题过程看表格数据,理解调控pH的目的,解决题目的问题。
三、浓度的控制
化丁生产中,原料液浓度控制的作用见表5。
例题3 (2016年上海卷节选)乙酸乙酯广泛用于药物、染料、香料等工业。实验时,通常加入过量的乙醇,原因是____。
答案:增大乙酸的转化率,有利于平衡正移动。
四、压强的控制
化工生产中,控制压强的作用见表6。
五、体系环境氛围及其他条件的控制(见表7)
例题4 (2023年广东卷节选)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。(NH4)2CO3提高了Ni、Co的浸取速-,其原因____。
答案:減少胶状物质对镍钴氢氧化物的包裹,防止生成胶体,加速沉淀的生成。
(收稿日期):2023-10-25)
