基于分子动力学的SiC化学机械磨削材料去除机理研究*
2024-05-21龚福潜朱博恩章博阳许荣滨
□ 龚福潜 □ 吴 柯 □ 朱博恩 □ 章博阳 □ 许荣滨
1.宁波大学 机械工程与力学学院 浙江宁波 315211
2.浙江五洲新春集团股份有限公司 浙江绍兴 312500
1 研究背景
SiC具有耐高温、硬度高、强度高、化学性质稳定等优点,在半导体、精密仪器、电子器件、集成电路等领域应用广泛[1]。SiC作为第三代半导体材料的典型代表,是发展大功率器件、高频高温器件、抗强辐射器件、蓝光激光器、紫外探测器等技术的核心,也是目前晶体生长领域的主流衬底材料之一[2-6]。
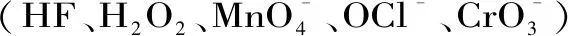
针对化学机械抛光的缺点,周立波等[15]提出了化学机械磨削技术。化学机械磨削具有面型精度和表面质量可控性较强、磨料利用率较高、加工效率较高等优点[16-18]。Wu Ke等[19]采用Cr2O3磨粒对蓝宝石进行化学机械磨削加工,对化学机械磨削过程中的固相生成物进行X射线光电子能谱分析,发现Cr2O3磨粒和蓝宝石会反应生成一种复杂的软质Cr-Al-O三元化合物。通过磨粒的机械作用实现软质层的去除,可以实现蓝宝石的平坦化加工。化学机械磨削技术已经成功应用于硅片、石英玻璃、K9光学玻璃等硬脆材料的平坦化加工[20-22],但是,目前少有文献研究SiC的化学机械磨削加工及材料去除机理。
笔者采用Lammps分子动力学仿真软件建立O2环境中SiO2磨料对SiC的化学机械磨削原子模型,通过仿真揭示化学反应机理,分析化学机械磨削过程中磨削温度和O2浓度对SiC氧化程度的影响,以及磨削深度、磨削速度、磨料半径对摩擦力和原子去除数量的影响,为实现SiC的化学机械磨削加工提供理论依据。
2 建模
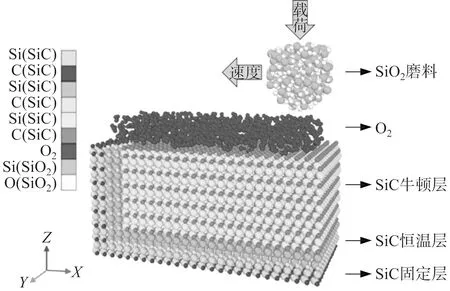
图1 总体仿真模型
3 仿真过程
(1) SiO2磨料顶端两层原子设为移动层,用于施加磨削深度和磨削速度。
(2) 初始化时,整个系统在300 K环境中弛豫2.5 ps。
(3) O2分子和SiC进行化学反应。
(4) SiO2磨粒以一定速度下向-Z轴方向移动,在SiC表面压入一定深度,然后以100 m/s的速度向-X轴方向移动。
(5) 用Ovito可视化软件分析仿真结果。
4 弛豫分析
采用正则系统,仿真参数见表1,温度控制类型为Nose-Hoover thermostat,X、Y向为周期性边界,Z向为固定性边界。弛豫过程的体系势能变化曲线如图2所示。弛豫初期体系势能急剧下降,弛豫中期体系势能呈缓慢下降,在2 ps,即8 000步后,势能逐渐达到平稳状态。

表1 仿真参数

图2 弛豫过程体系势能变化曲线
5 SiC在O2环境中反应机理
Si原子和O原子反应机理如图3所示。弛豫阶段后化学反应初期3.5 ps时,O1和O2原子在磨料的机械作用下进入SiC表面原子中,SiC表面原子的共价键强度降低。4 ps后,O2原子逐渐向SiC表面的Si1原子靠近,随后O2原子和Si1原子形成Si1-O2键,SiC晶体结构变得不稳定。5 ps时,O1原子和C1原子形成C1-O1键,并且O1原子和O2原子共价键逐渐拉长。6.7 ps后,O1原子和O2原子共价键完全断裂,形成由Si1-O2键组成的SiO氧化物。7.5 ps时,O3原子以相同的形式和Si1成键,形成由O2-Si1-O3键组成的SiO2氧化物。7.5 ps后,SiC表面持续生成由SiO2和SiO组成的软质氧化膜。SiO2和SiO生成数量如图4所示。随着化学反应的进行,SiC逐渐被氧化,SiC表面的SiO2和SiO氧化物数量逐渐增加。
微课还可以将教师从实验教学中解放出来,更多的与学生进行互动。在进行实验教学时,先使用传统教学方式讲解知识点,让学生了解原理,再让学生观看微课实验视频。此时,老师可以走到学生中巡视,观察他们在看微课时的反应,及时为他们答疑解惑,针对实验中出现的问题,进行讨论和分析,从而使教学更加的有效充实。
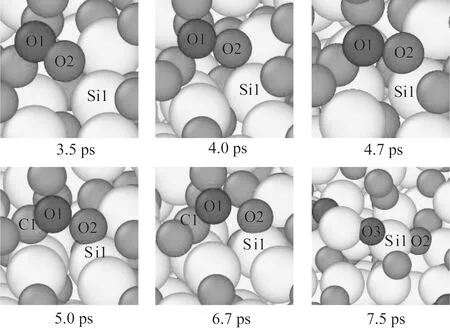
图3 Si原子和O原子反应机理

图4 SiO2和SiO生成数量
C原子和O原子反应机理如图5所示。在反应初期3 ps时,O1和O2原子在SiO2磨料的机械作用下进入SiC表面原子中。3.3 ps后,O1原子逐渐向C1原子靠近,随后O1原子、C1原子和Si1原子形成O1-C1-Si1键,C1-Si1键变得不稳定。4.6 ps时,O2原子和C2原子形成C2-O2键,O1原子和O2原子的共价键断裂。5 ps后,由于SiO2磨料的机械作用,C1-Si1键逐渐拉伸,随后O1-C1-Si1键断裂,O1原子和C1原子以CO的形式脱离SiC表面。5.5 ps后,SiC表面持续反应生成CO2和CO气体,脱离SiC表面。CO2和CO生成数量如图6所示。随着化学反应的进行,O原子和C原子反应生成CO2和CO气体的数量逐渐增加,并脱离SiC表面。同理,O原子和Si原子发生化学反应,生成软质氧化膜,在机械作用下实现氧化膜的去除。随后O原子会继续和SiC表面的C原子、Si原子发生化学反应,形成连续的反应过程。SiC会和O2发生化学反应,生成Si-O氧化膜和C-O气体,固相反应方程式为[23]:
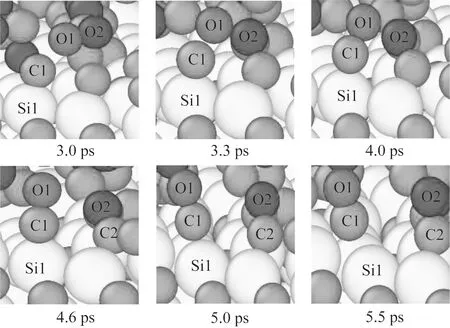
图5 C原子和O原子反应机理

图6 CO2和CO生成数量
SiC(s) + 3/2O2(g) → SiO(s) + CO(g)
2SiC(s) + 3O2(g) → 2SiO2(s) + 2CO(g)
SiC(s) + 2O2(g) → SiO2(s) + CO2(g)
6 磨削温度对化学反应影响
磨削温度对O2消耗量影响如图7所示,对Si-O键生成数量影响如图8所示,对CO2和CO生成数量影响如图9所示。当磨削温度相对较低时,由于温度的提高对SiC的表面活化能影响较小,O2分子扩散速率较低,因此O2消耗量相当,约为300个,Si-O键生成数量约为370个,CO2和CO生成数量约为140个。当磨削温度提高到1 600 K时,O2分子的扩散速率明显提高,从而降低SiC的表面活化能,提高化学反应速率,O2消耗量为342个,Si-O键生成数量约为440个,CO2和CO生成数量约为145个[24]。相同磨削温度下,在反应初期,由于SiO2磨粒和SiC表面的机械作用,大量O2进入SiC表面,O2消耗速度约为40个/ps。随着化学反应的进行,SiC表面生成氧化膜,阻碍O2和SiC的进一步化学反应,O2消耗速度减缓,约为7个/ps。同理,反应初期CO2和CO的生成数量较多,约为120个,随后CO2和CO的生成数量趋于平稳,约为140个,而Si-O键生成数量在反应过程中持续增加。由于化学作用强于机械作用,SiC表面逐渐被氧化膜覆盖。随着化学反应的进行,处于不饱和状态的Si原子、O原子、C原子在SiO2磨粒的机械作用下,逐渐生成Si-O键和C-O键。由于Si-O键比C-O键的键能高,成键稳定,因此Si-O键的生成数量多于C-O键的生成数量。
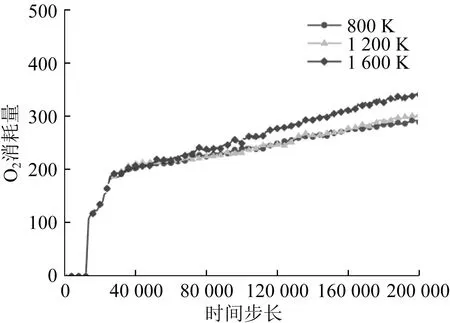
图7 磨削温度对O2消耗量影响
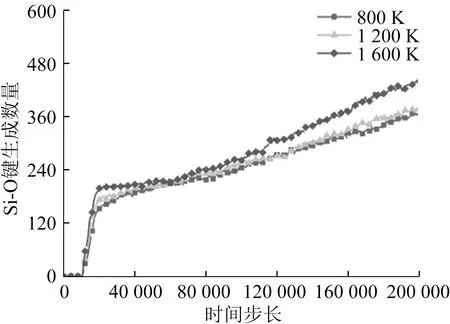
图8 磨削温度对Si-O键生成数量影响
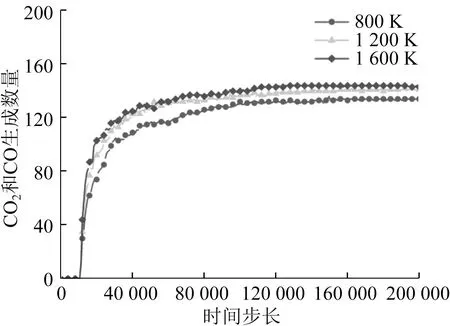
图9 磨削温度对CO2和CO生成数量影响
磨削温度对SiC径向分布函数影响如图10所示。弛豫时,SiC径向分布函数第一峰的峰值高,曲线窄,表明SiC保持晶体状态,内部结构稳定,Si-C键的键长约为1.89 Å。随着磨削温度的提高,径向分布函数的峰值逐渐减小,曲线逐渐变宽,由有序变无序,表明随磨削温度对O原子均方位移影响如图11所示,对Si原子均方位移影响如图12所示,对C原子均方位移影响如图13所示。弛豫阶段,原子位移量几乎不发生改变,不发生化学反应。随着化学反应的进行,SiC表面的Si原子和C原子发生位移,晶体结构变得不稳定,SiC表面被氧化。随着磨削温度的提高,O原子、Si原子、C原子均方位移增大,表明磨削温度提高对SiC化学反应有促进作用。相同磨削温度下,Si原子和C原子在反应初期均方位移相当,约为9 Å2。随着反应的进行,Si原子和O原子反应生成的SiO2和SiO覆盖在SiC表面,Si原子均方位移变得平稳,约为11 Å2。C原子和O原子反应生成的CO2和CO脱离SiC表面,因此C原子均方位移持续增大。
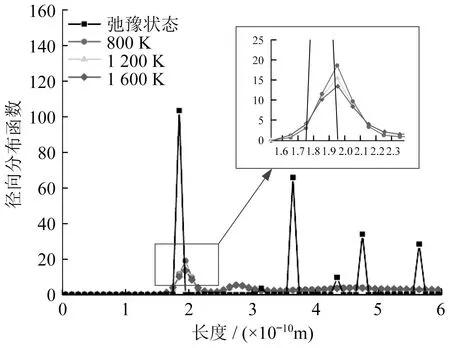
图10 磨削温度对SiC径向分布函数影响

图11 磨削温度对O原子均方位移影响
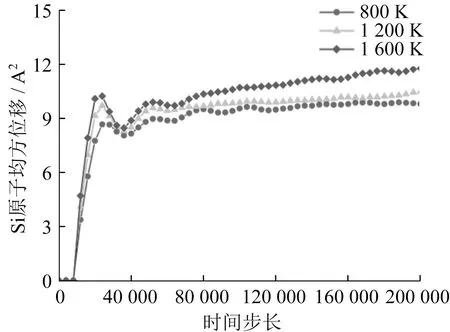
图12 磨削温度对Si原子均方位移影响
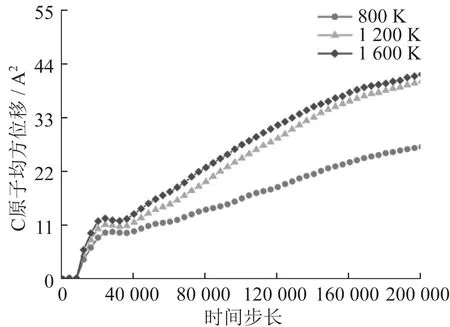
图13 磨削温度对C原子均方位移影响
着磨削温度的提高,化学反应速率加快,Si-C键断裂数量增加,SiC表面非晶化程度变高,此时Si-C键的键长约为1.95 Å。
7 O2浓度对化学反应影响
O2浓度对O2消耗量影响如图14所示,对Si-O键生成数量影响如图15所示,对CO2和CO生成数量影响如图16所示。随着O2浓度的增大,O2消耗量和化学反应产物生成数量均增加。反应过程中,600个O2浓度环境中Si-O键生成数量为376个,反应速率约为7.9个/ps,CO2和CO生成数量为133个,反应速率约为2.8个/ps。由于600个O2浓度未达到饱和,因此化学反应产物生成数量和速率低于900个O2浓度和1 200个O2浓度。反应初期,900个O2浓度和1 200个O2浓度达到饱和,化学反应速率相当,Si-O键生成数量约为390个,反应速率约为17.3个/ps,CO2和CO生成数量约为155个,反应速率约为6.8个/ps。随着化学反应的进行,O2浓度从饱和状态变为不饱和状态,1 200个O2浓度剩余O2浓度较大,因此Si-O键生成数量、化学反应产物生成数量较多,化学反应速率较快。1 200个O2浓度环境中,Si-O键生成数量共为598个,CO2和CO生成数量共为191个,多于900个O2浓度环境中。
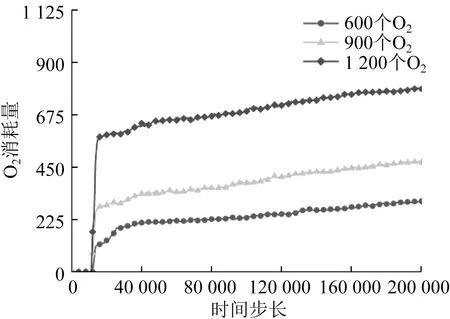
图14 O2浓度对O2消耗量影响

图15 O2浓度对Si-O键生成数量影响

图16 O2浓度对CO2和CO生成数量影响
O2浓度对SiC径向分布函数影响如图17所示。随着O2浓度的增大,Si-C键断裂数量增加,峰值逐渐减小,曲线逐渐变宽,表明增大O2浓度可以提高SiC的非晶化程度。
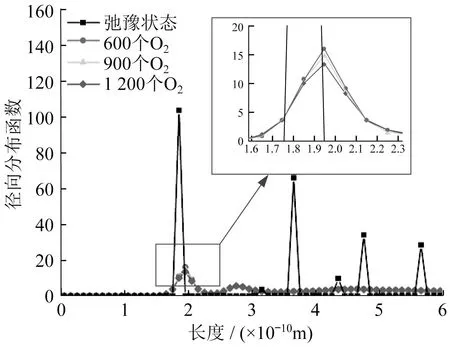
图17 O2浓度对SiC径向分布函数影响
O2浓度对O原子均方位移影响如图18所示,对Si原子均方位移影响如图19所示,对C原子均方位移影响如图20所示。随着O2浓度的增大,O原子、Si原子、C原子均方位移均增大,化学反应速率加快。600个O2浓度环境中,由于O2浓度未饱和,化学反应速率较慢,O原子均方位移为635 Å2,Si原子均方位移为10 Å2,C原子均方位移为40 Å2,O原子、Si原子、C原子均方位移小于900个O2浓度和1 200个O2浓度环境中。反应初期,900个O2浓度和1 200个O2浓度环境中,O原子、Si原子、C原子的均方位移相当,此时O2浓度达到饱和状态,化学反应速率相当。随着化学反应的进行,O2浓度逐渐减小,并由饱和状态变为不饱和状态,1 200个O2浓度剩余O2浓度较大,因此O原子、Si原子、C原子均方位移较大,SiC氧化程度较高。
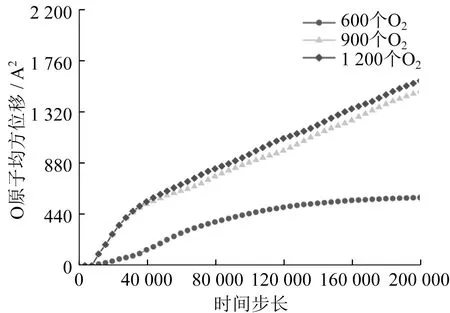
图18 O2浓度对O原子均方位移影响
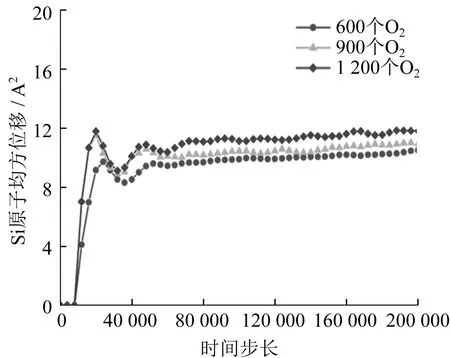
图19 O2浓度对Si原子均方位移影响
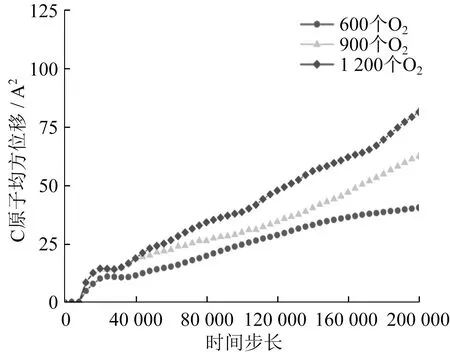
图20 O2浓度对C原子均方位移影响
8 磨削参数对摩擦力和原子去除影响
磨削深度对摩擦力影响如图21所示,磨削速度对摩擦力影响如图22所示,磨料半径对摩擦力影响如图23所示。当磨削深度从2 Å增大到6 Å时,磨粒与SiC的实际接触面积增大,摩擦力增大2倍,从600 nN增大到1 800 nN。由于磨削速度的提高不影响磨料与SiC的实际接触面积,因此磨削速度对摩擦力的影响较小。相较于磨削深度,磨料半径对磨粒与SiC的实际接触面积影响较大,因此当磨料半径从10 Å增大到15 Å时,摩擦力增大2.5倍。磨削参数对原子去除数量影响见表2。当磨削深度从2 Å增大到6 Å时,磨料和SiC之间相互摩擦和挤压的有效原子数量增加,因此原子去除数量明显增加,从98个增加到265个。磨削速度提高促使脱离SiC基体的原子运动距离更远,从而减小弹性恢复所需的距离,缩短对应时间,因此原子去除数量略微增加,从140个增加到171个[25]。当磨料半径从10 Å增大到15 Å时,由于磨削深度未改变,磨料两侧与SiC接触的原子数量增加,而磨料和SiC之间接触的有效原子数量未增加,因此原子去除数量变化不明显。
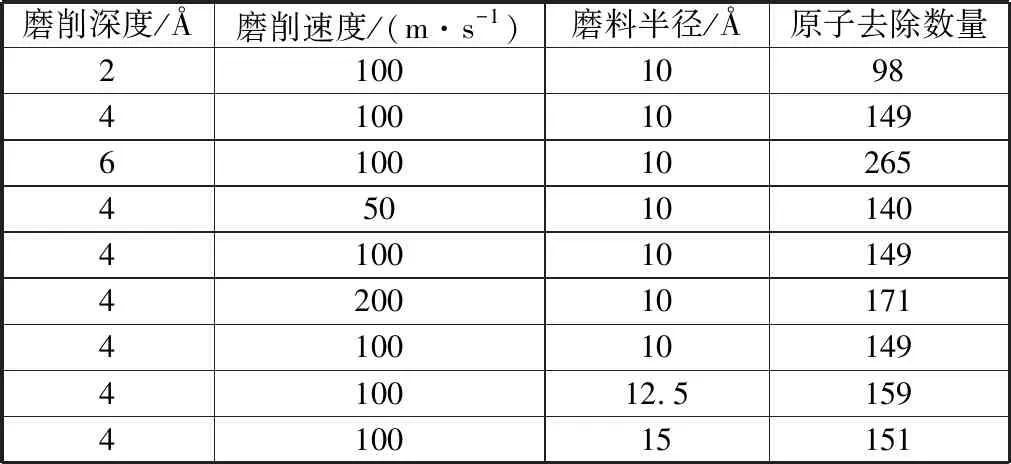
表2 磨削参数对原子去除数量影响
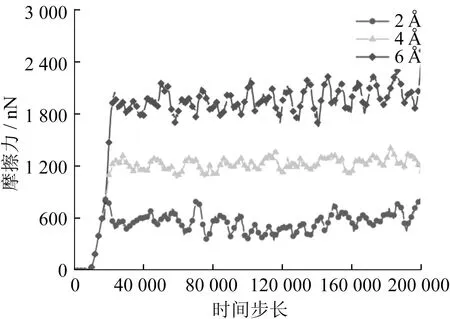
图21 磨削深度对摩擦力影响
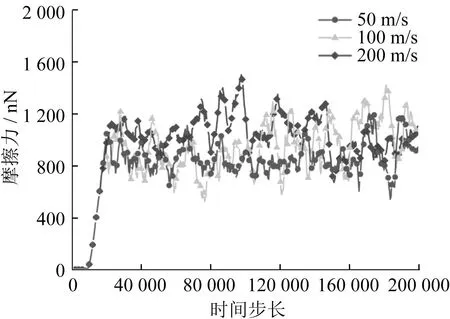
图22 磨削速度对摩擦力影响
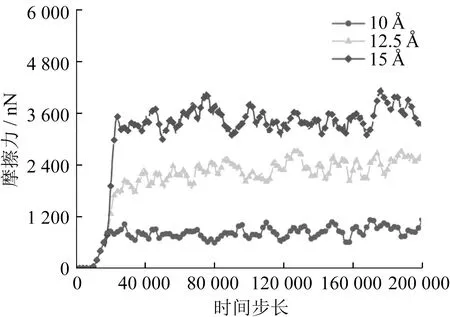
图23 磨料半径对摩擦力影响
9 结论
采用Lammps分子动力学仿真软件研究在O2环境中SiO2磨料对SiC化学机械磨削过程中的材料去除机理,分析不同磨削温度和O2浓度对化学反应产生的影响,以及不同磨削参数对摩擦力和原子去除数量的影响。
在O2环境中,SiC表面的Si原子和O原子反应生成SiO2和SiO氧化膜,并在磨料的机械作用下进行去除。C原子和O原子反应生成CO2和CO,并脱离SiC表面。
磨削温度的提高有利于加快SiC的氧化速率。O2浓度未达到饱和时,随着O2浓度的增大,化学反应速率加快。O2浓度达到饱和时,随着O2浓度继续增大,化学反应速率相当,当O2浓度减小至不饱和状态时,剩余O2浓度越大,化学反应速率越快。
磨削深度和磨料半径的增大使磨粒与SiC的实际接触面积增大,因此摩擦力逐渐增大。磨削速度的变化对摩擦力的影响不大。磨削深度的增大对原子去除数量增加有明显作用,磨削速度的提高对原子去除数量增加有略微作用。磨削深度相同时,随着磨料半径的增大,原子去除数量变化不明显。
